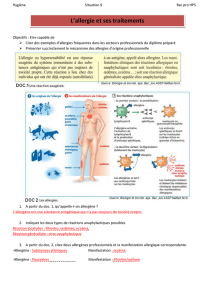
Dermatite atopique. La question.

In «Dermatologie et infections sexuellement transmissibles » Saurat, Grosshans, Laugier, Lachapelle, 5° édition, Masson, 2008 in press
Dermatite atopique
A. Taïeb
Généralités
Le terme de dermatite atopique (DA) ou eczéma atopique désigne les manifestations inflammatoires cutanées chroniques
et/ou récidivantes associées à l’atopie, trait héréditaire polygénique très prévalent, dont les diverses manifestations cliniques
(dermatite atopique, rhinite allergique et asthme) touchent environ un tiers de la population générale. Si le phénotype cutané
de l’atopie (dermatite/eczéma) est facilement identifiable, il nécessite, si on le soumet à une analyse descriptive, de proposer
des critères de diagnostic qui sont cliniques et surtout anamnestiques. Les critères de Hanifin et Rajka [1] ont été revus,
simplifiés et validés [2] (tableau 2.11).
Tableau 2.11 –Critères de diagnostic de l’United-Kingdom working party [2]
Critère obligatoire : dermatose prurigineuse ou parents rapportant
que l’enfant se gratte ou se frotte
Associé à trois ou plus des critères suivants :
1. Antécédents personnels de dermatite des plis de flexion (fosses
antécubitales, creux poplitée, face antérieure des chevilles, cou)
et/ou des joues chez les enfants de moins de 10 ans.
2. Antécédents personnels d’asthme ou de rhume des foins (ou
antécédents de maladie atopique chez un parent au premier degré
chez l’enfant de moins de 4 ans).
3. Antécédents de peau sèche généralisée au cours de la dernière
année.
4. Eczéma des grands plis visible ou eczéma des joues, du front et
des convexités des membres chez l’enfant au-dessous de 4 ans.
5. Début des signes cutanés avant l’âge de 2 ans (critère utilisable
chez les plus de 4 ans uniquement).
L’atopie est une prédisposition héréditaire du système immunitaire à privilégier des réactions d’hypersensibilité médiées par
les immunoglobulines E (IgE) vis-à-vis d’antigènes communs dans l’alimentation, l’environnement extérieur ou domestique.
Facteurs allergiques
Les antigènes susceptibles de déclencher une hypersensibilité IgE-dépendante, ou allergènes, sont suffisamment spécifiques
du phénomène atopique pour être dénommés atopènes. Ils varient cependant selon les conditions socioculturelles et
d’environnement des populations étudiées. Ainsi, le riz est un atopène au Japon et le pollen de bouleau en Scandinavie.
Cependant, certains atopènessont ubiquitaires dans les zones tempérées, comme l’allergène majeur de l’acarien domestique
(Dermatophagoides pteronyssinus).La pénétration des atopènes est possible à travers la peau et les muqueuses, malgré un
poids moléculaire élevé, en raison d’une activité protéasique intrinsèque.
En fonction de la voie de pénétration, on distingue les aéroallergènes qui peuvent être inhalés ou agir au contact de la peau et
les trophallergènes ingérés, des réactions croisées pouvant survenir entre des atopènes inhalés et ingérés (pollen de bouleau et
pomme, par exemple). Dans une population déterminée, les sensibilisations aux atopènes ont une prévalence variable selon
l’âge, qui tient grossièrement compte du mode, de la chronologie et de la fréquence d’exposition : les trophallergènes sont les
plus prévalents chez le nourrisson, puis les aéroallergènes deviennent majoritaires chez l’enfant et l’adulte. La peau est
facilement pénétrée en raison de prédispositions génétiques, mieux identifiées récemment dans la population européenne, et
un lien de causalité existe par ce biais entre l’atteinte cutanée et les atteintes muqueuses –asthme et rhinite- (3).
Cette évolution chronologique des sensibilisations (et des tolérances) est à corréler à l’atteinte des organes cibles de
l’atopie. La notion de cible variable dans le temps (fig. 2.10) de l’atopie reste cependant globalement une énigme (cf. infra
«Physiopathologie»). Elle pourrait être en relation avec la maturation, le délai et le degré d’exposition des diverses barrières
épithéliales (digestive, respiratoire, cutanée). Celles-ci comportent chacune un système immunitaire spécifique et sont
soumises à des facteurs locaux particuliers d’irritation ou d’inflammation non spécifiques (par exemple, textiles, irritants de
contact et flore microbienne pour la peau, aliments et agents infectieux pour le tube digestif, pollution atmosphérique et virus
pour les bronches et les voies aériennes supérieures).
Fig. 2.10 –Atteinte des organes cibles de l’atopie en fonction de l’âge (d’après [4]).

Dermatite atopique intrinsèque. Pour éviter d’être trop schématique, il faut signaler que, de façon minoritaire, le phénotype
«dermatite atopique» peut être dissocié de réactions IgE-dépendantes chez certains patients surtout adultes. On a suggéré le
terme de dermatite atopique intrinsèque ou non allergique pour ces patients, en les opposant comme pour l’asthme aux formes
extrinsèques communes, au mode de déclenchement allergénique prépondérant. Ces patients, par ailleurs atteints d’une forme
de dermatite cliniquement indiscernable, pourraient avoir une inflammation cutanée de déclenchement différent,
irritant,neurogène, ou auto-immun.
Comment met-on en évidence l’hypersensibilité IgE-dépendante? Les tests cutanés aux atopènes à lecture immédiate (prick
tests) mettent en évidence directement la dégranulation des mastocytes cutanés porteurs d’IgE spécifiques. Le dosage des IgE
sériques spécifiques reflète indirectement cette hypersensibilité. Celle-ci peut conduire à des réactions allergiques
immédiates, de démonstration clinique par des tests de provocation orale par exemple pour les allergies alimentaires [5]. Des
réactions retardées peuvent être mises en en évidence par des tests épicutanés aux aéroallergènes (atopy patch test).Chez le
nourrisson, la positivité des tests épicutanés précède la positivité des pricks tests et des IgE spécifiques (6).
Facteurs génétiques et environnementaux
Les études génétiques de l’atopie sont difficiles du fait de la variabilité du phénotype selon la chronologie, mais aussi la
gravité, ce qui rend plus difficile l’identification des formes frustes.Cinquante à 70 % des patients atteints de dermatite
atopique ont un parent au premier degré atteint de dermatite atopique, d’asthme ou de rhinite allergique, en comparaison avec
20 à 35 % pour les sujets non atopiques. Il existe un certain degré de spécificité d’organe cible dans la transmission du trait
atopique : dans leur descendance, les patients atteints de DA ont 50 % de leurs enfants atteints de DA et jusqu’à 80 % en cas
de mariage entre deux parents atteints de DA; 72 % des jumeaux homozygotes sont concordants pour le phénotype atopique
contre 23 % pour les jumeaux dizygotes [7]. Les mutations perte de fonction de la filaggrine associées à l’ichtyose vulgaire,
sont trouvées à l’état hétérozygote ou homozygote chez 30% des patients européens, sans lien évident avec la gravité de la
maladie (3, 8).
Toutes les études épidémiologiques menées en particulier en Europe indiquent une augmentation rapide de prévalence des
maladies rattachées à l’atopie. La dermatite atopique est présente chez 10 à 25 % des enfants dans les études nord-
européennes récentes, alors que les enquêtes des années soixante indiquaient des prévalences aux environs de 5 % . Ces
données sont interprétées comme reflétant l’influence de l’environnement sur le génotype.Les pays à haute prévalence sont en
train de voir celle-ci se stabiliser, ce qui correspond peut-être à une saturation de l’atteinte de la population génétiquement à
risque (9).
L’hypothèse la plus souvent avancée pour expliquer la prévalence accrue de l’atopie concerne l’urbanisation des populations
et le style de vie dit occidental. En période périnatale, la microflore intestinaleet plus généralement les stimulus microbiens de
l’immunité innée, comme le lipopolysacharide (LPS) présent dans les endotoxines abondantes en milieu rural, ont un rôle
globalement protecteur [10]. Le rôle de la colonisation cutanée staphylococcique, quasi constante chez l’atopique, est
probablement majeur dans la polarisation TH2 de la réponse immune (11). D’autres facteurs interviennent : le mode d’habitat
occidental mieux isolé et moins bien ventilé favorise l’exposition aux atopènes d’intérieur (acariens, animaux domestiques),
les habitudes alimentaires et hygiéniques (introduction précoce de trophallergènes, lavage souvent excessif de la peau),
l’exposition aux irritants comme le tabac et aux polluants automobiles ou industriels…
Les études sont rendues difficiles par le nombre de facteurs à prendre en compte, et qui peuvent biaiser l’analyse, et les
facteurs génétiques majeurs n’ont pas pu être pris en compte en raison de leur découverte récente. Un niveau
socioéconomique élevé est par exemple un facteur de risque démontré mais d’explication non univoque, car associant des
comportements complexes : grossesses plus tardives, enfants gardés en communauté en bas âge quand la mère travaille,
confort thermique de l’habitation, expositions allergéniques accrues alimentaires (diversification précoce) ou
aéroallergéniques (voyages plus fréquents)…
Histologie
Le mot dermatite ou eczéma est commode pour regrouper des aspects sémiologiques divers, mais qui ont un trait
histopathologique commun. Il est rare cependant, compte tenu de la spécificité de la combinaison des critères sémiologiques

In «Dermatologie et infections sexuellement transmissibles » Saurat, Grosshans, Laugier, Lachapelle, 5° édition, Masson, 2008 in press
et anamnestiques, d’avoir à pratiquer une biopsie pour diagnostiquer une DA. Ce geste a plutôt pour but d’éliminer une autre
affection.
L’aspect histologique comporte une atteinte épidermique prédominante avec un afflux de lymphocytes T (exocytose) qui
s’accompagne d’un œdème intercellulaire (spongiose) réalisant des vésicules microscopiques. Ces vésicules sont
exceptionnellement visibles macroscopiquement et c’est leur rupture à la surface de la peau qui détermine le caractère suintant
et croûteux des lésions, et constitue un excellent milieu de culture pour les contaminants bactériens.. Du fait du grattage,
l’épiderme s’épaissit (lichénification) et devient, chez l’enfant et l’adulte moins susceptible à un suintement issu de vésicules
microscopiques. Dans ce cas, les excoriations peuvent cependant déterminer des brèches épidermiques et une exsudation
secondaire.
Le derme superficiel comporte un infiltrat mononucléé périvasculaire. La dilatation des capillaires superficiels est responsable
de l’érythème et l’extravasation de protéines plasmatiques de l’œdème cutané (papules œdémateuses). De façon plus
caractéristique dans la DA que dans des eczémas de contact, des éosinophiles dégranulés sont objectivables mais uniquement
par immunohistochimie (présence de major basic protein).
BIBLIOGRAPHIE
[1] Hanifin J.M. et coll., Acta Dermatovener., 1980, suppl. 92, 44.
[2] Williams H.C. et coll., Br. J. Dermatol., 1994, 131, 406.
3. Palmer CN et coll. Nat Genet. 2006;38:441-6
[4] Rajka G., Essentials aspects of atopic dermatitis, Springer, Berlin, 1990.
[5] Sampson S.A. et coll., J. Pediatr., 1989, 115, 23.
6. Boralevi T et coll, Allergy, 2008
[7] Schultz-Larsen F. et coll., J. Am. Acad. Dermatol., 1993, 28, 719.
8. Hubiche T. et coll, Acta Derm. Venereol.2007;87:499.
9. Williams Het coll J Allergy Clin Immunol. 2007 Dec 20
[10] Braun-Fahrlander C et coll, N. Engl. J. Med., 2002, 347, 869.
11. Mandron M et coll.J Allergy Clin Immunol. 2006;117:1141
Physiopathologie --------------------------------------------------------------------------------------------------------
A.Hennino, F. Bérard, J.-F. Nicolas
L’eczéma de la dermatite atopique est du à l’activation dans la peau de lymphocytes T spécifiques d’antigènes. L’eczéma est
donc une réaction d’hypersensibilité retardée. Les antigènes sont des pneumallergènes capables de pénétrer l’épiderme dans
le cas des DA extrinsèques ou des autoantigènes épidermiques dans la cas des DA intrinsèques [1-3]. D’autres facteurs non
spécifiques concourent au développement et à la pérennisation des poussées (infectieux, neuromédiateurs).
Les avancées les plus remarquables sont :
-la caractérisation de l’anomalie génétique de la DA extrinsèque. Elle touche la production de la filaggrine, une molécule
nécessaire à la constitution de la couche cornée [4]. Ceci explique que les patients DA ont un trouble de la barrière cutanée
autorisant le passage de molécules de haut poids moléculaire dont les pneumallergènes. Cette pénétration facilitée des
allergènes est à l’origine de la sensibilisation et du déclenchement des poussées.
-l’analyse des LT à l’origine des lésions d’eczéma. Les travaux dans les modèles expérimentaux de DA, comme ceux dans
l’asthme, montrent que les LT CD8+ sont nécessaires à l’initiation des lésions [5]. Ces observations confirment les
similitudes entre eczéma allergique de contact et eczéma de la DA [6]et remettent en cause le dogme Th1/Th2 dans la
physiopathologie de la DA et de la maladie atopique en général [7].
ÉVOLUTION DES CONCEPTS
Le paradoxe. La compréhension des mécanismes immunologiques à l’origine des lésions d’eczéma s’est heurtée pendant de
nombreuses années à l’absence de lien établi entre l’aspect anatomoclinique et les anomalies biologiques et immunologiques
caractéristiques de l’affection. En effet, la lésion d’eczéma correspond à une réaction d’hypersensibilité (HS) retardée
(hypersensibilité de type IV de Gell et Coombs encore dénommée immunité cellulaire) et l’hyper-IgE observée chez la
majorité des patients atopiques est habituellement responsable de manifestations d’HS immédiate (immunité humorale). La
présence d’IgE sériques à taux élevés pourrait expliquer les troubles vasomoteurs et l’urticaire mais en aucun cas l’eczéma.
C’est pour cela que la DA ne peut être assimilée à une maladie allergique IgE [8]
Les progrès. La connaissance de la physiopathologie de l’eczéma de la DA a connu des progrès remarquables en raison de
plusieurs observations qui confirment que la peau peut être le site de sensibilisation et d’expression de la maladie:

–la caractérisation des lymphocytes T spécifiques d’allergène a souligné les similitudes et les différences entre DA et eczéma
de contact [7, 9];
–l’effet thérapeutique spectaculaire des immunosuppresseurs systémiques (ciclosporine, méthotrexate) et topiques
(tacrolimus, pimecrolimus) a démontré que l’eczéma de la DA est dû à l’activation de lymphocytes T dans la peau des
patients;
–l’observation d’eczéma au site du contact des tests épicutanés aux allergènes a permis de définir l’eczéma de la DA comme
un eczéma de contact aux protéines de l’environnement [10]. Ces DA correspondent aux DA dites «extrinsèques»
(allergiques) par analogie à la maladie asthmatique; il faut cependant noter que seul un nombre restreint de patients
présentent de tels tests cutanés positifs. Ces DA sont volontiers associées à d’autres manifestations atopiques (asthme, rhinite
et conjonctivite). On comprend ainsi facilement que la DA soit permanente chez les patients sensibilisés aux allergènes
perannuels (dermatophagoides de la poussière de maison, allergènes des moisissures, allergènes d’animaux domestiques) et
qu’elle soit saisonnière chez les patients sensibilisés aux allergènes saisonniers (pollens);
–la caractérisation de DA dites «intrinsèques» (non allergiques) associées à la présence d’autoanticorps (et probablement de LT
autoréactifs) dirigés contre des antigènes épidermiques, en particulier des kératinocytes [11]. Ces DA correspondraient en fait à des
maladies autoimmunes et seraient fréquemment en cause chez l’adulte. Il est en effet possible que l’inflammation cutanée de la DA
évoluant depuis plusieurs années aboutisse à une immunisation contre des protéines épidermiques avec génération de LT et
d’anticorps spécifiques d’autoantigènes. Le rôle de cette autoréactivité dans le développement des lésions cutanées est encore
inconnu;
-la sensibilisation allergénique par voie cutanée induit des réponses immunitaires systémiques [9]. Une étape majeure dans la
compréhension des réponses immunologiques initiées au niveau de la peau a été récemment franchie par des travaux expérimentaux
chez la souris, montrant que l’application de protéine (ovalbumine) ou d’allergène (dermatophagoïdes de la poussière de maison) sur
le tégument d’animaux aboutit à la génération d’IgE et de LT spécifiques et au développement d’une dermatite atopique de contact,
ce qui signifie qu’il y a eu pénétration des protéines dans la peau saine et activation de LT induisant une inflammation cutanée mixte
Th1/Th2 [5, 12]. Ces animaux sont capables alors de développer une crise d’asthme lorsque l’antigène est administrée par voie
bronchique. Ces travaux démontrent qu’il est possible de se sensibiliser et de développer des maladies allergiques systémiques par
immunisation cutanée. La voie muqueuse respiratoire et digestive sont d’autres voies de sensibilisation vis-à-vis d’allergènes à
l’origine de la DA.
SCHEMA PHYSIOPATHOLOGIQUE
Les mécanismes physiopathologiques à l’origine des lésions d’eczéma sont similaires à ceux de l’eczéma allergique de contact
et impliquent trois partenaires : l’antigène, les cellules présentatrices d’antigène du groupe des cellules dendritiques (DC) et
les lymphocytes T (LT) spécifiques [3,6,9].
Alors que dans la réaction d’eczéma de contact, les molécules prises en charge par les DC sont des haptènes (molécules de
faible poids moléculaire), qui diffusent très facilement à travers l’épiderme, les allergènes (pneumallergènes, pollens, poils
d’animaux, poussières de maison) sont des protéines de plusieurs milliers de daltons, capables de pénétrer dans les couches
superficielles de l’épiderme des patients DA en raison de l’altération de la barrière cutanée.
La DA extrinsèque doit être considérée actuellement comme une réaction d’hypersensibilité retardée de contact aux allergènes
de l’environnement (fig. 2.11). Cette définition est très certainement réductrice mais permet au moins de pouvoir raisonner sur
les différentes étapes qui conduisent un individu donné à développer une DA. Comme pour l’eczéma de contact, il faut
considérer trois phases :
-sensibilisation,asymptomatique, qui peut durer des mois ou des années;
-expression de l’eczéma qui survient chaque fois que le patient est en contact cutané avec l’allergène (les allergènes) auquel il
est sensibilisé ;
-résolution de l’inflammation par mise en jeu de mécanismes régulateurs/suppresseurs
L’expérience clinique et de nombreuses études démontrent que beaucoup de facteurs non immunologiques (psychologiques,
physiques, chimiques, alimentaires) vont permettre ou non le développement des lésions d’eczéma chez un individu
sensibilisé porteur d’une DA.
Fig. 2.11 –Physiopathologie schématique de la dermatite atopique.
Comme toute réaction immunitaire due aux lymphocytes T (LT) spécifiques d’antigène, la réaction inflammatoire de l’eczéma de la DA
comporte trois phases.
Phase de sensibilisation. Elle est cliniquement muette et aboutit à la génération de LT spécifiques qui se retrouvent au niveau cutané.
La sensibilisation se fait classiquement pendant la petite enfance par pénétration des allergènes de l’environnement au niveau cutané
et muqueux (respiratoire, digestif) (étape 1). Quelle que soit la voie de pénétration, les protéines allergéniques sont alors prises en
charge par les cellules dendritiques des épithéliums cutanéomuqueux, d’autant qu’il existe des IgE spécifiques d’allergènes sur la
membrane des cellules dendritiques (étape 2). Les cellules dendritiques migrent dans les ganglions lymphatiques drainants (étape 3) où
la présentation de peptides aux LT a lieu (étape 4), suivie de l’expansion clonale des LT spécifiques. Les LT effecteurs/mémoires
émigrent des ganglions, passent dans le canal thoracique puis dans le sang (étape 5) et se retrouvent dans les tissus muqueux et dans
le derme (étape 6).
Phase de déclenchement des lésions d’eczéma. La prise en charge des allergènes par les cellules de Langerhans, après pénétration
des couches superficielles de l’épiderme, aboutit à leur migration dans le derme et à l’activation des LT CD4+ et CD8+ spécifiques
(étape 7) producteurs de cytokines de type 2 et de type 1, capables d’activer d’autres types cellulaires dont les kératinocytes et les
cellules endothéliales (étape 8). Ceci aboutit à la production de cytokines inflammatoires et de chimiomokines assurant le recrutement
des leucocytes des capillaires au derme puis à l’épiderme où les kératinocytes subissent une intense apoptose (étape 9).

In «Dermatologie et infections sexuellement transmissibles » Saurat, Grosshans, Laugier, Lachapelle, 5° édition, Masson, 2008 in press
Phase de résolution des lésions. Elle est encore mal comprise et n’est pas représentée sur le schéma.
Phase de sensibilisation
Elle aboutit à la génération de LT spécifiques d’allergènes. La sensibilisation s’effectue dans l’enfance. Les lésions d’eczéma
de la DA nécessitent une présentation de peptides d’allergènes par des cellules dendritiques à des LT spécifiques au niveau
des ganglions lymphatiques. L’allergène pouvant pénétrer par voie respiratoire, digestive ou cutanée, la sensibilisation peut
avoir lieu au niveau des ganglions lymphatiques drainant ces différents épithéliums de revêtement. Il est certain que
l’inhalation ou l’ingestion d’allergènes peut induire des poussées de lésions d’eczéma dans la DA. Il est prouvé aussi que la
peau est un site de prise en charge d’allergènes, comme le montre l’induction de lésions d’eczéma chez des patients atopiques
par application de tests épicutanés aux aéroallergènes [10]. Au niveau de la peau, la prise en charge de l’allergène est
favorisée par la présence d’IgE spécifiques sur les CL.
La question principale qui reste posée est de savoir si le nourrisson porteur de DA peut s’immuniser uniquement par
pénétration d’allergènes au niveau cutané ou si les muqueuses sont indispensables à la mise en place de la sensibilisation.
Malgré des débats passionnés, rien n’est encore formellement démontré. En revanche, il existe de plus en plus d’arguments en
faveur du rôle de la pénétration cutanée des pneumallergènes dans l’induction d’une immunisation systémique, responsable de
maladie asthmatique [1-3].
Pénétration des allergènes de l’environnement. La pénétration des allergènes au niveau cutané est favorisée par les
anomalies de la barrière qui caractérisent les patients atopiques [14]. La peau atopique est sèche (xérose) et il manque le film
hydrolipidique naturel protecteur qui limiterait le contact direct des molécules de l’environnement avec la couche cornée. Des
anomalies de cohésion des cellules cornées majorent ce déficit de la barrière cutanée. Le prurit de l’eczéma atopique en dehors
des poussées d’eczéma est lié à la xérose cutanée et aboutit à la pénétration des molécules en contact direct avec la peau. Les
allergènes peuvent alors être pris en charge par les DC. Il est donc logique de penser que la pénétration des allergènes à
travers l’épiderme puisse suffire à générer une sensibilisation lors des premiers contacts, puis des lésions d’eczéma lors des
contacts ultérieurs.
La pénétration des allergènes est favorisée par les propriétés enzymatiques de la plupart d’entre eux [15]. Les allergènes les plus
étudiés sont ceux de la poussière de maison (Dermatophagoides pteronyssinus) (DerP). Ce sont des serine protéases dont les
cibles moléculaires sont les occludines, protéines transmembranaires des jonctions serrées assurant l’adhésion des cellules
épithéliales [26].
Néanmoins, la pénétration des allergènes n’est pas limitée au tissu cutané mais peut se faire à travers toute interface milieu
extérieur/épithéliums de revêtement, en particulier les muqueuses respiratoires (aéroallergènes) et digestive (allergènes
alimentaires). L’allergène est alors pris en charge par des cellules dendritiques présentatrices d’antigènes de ces différents
épithéliums.
Prise en charge des allergènes par les cellules de Langerhans. Les allergènes qui pénètrent les couches superficielles de
l’épiderme sont pris en charge (internalisés) par les cellules de Langerhans épidermiques et les DC dermiques délivrant alors
un «signal de danger » responsable de la maturation et de l’activation des DC. Une particularité des cellules dendritiques des
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
1
/
19
100%