Les nouveaux outils diagnostiques et pronostiques de l`amylose

Journal Identification = MET Article Identification = 0410 Date: September 3, 2013 Time: 4:42 pm
Mise au point
mt 2013 ; 19 (3) : 229-36
Les nouveaux
outils diagnostiques
et pronostiques
de l’amylose systémique
Nadine Magy-Bertrand
Service de Médecine interne, CHU Jean Minjoz, 3, boulevard Fleming, 25 000 Besancon,
France
L’amylose est une maladie rare, de diagnostic difficile. La confirmation de la pathologie repose
sur l’identification histologique de dépôts amyloïdes. Le typage de l’amylose est important
pour décider de la thérapeutique qui sera proposée. Des nouveaux outils diagnostiques et
pronostiques ont été développés dans la pathologie amyloïde durant ces 10 dernières années.
Certains sont des outils anciens qui ont été réactualisés (notamment en médecine nucléaire).
D’autres outils font appel aux nouvelles techniques de biologie moléculaire telles que la
protéomique. L’utilisation de ces nouveaux outils et la hiérarchisation de leur emploi dans
la démarche diagnostique vis-à-vis d’une suspicion diagnostique d’amylose permettent une
meilleure prise en charge de la pathologie amyloïde.
Mots clés : amylose, imagerie par résonance magnétique, imagerie nucléaire, biomarqueurs,
imagerie nucléaire
L’ amylose, identifiée pour la pre-
mière fois par Rokitansky en
1842 [1], est une maladie rare.
Les formes les plus fréquentes
d’amylose sont, par ordre de fré-
quence décroissante, l’amylose
immunoglobulinique (ou amylose
AL), l’amylose secondaire (ou amy-
lose AA) et l’amylose à transthyrétine
(ou amylose à TTR). Il est très impor-
tant de connaître dès la prise en
charge initiale quel est le type
d’amylose pour décider de la prise
en charge thérapeutique adaptée et
de la rapidité de mise en œuvre.
En effet, le pronostic de ces dif-
férents types d’amylose n’est pas
similaire, de même que les traite-
ments qui peuvent être proposés. À
titre d’exemple, une chimiothérapie
à visée hématologique ne traite pas
une amylose secondaire et une greffe
hépatique n’est d’aucune utilité dans
l’amylose AL. Le typage du dépôt
amyloïde doit donc être le plus précis
possible. Le développement d’outils
pronostiques s’est avéré nécessaire
lorsque les traitements de l’amylose
et notamment ceux de l’amylose AL
se sont développés. L’amylose AL car-
diaque est associée à une médiane
de survie de 6 mois en l’absence de
traitement ; il était donc nécessaire
de développer des outils permet-
tant d’évaluer rapidement l’efficacité
du traitement initial proposé pour
envisager un changement en cas
d’inefficacité. Le but de cette revue
est de présenter les nouveaux outils
diagnostiques et pronostiques utili-
sés dans la pathologie amyloïde. Les
différents domaines d’exploration
de la pathologie amyloïde seront
détaillés : l’anatomo-pathologie, la
médecine nucléaire, la radiologie et
les biomarqueurs pronostiques.
Analyse
anatomo-pathologique
des tissus amyloïdes
L’affirmation du diagnostic
d’amylose passe par l’identification
des dépôts amyloïdes dans les tissus
cibles. La coloration de référence
doi:10.1684/met.2013.0410
mt
Tirés à part : N. Magy-Bertrand
229
Pour citer cet article : Magy-Bertrand N. Les nouveaux outils diagnostiques et pronostiques de l’amylose systémique. mt 2013 ; 19 (3) : 229-36
doi:10.1684/met.2013.0410
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 04/06/2017.

Journal Identification = MET Article Identification = 0410 Date: September 3, 2013 Time: 4:42 pm
Mise au point
permettant l’identification des dépôts est le Rouge Congo.
Cette coloration identifie des dépôts déjà visibles par une
coloration standard de type HES (hématoxylline-éosine-
safran). C’est la bi-réfringence jaune-verte des dépôts,
colorés par le Rouge Congo en lumière polarisée, qui signe
le caractère amyloïde du dépôt.
La technique du Rouge Congo a été ensuite complétée
par d’autres colorations telles que la thioflavine T et le
bleu Alcian. Ces colorations permettent d’identifier des
dépôts amyloïdes non identifiés par le Rouge Congo ou de
confirmer le Rouge Congo. Ces techniques de coloration
diagnostiquent la présence d’un dépôt amyloïde mais ne
préjugent en rien du type d’amylose concerné ni de la
charge amyloïde du tissu analysé.
Les techniques d’immunohistochimie (IHC) sont
actuellement couramment employées pour typer le dépôt
amyloïde. L’IHC qui utilise des anticorps anti-SAP
confirme la nature amyloïde du dépôt car le composant
est inclus dans tous les types de dépôts amyloïdes. L’IHC
peut également employer des anti-SAA, des anti-TTR, des
anti-chaînes légères d’immunoglobulines pour typer les
catégories les plus courantes d’amylose. Actuellement, il
est accordé une bonne fiabilité aux IHC avec anti-SAA et
anti-TTR et une fiabilité moyenne aux anti-chaînes légères
(contamination possible du prélèvement par le sang du
patient).
Afin d’affiner l’identification du précurseur amyloïde
et de préciser la quantité d’amylose présente dans le tissu,
des scores et des techniques ELISA ont été développées
durant des 5 dernières années. L’équipe de Hazenberg
et al. [2] a rapporté une technique associant un score
des dépôts amyloïdes observés sur la lame après Rouge
Congo et une quantification après extraction dans de la
guanidine des chaînes légères kappa et lambda présentes
0.1
1
10
100
1000
Kappa (ng/mg graisse)
0 1+2+3+4+
Score amyloïde
Amylose AL kappa
A
0.1
1
10
100
1000
1000
Lambda (ng/mg graisse)
01+2+3+4+
Score amyloïde
Amylose AL lambda
B
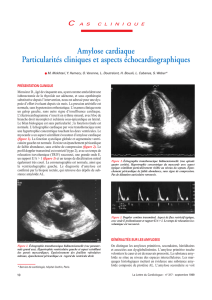
Figure 1. Concentration des chaînes libres liées à la maladie et le score d’amylose dans le tissu adipeux des patients avec amylose AL
(d’après [2]).
dans le dépôt amyloïde identifié dans la graisse sous-
cutanée du patient (figure 1). La figure décrit le cas d’une
amylose AL kappa et celui d’une amylose AL lambda.
Le ratio kappa/lambda des chaînes légères extraites du
dépôt est indicatif du caractère AL de l’amylose identifiée
et de la chaîne légère impliquée. Cette technique a éga-
lement été développée dans le diagnostic de l’amylose
à transthyrétine. L’étude rapportée par Hazenberg et al.
[3] inclut 38 patients atteints d’ATTR, 70 sujets contrôles
et 17 sujets porteurs de la mutation de la TTR sans
maladie. La quantité de dépôt amyloïde a été scorée de
0(<1% de la surface atteinte) à +4 (plus de 60 % de
la surface atteinte). Après cette quantification initiale, la
TTR a été extraite dans de la guanidine et une technique
ELISA sandwich a été employée pour déterminer la
concentration de TTR. La moyenne de la concentration
des patients avec ATTR était à 0,83 ng/mg contre 0,006
chez les contrôles. En retenant un seuil à 0,13 ng/mg,
32/38 ATTR étaient positifs (sensibilité de 84 %) 96 % des
contrôles étaient négatifs et 16/17 porteurs de mutation
sans maladie étaient sous le seuil de 0,13. La concor-
dance entre le score histologique et la concentration était
satisfaisante dans tous les groupes. Ce type de technique
permet donc une identification certaine du précurseur
amyloïde et permettra dans le futur d’évaluer une réponse
thérapeutique.
Les techniques de biologie moléculaires
Elles permettent l’identification du précurseur amy-
loïde qu’il s’agisse de transthyrétine mutée, d’une
chaîne légère d’immunoglobuline ou d’une variante rare
d’amylose systémique telle que l’amylose à lysozyme.
230 mt, vol. 19, n◦3, juillet-août-septembre 2013
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 04/06/2017.

Journal Identification = MET Article Identification = 0410 Date: September 3, 2013 Time: 4:42 pm
Le développement actuel de ces techniques a pour
principal but d’identifier des précurseurs amyloïdes non
reconnus par les techniques histologiques classiques, par
les techniques immunohistochimiques et par les tech-
niques d’immuno-électromicroscopie. Avec l’avènement
de la protéomique et le développement de la spectromé-
trie de masse, la tendance est l’association de plusieurs
techniques de biologie moléculaire. Lavatelli [4] et al. ont
ainsi rapporté une étude de cas permettant de démon-
trer l’apport de la spectrométrie de masse basée sur
la protéomique dans le diagnostic d’une amylose AL
(figure 2). Le patient est un homme de 62 ans qui pré-
sente une neuropathie périphérique. Les autres signes
cliniques sont une perte de poids, une dysphonie et
une amylose cardiaque (échocardiographie évocatrice,
NT-proBNP à 523 [n<322 ng/L]). Des dépôts amy-
loïdes sont identifiés par le Rouge Congo à l’analyse
histologique d’une masse rétropéritonéale. En immu-
nohistochimie, les marquages kappa/lambda sont peu
concluants. L’analyse des chaînes lourdes libres sériques
note une prédominance des chaînes et l’analyse des
chaînes légères libres sériques une prédominance des
chaînes lambda. Les analyses génétiques sont négatives
pour TTR, ApoAI, ApoAII, lyoszyme et fibrinogène. En
immuno-électromicroscopie de la graisse sous-cutanée
abdominale, les fibrilles amyloïdes sont en quantité abon-
dante mais non marquées par les anticorps anti-et
anti-lambda. L’analyse protéomique par technique 2D-
PAGE permet l’identification de protéines marquées par
les anticorps anti-lambda. L’analyse de ces protéines par
spectrométrie de masse (MALDI-TOF MS) et la compa-
raison à des séquences protéiques spécifiques révèle le
précurseur amyloïde qui est une chaîne légère lambda
(lambda V 10-54).
Imagerie nucléaire
et amylose systémique
Le diagnostic histologique d’une amylose systémique
par les techniques de coloration habituelles ne préjuge
pas de l’extension de l’amylose systémique et ne per-
met pas un suivi de l’efficacité des traitements entrepris.
L’imagerie nucléaire permet actuellement d’obtenir une
bonne visualisation de l’extension de certaines amyloses
systémiques [5] et peut, dans certains cas, autoriser un
suivi de l’efficacité des traitements.
La scintigraphie au composant P marqué
Il s’agit de la technique d’imagerie nucléaire la plus
utile dans le diagnostic de la localisation des dépôts amy-
loïdes dans l’ensemble du corps (figure 3). Le traceur
utilisé est le composant P marqué à l’iode 123 (123I). Le
composant P est une glycoprotéine, non fibrillaire, déri-
vée de la protéine amyloïde sérique (SAP), présente dans
tous les types de dépôts amyloïdes (AL, AA, sénile, TTR,
etc...). La SAP circule normalement dans le sérum des
sujets sains. La scintigraphie au SAP marqué a été mise
au point par l’équipe londonienne de Pepys et est actuel-
lement disponible au Royaume-Uni et aux Pays-Bas. La
diffusion de cette technique n’a pas été large car elle fait
appel à une protéine dérivée du sang : la SAP. La Food
and Drug Administration (FDA) américaine et les autori-
tés sanitaires franc¸aises ont refusé son développement sur
les territoires concernés en arguant du risque infectieux
hypothétique que le patient courait lors de cet examen.
La scintigraphie au SAP marqué permet de visualiser la
localisation des dépôts amyloïdes quel que soit le type
d’amylose [6] et un suivi de l’examen dans le temps permet
de juger de l’efficacité du traitement de l’amylose.
Anti-µAnti-λ
Anti-λ
10
200
AB C D
310
50KDa
98
Try
842.50
Try
1045.50
178-190
1743.50
1-12
1244.63
194-203
1711.60
115-133+Na
2008/03
115-133
1098.00
134-153 or T
2211.17
107-133
2807.56
16-48 PyroClu
3329.58
16-45
3329.58
Lambda IGLV10-54
134-153 Methyl
2225.2
65
45
31
21
14
25KDa
pt
SAP
ApoA-1
MW W
M
Anti-µ
Figure 2. A)Immuno-électromicroscopie (17000x) montrant des fibrilles amyloïdes dans le tissu adipeux avec marquage anti-lambda et
antique; B) 2D-PAGE protéome du tissu adipeux ; C) Immunoblot des protéines extraites du tissu adipeux séparées par SDS-PAGE ; D)
Correspondance entre la séquence théorique en acides aminés de la chaîne lambda et la séquence de la protéine extraite de la moelle
osseuse (d’après [4]).
mt, vol. 19, n◦3, juillet-août-septembre 2013 231
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 04/06/2017.

Journal Identification = MET Article Identification = 0410 Date: September 3, 2013 Time: 4:42 pm
Mise au point
Développement des techniques d’imagerie
nucléaire pour l’exploration de l’amylose
cardiaque
Durant les 10 dernières années, les différentes tech-
niques d’imagerie nucléaire ont essentiellement permis
d’approfondir la description de l’amylose cardiaque et de
la diagnostiquer plus précocement.
Les techniques permettent d’explorer l’innervation
cardiaque, le métabolisme cardiaque, la perfusion car-
diaque, les dépôts amyloïdes et la fonction ventriculaire
(tableau 1) [7]. Ces techniques ont principalement été
développées dans l’étude de l’amylose cardiaque AL
(médiane de survie à 6 mois sans traitement) et dans
l’étude de l’amylose cardiaque à transthyrétine (recherche
d’une atteinte cardiaque précoce avant de prendre la déci-
sion d’une transplantation hépatique). Nous décrirons les
deux principales techniques employées en pratique cli-
nique : la scintigraphie au 123I-MIBG et la scintigraphie au
99Tc-(pyro)phosphate.
La scintigraphie au 123I-MIBG
Cette technique a initialement été développée il y a
plus de 20 ans pour évaluer les séquelles de l’infarctus du
myocarde notamment sous l’angle de l’innervation sym-
pathique cardiaque. Le MIBG (métaïodobenzylguanidine)
est un agent neuronal bloqueur agissant sur le système
sympathique. Il adopte le même système de captation
et de stockage que la noradrénaline mais n’est pas sou-
mis au même métabolisme. Ce composant marqué à 123I
permet l’imagerie du système nerveux sympathique de
nombreux organes et en particulier du myocarde. Deux
indicateurs du fonctionnement sympathique myocardique
sont employés : le ratio H/M (heart/mediastinum) déter-
miné par le rapport entre la captation précoce du traceur
à 15-30 minutes et la captation tardive à 4 heures qui
évalue la distribution cardiaque sympathique et la fonc-
tion de captation des terminaisons nerveuses et le taux de
washout permettant d’évaluer la sympathicotonie (capa-
cité de stockage du traceur). Plus le ratio H/M est bas, plus
l’atteinte du système nerveux sympathique cardiaque est
sévère. Il existe une corrélation importante entre l’atteinte
du système nerveux autonome au cours de l’amylose et la
sévérité de la dénervation cardiaque [8, 9]. La dénervation
cardiaque est essentiellement observée dans les neuropa-
thies amyloïdes familiales (FAP) et dans les amyloses AL
avec atteinte du système nerveux autonome [9].
La scintigraphie au 99Tc-(pyro)phosphate (figure 3)
Depuis 1977, les dérivés phosphatés marqués au Tech-
nétium sont employés pour dépister les dépôts amyloïdes
[10]. Les dérivés phosphatés marqués lient les compo-
sants calciques présents dans les dépôts amyloïdes. Trois
types de dérivés phosphatés peuvent être utilisés pour
cartographier les dépôts amyloïdes (tableau 1). Nous insis-
terons essentiellement sur la scintigraphie au 99mTc-DPD
(diphosphates) qui permet de différencier une amylose car-
diaque AL d’une amylose cardiaque à transthyrétine. Ce
diagnostic différentiel est important car dans le cas de
l’amylose cardiaque AL le pronostic est péjoratif et les
traitements sont des chimiothérapies (avec ou sans auto-
greffe de cellules souches) à entreprendre rapidement et,
dans le cas de l’amylose à TTR, le pronostic est meilleur et
Tableau 1. Mécanisme physiologique cardiaque exploré suivant la technique d’imagerie nucléaire [7].
123I-MIBG
123I-BMIPP
99mTc(V)-DMSA
99mTc-sestamibi et 201Tl
99mTc-aprotinine
Innervation cardiaque
Métabolisme cardiaque
Perfusion cardiaque
Dépôts amyloïdes
Technique d’imagerie nucléaire (SPECT)
Mécanisme physiologique cardiaque exploré
232 mt, vol. 19, n◦3, juillet-août-septembre 2013
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 04/06/2017.

Journal Identification = MET Article Identification = 0410 Date: September 3, 2013 Time: 4:42 pm
AB
Figure 3. Vues antérieure et postérieure d’une scintigraphie au 99mTc-HDP (A) et d’une scintigraphie au 123I-SAP (B). La fixation
myocardique identifiée sur la scintigraphie osseuse n’est pas visible sur la scintigraphie au SAP marqué. Les deux examens montrent une
hyperfixation des grosses articulations. Les prises de contraste thyroïdiennes et gastriques sont physiologiques avec la scintigraphie au
SAP (d’après [5]).
les traitements passent essentiellement par la transplanta-
tion d’organes (foie-cœur). La distinction entre ces 2 types
d’amylose cardiaque s’effectue par la mesure de la capta-
tion du traceur qui est beaucoup plus importante en cas
d’amylose à TTR qu’en cas d’amylose AL [11].
Le TEP-scan
Les marqueurs radiopharmaceutiques utilisés lors de
la tomographie par émission de positrons et notamment le
18F-FDG ont un intérêt limité dans l’exploration des amy-
loses systémiques. Cependant l’utilisation d’autres agents
radiopharmaceutiques, tels que le 11C-BF-227 qui permet
la visualisation des dépôts amyloïdes myocardiques au
cours de la neuropathie amyloïde familiale, induira sans
doute le développement de cette technique pour juger de
l’extension de l’amylose systémique [12].
Imagerie par résonance magnétique
et amylose cardiaque (figure 4)
L’atteinte du parenchyme cardiaque par les dépôts
amyloïdes est la plus péjorative en termes de pronostic.
Elle est la cause principale de décès au cours de l’amylose
AL avec une médiane de survie de 6 mois en l’absence
de traitement et est l’une des principales causes de décès
au cours de l’amylose à TTR. Son identification précoce
est importante. L’échocardiographie permet de suspecter
une amylose cardiaque par le diagnostic d’une cardio-
myopathie restrictive avec parenchyme hyperbrillant et
hypertrophie du septum interventriculaire dont la taille a
une valeur pronostique [13]. Pour bien diagnostiquer une
amylose cardiaque, il faut un échographiste expérimenté.
La suspicion diagnostique d’amylose cardiaque peut éga-
lement être étayée par l’IRM cardiaque. Il n’existe pas
de supériorité de l’IRM cardiaque dans le diagnostic par
rapport à un échographiste expérimenté mais l’IRM peut
guider la biopsie endomyocardique. L’IRM cardiaque n’est
pas adaptée pour la surveillance de l’évolution de la car-
diopathie amyloïde sous traitement (cf. ci-dessous chapitre
biomarqueurs).
L’IRM permet de mettre en évidence des signes de car-
diopathie restrictive et dans un second temps d’attribuer
cette cardiopathie à l’amylose. L’aspect, témoin de la
cardiopathie amyloïde, le plus spécifique à l’IRM est
l’existence d’un rehaussement tardif du myocarde après
mt, vol. 19, n◦3, juillet-août-septembre 2013 233
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 04/06/2017.
 6
6
 7
7
 8
8
1
/
8
100%