Accès au thésaurus harmonisé gynécologie

Document créé le : 16/12/2014
Document validé le : 19/11/2015
- 1 -
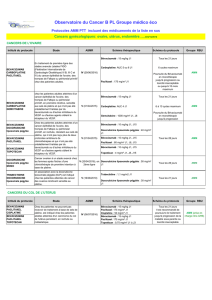
Thésaurus régional harmonisé des protocoles de gynécologie
Ce référentiel a été élaboré par un groupe de travail pluridisciplinaire de professionnels regroupant le Réseau Onco-normand (RON)
et l'Observatoire du Médicament, des Dispositifs médicaux et de l'Innovation Thérapeutique de Haute-Normandie (OMéDIT). Il fera l'objet
d'une mise à jour annuelle prenant en compte les recommandations nationales de pratique clinique.
Le prescripteur se réserve le droit d'adapter la posologie et le rythme d'administration si l'état physiologique, la tolérance et/ou les
traitements antérieurs reçus par le patient le justifient.
Le nombre de cycles est indiqué lorsque des données de la littérature ont été établies.
La chronologie d'administration des molécules de chimiothérapie correspond à l'ordre d'apparition des molécules dans les tableaux.
Références : Dossier du CNHIM Anticancéreux: utilisation pratique 7ème édition, décembre 2013, XXXIV, 5-6; Vidal Hoptimal 2015; Dorosz
2014; Référentiel de bon usage (RBU) ; Revue pluridisciplinaire en oncologie Nice Saint Paul de Vence 2012 Cancer de l'ovaire (Onko+, vol.5
cahier 2 n°41, octobre 2013), Recommandations de l'European Society of Medical Oncology (www.esmo.org), référentiel SFOG (www.sfog.fr).
Protocoles antiémétiques : AFSOS 2013 ; OMEDIT Centre 2015 ; Vidal Hoptimal 2015 ; ASCO 2006; MASCC 2007; National Comprehensive
Cancer Network Clinical (NCNN) : practice Guidelines in Oncology Antiemesis 2011; J.- P. Durand, I. Madeleine, F. Scotté : Recommandations
pour la prévention et le traitement des nausées et vomissements induits par la chimiothérapie, Bull Cancer 2009, 96: 951-960.
Niveau émétisant des protocoles de chimiothérapie : Dossier du CNHIM Anticancéreux: utilisation pratique 7ème édition, décembre 2013,
XXXIV, 5-6 et Thérapeutiques antiémétiques chez l'adulte associées à la chimiothérapie anticancéreuse, OMEDIT Centre (The Oncologist 2007 ;
12 : 1143 – 1150 : Directives pour le traitement antiémétique des nausées et vomissements induits par la chimiothérapie : recommandations
antérieures, actuelles et futures.
Ce référentiel a été élaboré par un groupe de travail multidisciplinaire de professionnels issus du Réseau Onco-normand (RON) et de l'OMéDIT : Dr. Nicolas
ALBIN, Dr. Cécile GUILLEMET, Dr. Marianne LEHEURTEUR, Dr. Marc BARON, Dr Benoît RESCH, Dr. Florence BASUYAU, Dr. Bernard CHERU, Dr. Doreya
MONZAT, Dr. Anaïs BRETEAU, Mr Nicolas HENRY

Document créé le : 16/12/2014
Document validé le : 19/11/2015
- 2 -
Sommaire
Cancer de l'ovaire
Polythérapies
Bevacizumab – Doxorubicine liposomale pegylée
Bevacizumab - Gemcitabine – Carboplatine
Bevacizumab – Paclitaxel
Bevacizumab – Paclitaxel - Carboplatine
Bevacizumab – Topotécan
BEP (Bléomycine, Etoposide, Cisplatine)
Docétaxel – Carboplatine
Doxorubicine liposomale pegylée - Carboplatine
Doxorubicine liposomale pegylée – Trabectédine
5-FU - Carboplatine
Gemcitabine - Carboplatine
Gemcitabine - Cisplatine
GEMOX (Gemcitabine, Oxaliplatine)
Paclitaxel - Carboplatine
Paclitaxel – Carboplatine 3 semaines sur 4
Paclitaxel - Cisplatine
Monothérapies
Bevacizumab - consolidation
Carboplatine J1 = J22
Doxorubicine liposomale pegylée
Gemcitabine
Paclitaxel 3 semaines sur 4
Topotécan
Topotécan 3 semaines sur 4

Document créé le : 16/12/2014
Document validé le : 19/11/2015
- 3 -
Sommaire
Cancer du col de l'utérus
Polythérapies
Bevacizumab – Paclitaxel - Cisplatine
Bevacizumab – Paclitaxel - Topotécan
5-FU - Carboplatine
5-FU – Cisplatine + Radiothérapie
Gemcitabine - Cisplatine
Paclitaxel - Carboplatine
Paclitaxel - Cisplatine
Topotécan - Carboplatine
Topotécan - Cisplatine
Monothérapies
Bevacizumab - consolidation
Carboplatine hebdo + Radiothérapie
Cisplatine J1 = J22
Cisplatine hebdo + Radiothérapie
Cancer de l'endomètre
Polythérapie
Doxorubicine - Cisplatine
Paclitaxel - Carboplatine
Monothérapies
Doxorubicine
Cancer des trompes de Fallope
Polythérapies
Bevacizumab – Doxorubicine liposomal pegylée
Bevacizumab - Gemcitabine – Carboplatine
Bevacizumab – Paclitaxel
Bevacizumab – Paclitaxel - Carboplatine
Bevacizumab – Topotécan
GEMOX (Gemcitabine, Oxaliplatine)
Paclitaxel - Cisplatine
Monothérapies
Bevacizumab - consolidation
Carboplatine J1 = J22
Gemcitabine
Paclitaxel 3 semaines sur 4
Topotécan 3 semaines sur 4
Autres cancers gynécologiques
Cancer de la vulve :
5-FU - Carboplatine
5-FU - Cisplatine
5-FU – Cisplatine + Radiothérapie
5-FU – Mitomycine C + Radiothérapie
Cancer du vagin :
Cisplatine hebdo + Radiothérapie
5-FU - Cisplatine
5-FU – Cisplatine + Radiothérapie

Document créé le : 16/12/2014
Document validé le : 19/11/2015
- 5 -
Cytotoxiques en polythérapie
Bevacizumab – Doxorubicine liposomal pegylée
Bevacizumab - Gemcitabine – Carboplatine
Bevacizumab – Paclitaxel
Bevacizumab – Paclitaxel - Carboplatine
Bevacizumab – Paclitaxel - Cisplatine
Bevacizumab – Paclitaxel - Topotécan
Bevacizumab – Topotécan
BEP (Bléomycine, Etoposide, Cisplatine)
Gemcitabine - Carboplatine
Gemcitabine - Cisplatine
GEMOX (Gemcitabine, Oxaliplatine)
Docétaxel – Carboplatine
Doxorubicine – Cisplatine
Doxorubicine liposomale pegylée - Carboplatine
Doxorubicine liposomale pegylée – Trabectédine
5-FU - Carboplatine
5-FU - Cisplatine
5-FU – Cisplatine + Radiothérapie
5-FU – Mitomycine C + Radiothérapie
Paclitaxel - Carboplatine
Paclitaxel – Carboplatine 3 semaines sur 4
Paclitaxel - Cisplatine
Topotécan - Carboplatine
Topotécan - Cisplatine
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
 37
37
 38
38
 39
39
 40
40
 41
41
 42
42
 43
43
 44
44
 45
45
 46
46
1
/
46
100%