Carcinome épidermoïde de la cavité orale

2
I -
F LEMOINE*, G.L, R M, C
B, V M, C B
UMR CNRS7211/INSERM 959, Université Pierre et Marie Curie, Groupe
Hospitalier Pitié Salpêtrière, Paris, France
Les cancers des voies aéro-digestives supérieures (VADS) se situent à la sixième place des cancers les
plus fréquents au monde et à la troisième place masculine française, après les cancers des bronches et de
la prostate. Les carcinomes épidermoïdes représentent les cancers des VADS de loin les plus fréquents
(plus de 90%). Bien que l’alcool et le tabac soient les principaux facteurs de risque de développement
de ces cancers, environ 15 à 20 % des cancers VADS sont diagnostiqués chez de jeunes adultes non
fumeurs et non buveurs. Récemment l’implication du papillomavirus (HPV) a été mise en évidence,
principalement dans les cancers de l’oropharynx. On estime que 20 à 93% de ces cancers de l’oropharynx
(amygdale et base de langue) sont liés à l’HPV-16, exprimant les oncoprotéines E6 et E7. Ces oncopro-
téines participent au processus de carcinogenèse. Enn, près de 10% des patients atteints de carcinomes
épidermoïdes de la cavité orale ne présentent aucun facteur de risque connu.
Malgré les thérapeutiques actuelles (radiothérapie, chirurgie et chimiothérapie), les cancer des VADS
ont un pronostic médiocre ne dépassant pas les 20% à 10 ans. Il apparait donc important de développer
de nouvelles stratégies telles celles destinées à stimuler le système immunitaire. Ces stratégies d’immu-
nothérapie sont d’autant plus envisageables qu’il existe des antigènes bien identiés comme les onco-
protéines E6/E7 de HPV pour lesquels les vaccins préventifs restent inecaces pour le traitement de
tumeurs établies ou encore des antigènes tumoraux associés tels MAGE3 et HER2/Neu.
Dans le cadre des cancers de VADS, diérentes stratégies d’immunothérapie anti-tumorale (vaccins
ADN, peptides HLA-restreints, vaccination par vecteurs viraux, transfert adoptif de lymphocytes T
cytotoxiques (CTL), injection de cellules dendritiques) ont été développées. La plupart des stratégies
ont été étudiés dans des modèles de tumeurs induits par HPV, et ont montré des résultats intéressants
chez l’animal. Chez l’homme, diérentes stratégies vaccinales pour le traitement de tumeurs HPV-in-
duites et notamment les tumeurs cervicales ont été proposées. Toutefois, la plupart des études cliniques
se sont révélées décevantes.
An d’améliorer la prise en charge des patients atteints de cancer des VADS, nous décrirons de nouvelles
approches d’immunothérapie vaccinale curative utilisant des vecteurs viraux et/ou non-viraux destinés
à cibler in vivo les cellules dendritiques, cellules les plus ecaces pour induire des réponses CTL. Parce
que ces stratégies seules risquent d’être insusantes, il apparaît important de combiner les approches
vaccinales aux thérapeutiques classiques (radio/chimiothérapie) mais également à des stratégies plus
innovantes permettant de renforcer la réponse immune. Grâce à l’étude du microenvironnement tumo-
ral des patients atteints de cancer des VADS induits ou non par HPV, diérents mécanismes favorisant
l’échappement des cellules tumorales au système immunitaire ont été identiés. Il est alors possible de
prendre en compte ces observations et de proposer de nouvelles voies thérapeutiques telles la dépletion
in vivo de lymphocytes T régulateurs, le blocage de la voie PD1-PD1-ligand, l’utilisation d’inhibiteur de
la voie IDO , etc….Ces derniers aspects seront discutés.
Ainsi, un nouvel arsenal thérapeutique, encore aujourd’hui expérimental, est en cours de développe-
ment, mais sa mise en oeuvre à terme devrait considérablement améliorer le pronostic des patients
atteints de cancer des VADS.
2
C
-
P SAINTIGNY
Department of oracic/Head & Neck Medical Oncology,
e University of Texas MD Anderson Cancer Center, Houston, Texas
Les lésions orales à potentiel malin sont diverses, peu fréquentes et leur traitement est mal codié (1).
La valeur prédictive des critères cliniques et anatomo-pathologiques pour prédire le risque de transfor-
mation maligne est faible, et le suivi de ces lésions nécessite une expertise clinique particulière. Les plus
fréquentes sont les leucoplasies orales, qui ont des taux de transformation maligne de l’ordre de 20 % sur
des périodes de 30 ans (2). Elles sont plus fréquentes chez les individus alcoolo-tabagiques. Une mino-
rité de leucoplasies orales atteint des personnes non alcoolo-tabagiques ; leur agent étiologique n’est pas
connu et semblent associées à un risque plus élevé de transformation maligne. Le suivi des lésions à
potentiel malin est important car elle peut et doit permettre un dépistage précoce des carcinomes épi-
dermoïdes de la cavité buccale autorisant une chirurgie à visée curatrice (3). Plusieurs agents ont été ou
sont évalués pour prévenir la transformation maligne des leucoplasies orales, ouvrant à terme la pers-
pective d’une chimioprévention, mais à ce jour aucun d’entre eux n’a fait la preuve de son ecacité (4).
Enn, pour le médecin biologiste, l’étude des lésions à potentiel malin de la cavité buccale est un modèle
passionnant à au moins deux niveaux : 1-la cavité buccale est facilement accessible, ce qui permet l’étude
de la séquence des modications moléculaires au cours du long processus de transformation maligne
; 2-la cavité buccale est considérée comme un miroir aux dégâts causés par le tabagisme sur l’ensemble
de l’arbre respiratoire, et pourrait donc en théorie avoir un intérêt pour les patients tabagiques à risque
SESSION
Carcinome épidermoïde de la cavité orale
Coordination : Chloé BERTOLUS

2
A -
-
: ’ ASED (A S
E D)
J ADRIEN , B BEAUJAT , A MALLET , L GAM-
BOTTI , C BERTOLUS
1. unité de Recherche Clinique et INSERM U436, Hôpital de la Pitié-Salpê-
trière et Université Paris 6, Paris
2 service d’ORL, Hôpital Tenon et Université Paris 6, Paris
3 service de Chirurgie Maxillo-Faciale, Hôpital de la Pitié-Salpêtrière et Uni-
versité Paris 6, Paris
Introduction Le pronostic des carcinomes épidermoïdes des VADS est d’autant plus péjoratif qu’ils
sont diagnostiqués tardivement. L’inuence de facteurs démographiques, socio-économiques et liés au
parcours de soins des patients sur le stade au diagnostic du cancer des VADS n’a pas encore fait l’objet
de recherche. L’objectif de l’étude est de déterminer lesquels de ces facteurs sont associés à un diagnostic
tardif (cancers au stade T3/T4).
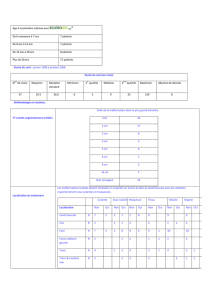
Matériels et méthodes L’étude ASED multicentrique française a recueilli ces données à partir de deux
questionnaires (un rempli par le patient et un par le chirurgien). Les patients (n = 435) présentant un
carcinome épidermoïde des VADS (tout stade TNM) sont inclus de manière prospective de décembre
2010 à juin 2012. L’analyse principale est stratiée sur le stade T (T1/T2 vs T3/T4). L’analyse secondaire
de facteurs de risque est faite par régression logistique uni- et multivariée modélisant la probabilité
d’avoir un cancer T3/T4 au diagnostic, après ajustement sur le sexe et le centre investigateur.
Résultats Les patients T3/T4 représentent 52% de l’échantillon. Leur IMC est plus faible que celui des
patients T1/T2 (23 vs 24, p = 0,04). La précarité selon le score EPICES est plus fréquente dans le groupe
T3/T4 (76% vs 69%, p = 0,14). La consommation de tabac et d’alcool n’est pas associée à la gravité du dia-
gnostic. Les centre franciliens recrutent plus de patients T3/T4 que T1/T2, contrairement aux centres
du Sud (p = 0,04). Les délais de consultation sont identiques dans les deux groupes. Les facteurs associés
à un diagnostic tardif en multivarié sont l’activité professionnelle (OR = 0,5 [0,3-0,8] vs non actif), la
consultation spécialisée préalable (OR = 0,6 [0,3-0,9]) et la localisation tumorale hypopharyngée (OR =
3,5 [1,7-7,2] vs cavité buccale).
Conclusion La détection tardive des carcinomes épidermoïdes des VADS est inuencée par l’activité
professionnelle, la consultation préalable d’un médecin spécialiste en cancérologie des VADS et la loca-
lisation tumorale.
Mots-clés Carcinome épidermoïde des VADS, diagnostic tardif, précarité, parcours de soins.
de cancers pulmonaires (concept de champ de cancérisation) (5). L’un des obstacles majeur à cette
recherche est la nécessité d’inclure les patients atteints de lésions à potentiel malin dans des cohortes
prospectives et d’y associer une collection de matériel biologique.
Dans cette présentation nous décrirons nos travaux dont les objectifs sont les suivants : 1-la mise en
évidence de marqueurs moléculaires pour identier les patients porteurs de leucoplasies orales à très
haut risque de développer des carcinomes épidermoïdes de la cavité buccale ; 2-la recherche de nou-
velles cibles thérapeutiques pour la prévention de la transformation maligne. Notre recherche se base
sur l’analyse de biopsies de leucoplasies orales recueillies de façon prospective chez des patients inclus
dans des essais cliniques de chimioprévention (6-8), ainsi que sur l’utilisation de modèles précliniques
in vitro et in vivo. Les résultats utilisant diverses plateformes d’analyse à haut-débit pour caractériser les
anomalies du génome et du transcriptome de leucoplasie orale seront présentées. Dans ce domaine de
la recherche, les collaborations entre centres experts sont indispensables pour permettre la validation
des biomarqueurs candidats dans des cohortes indépendantes. Divers projets allant dans ce sens seront
présentés.
Références
1. Sarode SC, Sarode GS, Karmarkar S, Tupkari JV. A new classication for potentially mali-
gnant disorders of the oral cavity. Oral Oncol. 2011;47:920-1.
2. Silverman S, Jr., Gorsky M, Lozada F. Oral leukoplakia and malignant transformation. A fol-
low-up study of 257 patients. Cancer. 1984;53:563-8.
3. Sankaranarayanan R, Ramadas K, omas G, Muwonge R, ara S, Mathew B, et al. Eect of
screening on oral cancer mortality in Kerala, India: a cluster-randomised controlled trial. Lan-
cet. 2005;365:1927-33.
4. William WN, Jr., Heymach JV, Kim ES, Lippman SM. Molecular targets for cancer chemopre-
vention. Nat Rev Drug Discov. 2009;8:213-25.
5. Bhutani M, Pathak AK, Fan YH, Liu DD, Lee JJ, Tang H, et al. Oral epithelium as a surro-
gate tissue for assessing smoking-induced molecular alterations in the lungs. Cancer Prev Res
(Phila). 2008;1:39-44.
6. Saintigny P, El-Naggar AK, Papadimitrakopoulou V, Ren H, Fan YH, Feng L, et al. DeltaNp63
overexpression, alone and in combination with other biomarkers, predicts the development of
oral cancer in patients with leukoplakia. Clin Cancer Res. 2009;15:6284-91.
7. Saintigny P, Zhang L, Fan YH, El-Naggar AK, Papadimitrakopoulou VA, Feng L, et al. Gene
expression proling predicts the development of oral cancer. Cancer Prev Res (Phila). 2011;4:218-
29.
8. Taoudi Benchekroun M, Saintigny P, omas SM, El-Naggar AK, Papadimitrakopoulou V,
Ren H, et al. Epidermal growth factor receptor expression and gene copy number in the risk of
oral cancer. Cancer Prev Res (Phila). 2010;3:800-9.

2
E -
2
T - -
E SCHWOB (P)
Service de chirurgie maxillo-faciale
Hôpital de la Pitié-Salpêtrière - Paris
H REYCHLER (B)
Service de stomatologie et chirurgie maxillo-faciale
Université catholique de Louvain
Cliniques universitaires saint-Luc. Bruxelles, Belgique
Au cours de cet exposé, l’auteur, faisant référence à une analyse actualisée et aussi exhaustive que
possible de la littérature, détaillera les modalités thérapeutiques modernes du cancer buccal, toutes en
els illustrant par des cas traités de manière pluridisiciplinaire au sein de la Clinique de Cancérologie
cervico-maxillo-faciale de son institution.
L’accent sera mis sur les nouveautés et sur les approches, parfois encore expérimentales ou en cours
de validation au sein d’études cliniques, et cela tant au niveau strictement oral qu’au niveau cervical, les
deux sites et donc les deux facettes de tout traitement chirurgical étant toujours étroitement liés.
La chirurgie garde de nombreuses indications, aussi bien en première intention qu’en chirurgie de rat-
trapage : les aspects de qualité de vie doivent primer dans le choix de techniques aussi bien de résection
que de reconstruction. L’autre particularité des thérapeutiques chirurgicales est la très nette tendance à
leur moindre agressivité voire extension, respectant mieux les aspects fonctionnels et esthétiques tout en
ne dérogeant nullement aux stricts critères oncologiques.
La radiothérapie a connu ces dernières années d’énormes avancées : même s’il ne peut être question
de les détailler et encore moins de les analyser car cela ressort d’une autre spécialisé, les conséquences
sur la cavité orale mais aussi sur le pronostic des cancers buccaux sera tout de même évoqué.
La chimiothérapie est très certainement le domaine thérapeutique du cancer buccal où le moins
d’avancées spectaculaires ont pu être obtenues, et pourtant ce n’est pas faute d’études ni d’essais ; leur
combinaison avec la radiothérapie ne peut cependant être passée sous silence.
Par contre, les thérapies dites ciblées, d’ailleurs largement évoquées dans d’autres communications, se-
ront à l’honneur : l’exposé se concentrera sur celles utilisées au sein de l’arsenal thérapeutique du cancer
buccal, leur ecacité restant souvent à démontrer avant d’aboutir à leur recours systématique.
Quelques messages d’espoir permettront de conclure et d‘ouvrir des voies encourageantes pour l’ave-
nir de ces patients.
2
A ’
-
F BENSLAMA (P)
2
U ’
’ ’ --
J L COLL (G)
1
/
3
100%