Poids de la génétique dans le risque de faire une MAI

sylvain.dubucquoi@univ-lille2.fr

•Contexte
•Mécanismes de tolérance (rappels)
•Mécanismes impliqués en auto-immunité (rappels)
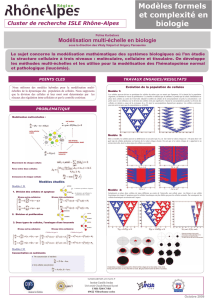
•Pourquoi la génétique ?
–Type d’études
–Anomalies révélées
•Exemples
–La maladie cœliaque
–La SEP
•Conclusion

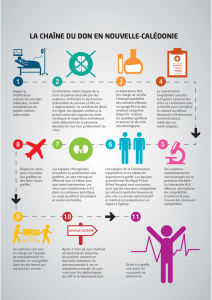
- Maladie auto-immune : rupture des mécanismes de tolérance du système
immunitaire vis-à-vis de constituants de l'organisme (auto-antigènes) conduisant/
associé à un dysfonctionnement des (l’)organe(s) cible(s), combiné (ou non) à un
processus inflammatoire systémique.
- Évolution chronique, par poussées (succession d’épisodes d’agression et de
rémission).
- Exceptionnellement en relation avec un agent pathogène ou toxique identifié
(aujourd’hui) : maladies complexes
- Les traitements actuels ne peuvent, au mieux, que contrôler les poussées. Il est
rare qu'ils apportent la guérison (même si progrès +++ avec les biothérapies).

Induction d’apoptose
Récepteurs inhibiteurs
Cellules régulatrices
(« contexte »)
Cytokines inhibitrices…
Élimination des cellules exprimant un récepteur
autoréactif de forte avidité pour les auto-antigènes
durant les étapes de maturation
(pour les LB : processus de révision du BCR)
4
Poids de l’immunité innée

Facteurs
génétiques
Système
immunitaire
Facteurs
environnementaux
MAI
HLA
- Infections
- Œstrogènes
- UV / Vit D
- Médicaments
- Microbiote
- Tabac
- Obésité
- Pollution (métaux lourds…)
- Complément
- Récepteurs de
cytokines…
Facteur de susceptibilité
tissulaire (« fragilité »)
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
1
/
29
100%