Cours résumé - Pavot

Problématique : Comment est régulée l'apport de sucre dans le sang ?
Thème 1 – Glycémie et diabètes
Activité 0 : rappels
Situation-problème :
Médecin, on vous amène un enfant de 4 mois : Il a des diarrhées à répétition, n’a pas
d’appétit et maigrit. On observe une accumulation anormale de sucres de grande taille (comme
l'amidon) dans l’intestin. Leur accumulation provoque l’irritation de l’intestin, la diarrhée
permanente et les ballonnements. Une biopsie de la paroi intestinale révèle une structure anormale
de la membrane des cellules de la paroi intestinale. De plus, des analyses des sucs digestifs
intestinaux montrent un déficit d'une enzyme : la sucrase-isomaltase. Quel est le problème de
l'enfant au niveau intestinal ?
Chapitre 1 : Importance des enzymes dans l'apport de glucose sanguin
Problème : Dans quelles mesurent les enzymes sont-elles impliquées dans la
digestion ?
I – Les enzymes : des catalyseurs biologiques .
Activité 1 : Fonction de catalyse et enzymes
Bilan : Les enzymes sont des catalyseurs, c'est-à-dire des substances qui, à faible dose, accélèrent
une réaction chimique et se retrouvent intactes à la fin de la réaction (augmentation de la vitesse de
réaction d'un facteur 107 à 1016). Les enzymes digestives permettent ainsi d'assurer une digestion
rapide des sucres (tel que l'amidon).
De plus, comme ce sont des protéines synthétisées par des cellules, on parle de biocatalyseurs ou de
catalyseurs biologiques.
Situation-problème :
La maladie de l'enfant est en fait une maladie héréditaire orpheline appelée déficience en
sucrase-isomaltase ou intolérance au saccharose (=sucrose en anglais) et à l'isomaltose. Il y a donc
une accumulation de saccharose et d'isomaltose (lui-même venant de la dégradation de l'amidon).
Le traitement consiste donc en l'exclusion du saccharose (betterave, canne à sucre) et de l'amidon
(farine de blé) dans l'alimentation. Par contre tous les aliments contenant d'autres sucres complexes
comme le maltose (grain d'orge) ou l'inuline (agave, artichaut) ne posent pas de problème.
Pourquoi ?
Problème : Dans quelles mesurent les enzymes sont-elles spécifiques dans la
digestion de certains sucres ?

II – Les enzymes : des catalyseurs spécifiques .
A – Spécificité enzymatique :
Activité 2 : Etude de la spécificité chez les enzymes
Bilan : Les enzymes ont une double spécificité :
•Une enzyme n'agit que sur un seul substrat. On parle de spécificité de substrat. Ainsi les
enzymes digestives glucidiques vont chacune digérer un type de sucre particulier.
•Pour un substrat donné, une enzyme ne catalyse qu'un seul type de réaction. Ainsi les
enzymes digestives glucidiques vont catalyser qu'un seul type de réaction et former des
types de sucre différents.
Remarque : Le nom de l'enzyme est généralement formé en ajoutant le suffixe « ase » soit au nom
du substrat ou soit au type de réaction chimique catalysée.
B – Vitesse de réaction enzymatique :
Activité 3 : Etude de la vitesse de réaction des enzymes
Bilan : La vitesse d'une réaction chimique est définie par la quantité de produit qui se forme par
unité de temps (v=dP/dt). Cette vitesse n'est pas constante ; elle est plus importante en début de
réaction (vi = vitesse initiale) puis diminue progressivement jusqu'à devenir nulle lorsque tout le
substrat a été transformé en produit.
Pour une concentration donnée d'enzyme, la vitesse initiale du réaction peut être augmentée en
augmentant la concentration de substrat jusqu'à atteindre une valeur limite Vmax. Cela montre que
l'enzyme devient saturée en substrat et donc qu'il se forme un complexe enzyme-substrat.
Situation-problème :

Certains individus ont dû mal à assimiler certains acides aminés. Ces personnes ont une
carboxypeptidase inactive ne parvenant pas à fixer ou à catalyser la transformation du substrat. La
carboxypeptidase (CPA) est une enzyme pancréatique impliquée dans la digestion des protéines.
Pourquoi ?
Problèmes : Comment expliquer que certaines enzymes fonctionnent mal ? Comment
fonctionne le complexe enzyme-substrat ?
III – Le complexe enzyme-substrat :
A – L'exemple de la carboxypeptidase :
Activité 4 : Etude d’une enzyme : la carboxypeptidase
Bilan : L'enzyme a une structure géométrique tridimensionnelle de forme globulaire. Une partie de
cette enzyme est une petite cavité qui est capable d'épouser parfaitement le substrat : il s'agit du site
actif. Il est subdivisé en 2 : un site de fixation (ou de reconnaissance) et un site catalytique.
Le site de fixation est la partie strictement complémentaire au substrat : elle est constituée de
quelques acides aminés qui construisent une cavité. Il permet la formation du complexe enzyme-
substrat et explique la spécificité de l'enzyme pour son substrat.
Le site catalytique est la zone de l'enzyme qui assure la réaction chimique et qui explique la
spécificité de réaction de l'enzyme. Il est constitué de quelques acides aminés qui interviennent dans
une réaction chimique précise à l'origine d'un produit précis.
Question : Comment expliquer le problème de fonctionnement de la CPA ?
Activité 5 : Structure des enzymes
Bilan : Une modification de la séquence protéique d'une enzyme peut entraîner le changement de la
structure spatiale et donc entraîner un problème de fonctionnement du site actif ou soit créer un
nouveau fonctionnement.
Question : Existe-t-il d'autres facteurs influençant le fonctionnement du site actif ?
B – Des facteurs influençant le fonctionnement d'une enzyme :
Activité 6 : Etude du pH et de la température sur l'activité enzymatique
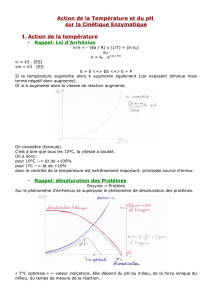
Bilan : Chaque enzyme possède une activité maximale pour une gamme de températures que l'on
nomme optimum thermique : pour des températures inférieures à cet optimum, l'agitation thermique
des molécules est trop faible et les enzymes mettent du temps pour rencontrer leur substrat. Au-delà
de l'optimum thermique, la protéine perd sa forme spatiale, le site actif disparaît : il n'y a plus de
réaction possible.
Il existe aussi un pH optimal qui correspond à une gamme de pH pour lesquels l'enzyme a une
activité maximale : dès que le pH du milieu s'écarte du pH optimal, les acides aminés qui
constituent l'enzyme se chargent différemment (ils deviennent des anions ou des cations selon le
pH). Les interactions entre les acides aminés de l'enzyme sont modifiées, elle perd son activité.
1
/
3
100%