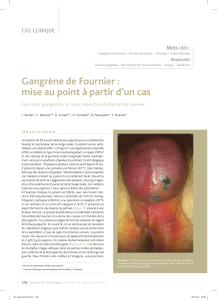
La gangrène de Fournier - Chirurgie

FCC 18 - La gangrène de fournier
SOMMAIRE
Président:
G. MANTION (Besançon)
Modérateurs :
S. ROHR (Strasbourg)
P. MATHIEU (Besançon)
Gangrène de Fournier : présentation de la pathologie
F. MATHIEU (Besançon)
Prise en charge chirurgicale (phase initiale – phase des pansements)
M. CADOT (Brest)
Prise en charge médicale
P. MONTRAVERS (Paris)
Phase de reconstruction
C. CANNISTRA (Paris)

FCC 18 - La gangrène de fournier
GANGRENE DE FOURNIER
-
PRESENTATION DE LA PATHOLOGIE
Pierre MATHIEU, Marianne LAVY
Service de Chirurgie
Viscérale, Digestive et Cancérologique
Unité de Transplantation Hépatique
CHRU Hôpital Jean Minjoz Bd Fleming
25000 Besançon
Email : pmathieu@chu-besancon.fr
Définition
La gangrène de Fournier est une dermo-hypodermite aiguë avec cellulite nécrosante du périnée primitive ou
secondaire (selon la conférence de consensus européennes de Tours en 2000
[1]
) .
• Historique
La toute première description de cellulite nécrosante du périnée date probablement d’Avicenne dans son
« canon de la médecine » autour de l’an mille. Baurienne en 1764 fut le second à décrire cette pathologie avant
que Jean Alfred Fournier ne formalise le tableau. Ce dermatologue spécialisé en vénérologie décrit en 1883
puis en 1884 une fasciite génito-périnéale d’évolution fulminante d’étiologie indéterminée chez l’homme
appelée Maladie de Fournier. Par extension, le terme de Gangrène de Fournier est passé dans l’usage pour
désigner toutes les gangrènes périnéales.
Physiopathologie
La multiplicité des termes employés pour décrire la gangrène de Fournier depuis la gangrène périnéale à la
cellulite pelvipérinéale en passant par la fasciite nécrosante du périnée témoignent de la méconnaissance de la
maladie. Elle regroupent une entité physiopathologique bien précise correspondant à une nécrose septique,
sans pus initialement, diffusant dans le tissus celluleux sous cutané et les loges pelvipérinéales le long des
fascias de Colles, de Buck, de Scarpa et de Dartos qui le prolonge. Le cercle vicieux de l’hyperpression dans les
loges inextensibles associée à la thrombose capillaire par les phénomènes septiques locaux et les toxines des
germes impliqués expliquent le caractère nécrosant de cette fasciite. Les myonécroses sont plus rares.
La diffusion du processus est importante au niveau des organes génitaux externes, du périnée, de la face
antérieur de l’abdomen mais est limitée sur les côtés et en arrière en raison de l’insertion des différents fascias.
Les testicules, les corps caverneux, l’appareil ano-rectal, la prostate et la vessie dont la vascularisation
dépendent directement des vaisseaux rétropéritonéaux sont généralement épargnés. L’extension du sepsis se
fait à une vitesse de 2 à 3 cm/h et justifie une prise en charge sans délai.
• Microbiologie
La synergie bactérienne locale des germes anaérobies strict ou aérotolérants, des bacilles gram négatifs et des
cocci est classiquement invoquée dans les Gangrènes de Fournier secondaires. Ces germes correspondent aux

FCC 18 - La gangrène de fournier
germes commensaux locaux et peuvent être associés à des levures. Les examens bactériologiques peuvent être
faussement négatif par défaut de prélèvement, par la difficulté à cultiver les germes anaérobies et en raison de
l’antibiothérapie probabiliste qui doit être instaurée dès le diagnostic posé avant même la réalisation des
prélèvements chirurgicaux. Ces difficultés d’identification des germes justifient la réalisation de prélèvements
multiples comprenant notamment la ponction de phlyctènes et la culture de fragments de nécrose tissulaire.
La répartition des différents germes est très variable en fonction des publications. L’isolement des germes
anaérobies étant particulièrement difficile, il est difficile de déterminer leur importance réelle dans le
développement de la maladie.
Le Clostridium perfringens présent dans un peu moins d’un tiers des cas est responsable d’une authentique
gangrène gazeuse associant une infection locorégionade fulminante par sécrétion d’une hyaluronidase et d’une
collagénase empêchant l’organisme de circonscrire la diffusion de la fasciite. La production de gaz dissèque les
espaces cellulo-graisseux et la sécrétion d’exotoxines génère un choc septique et des troubles de la
coagulation. Les autres anaérobies gazogénes (Clostridium non perfringens) ou non gazogènes (Bactéroïdes
fragilis sécrétant des enzymes et naturellement résistant à l’ampicilline, Prevotella, Porphyromonas ,
Fusobacterium, Peptostreptococcus, Peptococcus, Veillonella, Propionibacterium acnes, Actinomyces,
Bifidobacterium) peuvent également être retrouvés.
Escherechia coli est le germe le plus fréquemment isolé (environ 40% des cas). Le streptocoque beta-
hémolytique du groupe A et le staphylocoque doré sont par ordre décroissant les germes les plus retrouvés
après l’E. coli. Ils sont respectivement responsables des gravissimes « Streptococcal Toxix Shock Syndrome »
et « Staphylococcal Toxic Shock Syndrome ». Les autres bactéries non spécifiques sont Streptococcus,
Enterococcus, Pseudomonas aeruginosa,, Enterobacter, Klebsiella, Proteus mirabilis, Morganella morganii,
Acinetobacter, Shewanella putrifaciens, Vibrio vulnificus. De rares cas d’infection à levures ont été rapportées à
Candida et à Lactobacillus.
Une flore polymicrobienne est retrouvée dans environ 50% des cas, une flore monomicrobienne dans 40% des
cas et l’absence de germe dans 10% des cas si les prélèvements sont effectués correctement. Le groupe des
germes anaérobies et celui des bacilles gram négatif représentent 40 % des effectifs chacun.
• Classifications
Il existe de multiples classifications de la gangrène en fonction de l’extension anatomique du sepsis, de la
nature des tissus nécrosé, de la profondeur des lésions, de l’aspect clinique de l’atteinte périnéale. Ces
classifications sont souvent incommodes à utiliser et n’ont que rarement des implications thérapeutiques. La
classification publiée dans l’EMC par C. Arvieux en 2011
[2]
a le mérite de s’appuyer sur l’écologie bactérienne et
sur sa corrélation anatomo-clinique et étiologique :
Type I (flore polymicrobienne) : secondaire à un traumatisme, à une intervention chirurgicale, à une infection
urogénitale, à une infection anogénitale ;
Type II (Streptococcus pyogenes) : 50 % des formes idiopathiques ;
Type III (Clostridium perfringens) : gangrène gazeuse.

FCC 18 - La gangrène de fournier
Circonstances de survenue
Globalement rares dans les pays développés, les fasciites périnéales apparaissent dans des circonstances bien
définies.
• Epidémiologie
L’incidence des gangrènes de Fournier est d’environ 0,3/100 000 habitant dans les pays occidentaux. Elles
surviennent à un âge moyen de 50 ans.
La situation socio-économique intervient par le biais d’une hygiène déficiente, du déficit de prise en charge des
pathologies chroniques (diabète, alcoolisme, HIV, obésité), d’une sous- médicalisation responsable de
gangrènes déjà évoluées au moment du diagnostic. La prévalence est bien plus importante dans les pays
africains et asiatiques pour ces mêmes raisons.
Le sex ratio est classiquement entre 10/1 et 8/1. La surreprésentation des hommes peut être expliquée par les
conditions anatomiques différentes chez la femme. La présence de la filière génitale et de ses insertions
particulièrement solides réalisent une barrière physique à la diffusion locale de la nécrose septique mais
favorise par contre son extension vers le rétropéritoine lorsqu’elle survient. La riche vascularisation du tractus
génital favorise également l’oxygénation de la région et est un frein théorique au développement des germes
anaérobies. Une troisième explication au déséquilibre de la répartition statistique des gangrènes entre les
sexes est un biais de recrutement et de diagnostic. Les lésions pelvi-périnéales féminines sont le plus souvent
prises en charge dans les services de gynécologie-obstétrique où cette pathologie n’est pas forcement
identifiée comme une gangrène de Fournier . R CZYMEK
[4]
a publié un sex ratio de 3/1 pour 38 patients en 12
ans en Allemagne en 2009 qui correspond probablement plus à la réalité.
• Etiologie
L’origine des gangrènes de Fournier est identifiée dans 64 % des cas de la plus grande série publiée
[3]
. Les
portes d’entrée sont par ordre de fréquence cutanées (24%), anorectales ou coliques (21%) et urogénitales
(19%). Les formes dites idiopathiques correspondent à l’absence d’étiologie retrouvée. La gangrène peut être la
complication d’une pathologie médicale (56%) mais elle est le plus souvent dans les pays développés iatrogène
(23%) ou post-traumatique (21%). Seule les fasciite scrotale sans lésion préexistante chez l’homme jeune
(14%), le plus souvent à Streptocoque A, sont d’authentiques Maladies de Fournier au sens premier.
Les radionécroses, les brûlures, les piqûres d’insectes et les lésions parasitaires, les chirurgie herniaires ou
pariétale, les adénolymphites suppurées, les furoncles et autres abcès cutanés, les intertrigos, les abords
chirurgicaux du Scarpa, les escarres sont les principales sources cutanées de gangrène.
Les circoncisons et les excisions sont des étiologies fréquentes chez l’enfant. Les autres étiologies urologiques
comprennent les urétrites, les prostatites, les orchi-épididymites, les tumeurs de vessie, les sondages urinaires
traumatiques et les cystocatheters, les sténoses urétrales, les biopsies de prostate, les endoscopies des voies
urinaires, les abcès rénaux , les abcès rétropéritonéaux de toutes natures, les calculs urinaires, les chirurgies de
l'incontinence (TVT, TOT), les cures d’hydrocèle.
Les lésions vénériennes, les bartholinites, les abcès vulvaires, les sepsis utérins et annexiels, les traumatismes
obstétricaux, les épisiotomies, les hystérectomies, les cures de prolapsus, les fausses couches et les

FCC 18 - La gangrène de fournier
avortements même spontanés, les césariennes et les manœuvres gynécologiques ou obstétricales sont
pourvoyeuses de gangrènes d’origine gynécologiques.
Les abcès et les fistules de la marge anale, les fissures anales, les complications hémorroïdaires, les gestes et les
complications de la chirurgie proctologique, rectale, colique et appendiculaire, les sigmoïdites, les
appendicites, les hernies étranglées, les cancers colo-rectaux, les perforations rectales iatrogènes ou non et les
corps étrangers intra-rectaux sont autant d’étiologies digestives non exhaustives aux gangrènes de Fournier.
Outre les traumatismes iatrogènes précédemment cités, les esquilles osseuses d’une fracture du bassin, les
traumatismes directs par un agent vulnérant, les délabrements traumatiques des accidents à haute énergie, les
contusions sévères et les hématomes pelvi-périnéaux disséquants peuvent aussi déclencher une fasciite
nécrosante.
• Facteurs de risque de développement d’une gangrène
Les gangrènes surviennent sur un terrain particulier impliquant souvent une forme d’immunodépression plus
ou moins importante. Le diabète est le facteur de risque le plus fréquent (10 à 60% des cas). Les autres facteurs
favorisant sont l’alcoolisme, l’obésité, l’insuffisance rénale chronique, la cirrhose, l’âge avancé, l’insuffisance
cardiaque, les cancers, les hémopathies , le SIDA et la séroconversion HIV, les artériopathie, l’hypertension
artérielle, la grabatérisation, la paraplégie, la corticothérapie, les traitements immunosupresseurs, les
polytraumatismes, les chimiothérapies et la radiothérapie. Ces facteurs sont souvent associés.
Il existe également des facteurs locaux facilitant le développement d’une gangrène. Un défaut d’hygiène
favorise la pullulation microbienne et les lésions cutanées pouvant servir de porte d’entrée aux germes. Les
attritions tissulaires traumatiques altèrent la vascularisation des tissus qui sont infiltrés par l’œdème. Les
hématomes permettent aux germes anaérobies de mieux se développer et de diffuser plus rapidement. La
présence d’une contamination des plaies en particulier telluriques et la présence de corps étrangers dans les
traumatismes non iatrogènes et les plaies de guerre sont responsables d’une inoculation massive des plaies.
Diagnostic
Il repose sur un examen clinique soigneux dans un contexte étiologique évident ou sur un terrain prédisposé
qui doit être recherché.
• Diagnostic positif
Les signes locaux initiaux sont souvent peu marqués. Ils associent un érythème discret et/ou une pâleur et/ou
un œdème du scrotum, de la verge, du périnée, des cuisses ou de la paroi abdominale à une douleur majeure,
continue, prurigineuse ou cuisante. Le contraste entre les signes fonctionnels très bruyant et les signes
physiques peu importants au début sont caractéristique de la pathologie et doivent faire évoquer le diagnostic
sans retard.
L’évolution locale se fait vers une tension douloureuse, dure et exsudative du scrotum, des phlyctènes souvent
hémorragiques, des plaques de cyanose et de livedo, de la nécrose fétide s’étendant rapidement. La crépitation
neigeuse est pathognomonique mais présente dans moins d’un tiers des cas. Après la phase d’hyperesthésie
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
1
/
24
100%