Placebo - Edimark

La Lettre du Cancérologue
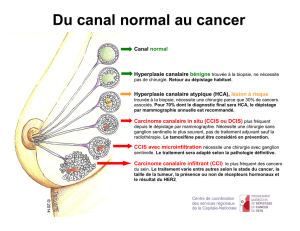
Prévention du cancer du sein avec l’exemestane
chez des femmes ménopausées : méthodologie
Critère principal :
incidence des cancers du sein invasifs
1
Étude de prévention NCIC CTG MAP.3
Etude de phase III, en double aveugle versus placebo
•Critères d’inclusion
–Femmes ménopausées et > 35 ans
–>1 facteur de risque de cancer du
sein :
•âge > 60 ans
•score de Gail > 1,66 %
•antécédents d'hyperplasie
canalaire atypique, hyperplasie
lobulaire atypique et cancer
lobulaire in situ
•cancer canalaire in situ avec
mastectomie
•Critères d’exclusion
–mutations BRCA 1 et 2
–antécédents de cancer du sein
canalaire in situ
–antécédents de cancer du sein ou
autre cancer
R
Exemestane
25 mg/jour pendant 5 ans
Placebo
1 pilule/jour pendant 5 ans
n = 4 560
Février 2004 - Mars 2010
Double
aveugle
Stratification
Utilisation d'aspirine
Score de Gail (< 2,0 versus > 2,0)
Femmes
ménopausées
à risque augmenté
de cancer du sein
D’après Goss P et al., LBA504 actualisé

La Lettre du Cancérologue
Etude de prévention primaire du cancer du sein
NCIC CTG MAP.3 (1)
2
Incidence cumulée de cancer du sein invasif
Incidence cumulée (%)
0Années
1 2 3 4 5
2275 1905 1468 986 477 82
2285 1902 1468 980 464 77
Patientes (n)
Placebo
Exemestane
0
1
2
3
4
5
Exemestane
Placebo
Exemestane
Placebo 0,55 % (0,36-0,73)
0,19 % (0,08-0,30)
HR = 0,35 (IC95 : 0,18-0,70)
p = 0,002 (log-rank test)
Incidence annuelle (IC95)
D’après Goss P et al., LBA504 actualisé

La Lettre du Cancérologue
Etude de prévention primaire du cancer du sein
NCIC CTG MAP.3 (2)
Risque de cancer du sein invasif
en fonction de l’analyse en sous-groupes planifiée
3
Toutes
Aspirine
Oui
Non
Score de risque Gail
< 2,0 %
> 2,0 %
Âge> 60 ans
< 60 ans
IMC< 25
25-30
> 30
Antécédents ADH, ALH ou LCIS*
*ADH hyperplasie canalaire atypique,
ALH : hyperplasie lobulaire atypique ,
LCIS : cancer lobulaire in situ
Oui
Non
Sous-groupes HR (IC95) p
0,01 0,1 1,0
Exemestane meilleur Placebo meilleur
0,35 (0,18-0,70)
0,12 (0,01-0,92)
0,43 (0,21-0,91)
0,34 (0,09-1,27)
0,36 (0,16-0,80)
0,29 (0,12-0,73)
0,44 (0,15-1,27)
0,35 (0,09-1,29)
0,31 (0,10-0,94)
0,41 (0,13-1,30)
0,61 (0,20-1,82)
0,26 (0,11-0,64)
0,24
0,92
0,58
0,94
0,25
D’après Goss P et al., LBA504 actualisé

La Lettre du Cancérologue
Etude de prévention primaire du cancer du sein
NCIC CTG MAP.3 (3)
Effets secondaires selon la sévérité et le bras de traitement
4
Exemestane (n = 2 240) Placebo (n = 2 248)
Toxicité < grade 2 > grade 3 Total (%) < grade 2 > grade 3 Total (%) p
Total 1 395 568 1 963 (88) 1 434 467 1 901 (85) 0,003
Bouffées de chaleur
Fatigue
Insomnie
833
492
215
67
33
15
900 (40)
525 (23)
230 (10)
742
440
182
43
25
7
718 (32)
465 (21)
189 (8)
< 0,0001
0,03
0,04
Diarrhée
Nausée 109
149 9
3118 (5)
155 (7) 74
120 1
275 (3)
122 (5) 0,002
0,04
Arthrite
Douleurs articulaires
Douleurs musculaires
215
587
131
32
78
16
247 (11)
665 (30)
147 (7)
179
572
178
17
34
14
196 (9)
606 (27)
192 (9)
0,01
0,04
0,01
Dépression 213 23 236 (11) 226 9 235 (10) 0,96
Sécheresse vaginale 351 1 352 (16) 343 343 (15) 0,68
D’après Goss P et al., LBA504 actualisé
1
/
4
100%