2 - AMPCfusion

1
UE13 – Parcours n°3 – Signalisation
cellulaire – cours n°2
02/03/2016
Marc LOMBES
marc.lombes@u-psud.fr
RT : CHIQUET Charlotte
Marc-Anthony CHOUILLARD
RL : MAFI Donia
Structure/Fonction des récepteurs stéroïdiens
Plan :
I. La superfamille des récepteurs nucléaires
A- Historique
B- Mécanisme d’action des hormones stéroïdes
C- Homologie des récepteurs stéroïdiens, organisation
fonctionnelle
D- Classification des récepteurs nucléaires : arbre phylogénétique
E- Structure et domaines fonctionnels des récepteurs stéroïdiens
(organisation génomique)
II. Approche méthodologique
A- Mise en évidence des régions cibles à la régulation hormonale
B- Autres techniques
III. Les récepteurs nucléaires
A- Les domaines fonctionnels d’un récepteur nucléaire
1) Le domaine central ou DNA Binding Domain (DBD)
2) Le domaine C-Ter ou Ligand Binding Domain, (LBD)
3) Le domaine N-Ter (NTD)
B- Les localisations subcellulaires
C- Les modifications post-traductionnelles des RN
1) Phosphorylation
2) Ubiquitinylation et sumoylation
3) Acétylation, méthylation, palmitoylation
IV. Régulation hormono-dépendante de la transcription
A- La machinerie transcriptionnelle basale
1) La structure chromatinienne
2) Les mécanismes de régulation de la transcription
B- Complexe de corégulateurs; coactivateurs, corépresseurs et
régulation de la transcription

2
I. La superfamille des récepteurs nucléaires
La superfamille des récepteurs nucléaires est une famille très importante car c’est la plus
grande famille de facteurs de transcription chez les Eucaryotes.
A- Historique
A partir des années 80 a lieu la première purification des récepteurs nucléaires aux
hormones stéroïdes. Le premier récepteur purifié par des techniques biochimiques classiques
est le récepteur aux œstrogènes, suivi de la purification d'autres récepteurs aux hormones
stéroïdiennes, notamment ceux de la progestérone et des glucocorticoïdes à partir de tissus
cibles comme l’utérus pour les œstrogènes ou la progestérone et le foie pour les
glucocorticoïdes.
En 1985, l’avènement de la technique de clonage moléculaire a permis le clonage de l’ensemble
des récepteurs nucléaires et la découverte de la super famille des récepteurs nucléaires. Le
premier récepteur à avoir été cloné est celui des glucocorticoïdes, puis ceux de la progestérone,
de l’œstradiol puis un peu plus tard, ceux des hormones thyroïdiennes, de la vitamine D, de
l’acide rétinoïque… Enfin, des récepteurs dits orphelins ont été identifiés récemment,
récepteurs pour lesquels on ne connaissait pas à l’époque le ligand naturel. Aujourd’hui on a
trouvé pour certains d’entre eux, des ligands : les récepteurs PPAR sont, par exemple, activés par
des dérivés lipidiques. Il existe en particulier des « vrais » récepteurs orphelins pour lesquels
aucun ligand endogène n’a encore été identifié à ce jour (Nurr1). Enfin, c’est dans les années
2000 qu’on utilise pour la première fois le concept de corégulateur, suivi de leur caractérisation.
B- Mécanisme d’action des hormones stéroïdes
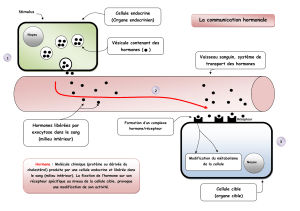
La régulation transcriptionnelle est induite par des récepteurs nucléaires. L’hormone
stéroïdienne circule dans le sang, elle entre ensuite dans la cellule cible, généralement par
diffusion passive. Elle interagit ensuite avec un COMPLEXE MACROMOLECULAIRE qui
comporte une sous-unité capable de lier l’hormone, il s’agit du récepteur stéroïdien (SR),
ainsi que plusieurs protéines partenaires. Le complexe hormone-récepteur subit des

3
modifications conformationelles : des protéines interactantes vont être libérées, ce qui va
permettre au complexe hormone-récepteur de migrer dans le noyau.
Les récepteurs nucléaires ont donc un tropisme et une action nucléaire.
Puis, le complexe hormone-récepteur subit des modifications post-traductionnelles
(phosphorylation, sumoylation…), cela va permettre au récepteur de se dimériser et d’aller
interagir avec des séquences particulières de l’ADN. Il va alors recruter des partenaires
moléculaires spécifiquement nucléaires appelés cofacteurs (activateurs ou répresseurs selon la
situation), à l’origine du recrutement de la RNA polymérase de type II qui permet la néosynthèse
des ARNm. Cela conduit à la synthèse ou à la répression de protéines spécifiques et donc au
déclenchement d’effets physiologiques spécifiques.
Il est important de noter qu’une hormone particulière agit sur une cellule cible particulière et va
être responsable d’un effet physiologique spécifique.
C- Homologie des récepteurs stéroïdiens, organisation
fonctionnelle
L’homologie entre les différents types de récepteurs stéroïdiens est très importante mais
varie en fonction du domaine protéique du récepteur impliqué : la partie centrale de la molécule,
qui est le domaine d’interaction avec l’ADN, le DBD (DNA Binding Domain), est très bien
conservée (>90%). Il s’agit de la signature de ces récepteurs censés lier l’ADN.
De même, le domaine C-Ter ou LBD (Ligand Binding Domain), qui est le domaine de
liaison à l'hormone, a une forte homologie mais est plus divergent que le DBD.
Enfin le domaine N-ter ou NTD est en revanche très divergent (<15%), avec une grande
variabilité en longueur et en séquence.
L’ensemble de ces récepteurs nucléaires est regroupé sous le nom de superfamille des
récepteurs nucléaires et forme l’arbre phylogénétique des récepteurs nucléaires. C’est la plus
grande famille de facteurs transcriptionnels chez les eucaryotes (+++). Cette superfamille est
classée en 6 groupes, désignés par un chiffre. A l’intérieur de ces groupes, il existe des sous-
groupes nommés par une lettre qui eux même contiennent des membres. Cette classification
permet de nommer individuellement chaque récepteur (par exemple NR3C1 pour le récepteur
des glucocorticoïdes). Il existe 48 membres de cette superfamille chez l’homme, 21 chez la
drosophile et presque 300 chez C.Elegans.
D- Classification des récepteurs nucléaires
Elle peut se faire :
> En fonction de leur capacité à lier un ligand naturel ou synthétique
- Récepteurs endocriniens : le ligand est un lipide hormonal (dérivé du cholestérol),
c’est le cas des récepteurs stéroïdiens. Ces récepteurs sont de haute affinité pour les stéroïdes
(ex : récepteur à l’acide rétinoïque, aux hormones thyroïdes, à la vitamine D, aux
glucocorticoïdes, aux minéralocorticoïdes, aux œstrogènes…)
- Récepteurs orphelins adoptés : RXR (pour le récepteur de l’acide rétinoïque), PPAR,
LXR, dont les ligands sont souvent des dérivés lipidiques. Ces récepteurs sont de basse affinité
pour les lipides.
- Récepteurs orphelins, de type SF1, ERR (des perturbateurs endocriniens comme le
bisphénol A peuvent s’y lier)…
Remarque : cette classification évolue car on connaît de plus en plus de ligands capables de se lier à
ces récepteurs dits, au départ, orphelins.

4
> En fonction de leur capacité à lier l’ADN
- Les récepteurs stéroïdiens homodimères : ils se lient sous forme dimérique à l’ADN
(récepteurs aux glucocorticoïdes, aux minéralocorticoïdes, à la progestérone, aux androgènes, à
l’œstrogène…)
- Les hétérodimères : ils ont un monomère spécifique (comme celui à vitamine D ou
de l’hormone thyroïdienne par exemple) qui va s’hétérodimériser avec un partenaire
privilégié : le récepteur RXR (c’est un récepteur de l’acide 9 Cis rétinoïque),
- Les récepteurs orphelins dimériques : GCNF, RXR…
- Les récepteurs se liant sous forme de monomère : SF1 , ERR, ROR…
E- Structure et domaines fonctionnels des récepteurs stéroïdiens
Il existe 3 grands domaines fonctionnels : le domaine N-Ter qui a un rôle très important
dans les fonctions de transactivation (-répression) et de corégulation ; le domaine central, qui
se lie à l’ADN ; le domaine C-Ter, qui lie le ligand. Chaque domaine a des fonctions spécifiques.
Les récepteurs nucléaires ont aussi une organisation génomique très conservée.
Généralement, l’exon 1 est non traduit, le codon ATG d’initiation de la traduction est
généralement situé au tout début de l’exon 2, celui-ci code le domaine N-ter du récepteur
stéroïdien. Les 2 petits exons 3 et 4 codent la partie centrale (le DBD). Enfin, les exons 5 à 9
codent la partie C-ter (LBD).
La composition des gènes des différents récepteurs stéroïdiens ont une organisation
exon/intron très similaire, comme par exemple les récepteurs aux glucocorticoïdes et aux
minéralocorticoïdes. Cependant, pour le récepteur des minéralocorticoïdes, en 5’, deux premiers
exons ne sont pas traduits alors que pour le récepteur des glucocorticoïdes, on a surtout un exon
9 épissé de manière alternative, qui donne donc des isoformes. De même, les récepteurs aux
androgènes et à la progestérone sont similaires d’un point de vue organisationnel. C’est donc
l’organisation structurale des gènes des récepteurs nucléaires qui est très conservée.
/ !\ ATTENTION : Cependant (avec comme exemple le récepteur humain des
minéralocorticoïdes) le gène peut conduire à différents isoformes de messagers et à des
variants protéiques. Le gène du récepteur des minéralocorticoïdes comporte deux exons non
traduits qui sont 1alpha et 1béta, générés par deux promoteurs alternatifs (P1 et P2). En
fonction de l’utilisation de l’un ou l’autre promoteur, on aura l’un ou l’autre exon 1 et donc deux
isoformes d’ARNm, mais comme l’exon 1 n’est pas traduit, ils conduiront à la même protéine. Il

5
existe d’autres isoformes, dépendant de mécanismes excision/épissage alternatifs qui
conduisent à des variants, dont certaines parties peuvent être délétées (ex :hMRΔ5,6). Il existe
enfin des variants protéiques issus de l'utilisation alternative du codon d’initiation de la
traduction, qui conduit à deux protéines dont l’activité transcriptionnelle n’est pas identique.
Ainsi, un même gène peut conduire à différentes isoformes d’ARNm et donc à différentes
protéines aux structures et fonctions distinctes.
II. Approches méthodologiques
Ce chapitre doit faciliter la lecture d’articles, l’analyse de résultats… On étudie ici des techniques
utilisées en endocrinologie moléculaire : le séquençage, la méthode Sanger, ChIP, PCR, RT-PCR…
A- Mise en évidence des régions cibles de la régulation hormonale
On cherche dans les parties 5’ flanquantes d’un gène, des séquences susceptibles d’être régulées
par un type d’hormone et de récepteur.
La méthode est systématique :
0- Clonage des parties régulatrices du gène, c'est à dire des parties 5'-flanquantes
1- Couplage de la partie 5'-flanquante à un gène rapporteur par substitution du gène
par un gène rapporteur (luciférase +++, CAT, β-galactosidase…)
2- Création de mutants de délétion : On crée des mutants de délétion de la région 5'-
flanquante pour étudier la capacité des séquences flanquantes à induire l’expression du gène
rapporteur dont on suit l’activité ; et on identifie une région indispensable pour l'expression
du gène et sa régulation.
3- Couplage avec un promoteur hétérologue : (généralement la thymidine Kinase).
Pour confirmer que la région trouvée est importante, on couple cette région avec un promoteur
(et le gène rapporteur) dans une autre construction plasmidique et on regarde si ce plasmide
répond ou non à une hormone particulière.
4- Études plus fines : le retard sur gel, précipitation de la chromatine (ChIP),
transgenèse, … ces études permettent de mieux comprendre les mécanismes de régulation et
d’identifier dans les séquences régulatrices le fragment d’ADN d'intérêt.
B- Les autres techniques
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
1
/
19
100%