chap 8 énergie chimique

Classe de troisième Chimie Chapitre 8
1
Energie chimique
Objectifs :
- Savoir qu’une pile est un réservoir d'énergie chimique.
- Savoir que lors de son fonctionnement l’énergie chimique est transférée sous d'autres formes.
- Savoir que l’énergie mise en jeu dans une pile provient d’une réaction chimique ; et que la consommation de
réactifs entraîne l’usure de la pile.
- Savoir réaliser, décrire et schématiser la réaction entre une solution aqueuse de sulfate de cuivre et de la
poudre de zinc : - par contact direct
- en réalisant une pile.
I)
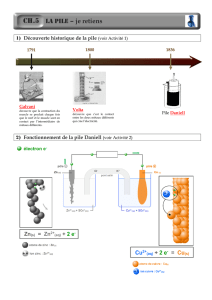
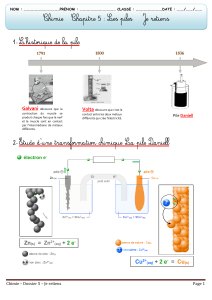
Approche historique de la pile
1) La pile Volta, principe général d’une pile
Alessandro Volta, travaillant sur les travaux de Galvani, découvre en 1799, qu’en
empilant des disques de cuivre et de zinc séparés par des rondelles de carton
humidifiés à l’eau salée, on produit de l’électricité.
Approchons-nous de plus près, et modélisons les
réactions chimiques qui se déroulent sur les deux
plaques :
Du côté du cuivre, la molécule d’eau va capturer
deux électrons du cuivre et produire des ions
hydroxyde et du dihydrogène : il y a donc un déficit
d’électron : c’est le pôle +
Or ces électrons proviennent bien de quelque part !!
Du côté du zinc : le zinc se fait déposséder de deux
de ses électrons !
Consommation d’électron d’un côté, production
d’électron de l’autre, circulation d’électron entre les
deux : un courant électrique est né !
RQ : cette première configuration présente néanmoins des inconvénients : des dépôts dus aux
produits des réactions s’accumulent sur les plaques métalliques, ce qui empêche la pile de
fonctionner correctement. Il faut alors sortir les plaques, les nettoyer …
2) Les piles d’aujourd’hui
Aujourd’hui les piles sont conçues différemment, même si le principe reste le même. L’évolution
majeure à été apportée par Becquerel qui fabriquât la première pile à deux liquides séparés.
On utilise plus de lames de cuivre et de zinc comme à l'époque de Volta, mais on utilise des
matériaux comme le carbone recouvert d'une gaine de zinc. Les solutions ioniques ont été
remplacées par des gels pâteux qui évitent que la pile ne coule.
II)
Fabrication d’une pile simple
1) Réaction entre le zinc et une solution d’ion cuivre II

Classe de troisième Chimie Chapitre 8
2
a. Bilan chimique
Lorsque l’on introduit du zinc dans une solution de sulfate de cuivre II. On constate plusieurs
choses :
Une élévation de la température : on passe de 21, 0°C à 48,2°C
Un dépôt de cuivre se forme sur le zinc
La disparition des ions cuivre II : la solution se décolore.
On peut conclure que lors de cette transformation chimique :
les ions cuivre II sont consommés tandis que du cuivre est
produit. L’élévation de température nous informe que cette
transformation chimique produit de l’énergie sous forme de
chaleur.
b) Bilan énergétique
La chaleur crée lors de la réaction du zinc et des ions cuivre provient de l’énergie chimique des
réactifs. Lors de la rupture des liaisons des réactifs de l’énergie est libérée : une partie est utilisée
pour former les produits (dont le cuivre), une autre partie est diffusée dans l’environnement : ça
chauffe !
2) La pile cuivre/zinc
a) Sans séparation
Dans cette pile, deux plaques : une en zinc et l’autre en cuivre trempent
dans une solution contenant des ions cuivre II. Ions identifiables grâce à
la soude puisqu’ils forment un précipité bleu. On mesure une tension
d’environ 0,82 V, il y a bien fabrication de courant électrique, notre pile
fonctionne !
Si on laisse la pile fonctionner longtemps, on observe que :
Du cuivre se dépose sur la plaque de zinc et tombe au fond du bécher
La plaque de zinc a diminuée
La solution perd sa couleur bleutée
Apparition d’ions zinc dans la solution, caractérisés par la soude.
On conclut que lors de son fonctionnement, des réactions chimiques ont lieu :
Formation de cuivre, Disparition du zinc, Disparition des ions cuivre II, Appartion des ions zinc II.

Classe de troisième Chimie Chapitre 8
3
La pile s’arrètera de fonctionner lorsqu’il n’y aura plus de réactifs : consommation totale de la
plaque de zinc et/ou des ions cuivre II.
b) Avec séparation (Hors programme)
Pour éviter le dépôt de cuivre sur la plaque de zinc qui
parasite la formation de Zn
2+
et donc le fonctionnmeent
de notre pile, on sépare les deux plaques dans deux
solutions différentes.
Parler du rôle du pont salin : il faut que le circuit soit
fermé !!
III)
La pile, convertisseur et réservoir d’énergie
1) Bilan énergétique d’une pile
Le rôle d’une pile est de fournir de l’énergie électrique au circuit. Cette énergie électrique, nous
l’avons vu, provient des réactions chimiques qui ont lieu dans la solution et se répartit suivant le
diagramme suivant :
2) La pile, un réservoir d’énergie
La pile fonctionne tant qu’elle contient des réactifs à transformer. Lorsque l’un des réactifs est
épuisée, elle cesse de fonctionner : elle est usée. Dans le cas de notre pile, soit il n’y a plus d’ion
Cuivre II, soit il n’y a plus de zinc :

Classe de troisième Chimie Chapitre 8
4
Pour conclure :
https://www.youtube.com/watch?v=mItO3l82Ic0
3) Les différentes piles du commerce
Les piles du commerce sont de trois types :
- La pile saline (ou pile Leclanché)
:
c’est la plus ancienne et la moins chère mais sa
durée de vie est courte. Elle délivre une tension de 1,5 V.
On l’utilise pour des utilisations peu exigeantes : réveil, jouets…
- La pile alcaline : de constitution très proche de la pile saline, elle délivre une tension de
1,5V mais peut fournir des courants plus importants pendant plus longtemps. Elle est
plus chère.
Elle convient à des usages plus exigeants : appareils photo, mp3….
- La pile au lithium :
Elle est encore plus chère, mais délivre beaucoup plus d’énergie que
les précédentes. Sa tension peut varier de 1,2V à 3,5V. Elle permet un usage de longue
durée.
On l’utilise dans les calculatrices, montre, stimulateurs cardiaques
…

5
Objectifs :
- Savoir qu’une pile est un réservoir d'énergie chimique.
- Savoir que lors de son fonctionnement l’énergie chimique est transférée sous d'autres formes.
- Savoir que l’énergie mise en jeu dans une pile provient d’une réaction chimique ; et que la consommation de
réactifs entraîne l’usure de la pile.
- Savoir réaliser, décrire et schématiser la réaction entre une solution aqueuse de sulfate de cuivre et de la
poudre de zinc : - par contact direct
- en réalisant une pile.
Objectifs :
- Savoir qu’une pile est un réservoir d'énergie chimique.
- Savoir que lors de son fonctionnement l’énergie chimique est transférée sous d'autres formes.
- Savoir que l’énergie mise en jeu dans une pile provient d’une réaction chimique ; et que la consommation de
réactifs entraîne l’usure de la pile.
- Savoir réaliser, décrire et schématiser la réaction entre une solution aqueuse de sulfate de cuivre et de la
poudre de zinc : - par contact direct
- en réalisant une pile.
Objectifs :
- Savoir qu’une pile est un réservoir d'énergie chimique.
- Savoir que lors de son fonctionnement l’énergie chimique est transférée sous d'autres formes.
- Savoir que l’énergie mise en jeu dans une pile provient d’une réaction chimique ; et que la consommation de
réactifs entraîne l’usure de la pile.
- Savoir réaliser, décrire et schématiser la réaction entre une solution aqueuse de sulfate de cuivre et de la
poudre de zinc : - par contact direct
- en réalisant une pile.
Objectifs :
- Savoir qu’une pile est un réservoir d'énergie chimique.
- Savoir que lors de son fonctionnement l’énergie chimique est transférée sous d'autres formes.
- Savoir que l’énergie mise en jeu dans une pile provient d’une réaction chimique ; et que la consommation de
réactifs entraîne l’usure de la pile.
- Savoir réaliser, décrire et schématiser la réaction entre une solution aqueuse de sulfate de cuivre et de la
poudre de zinc : - par contact direct
- en réalisant une pile.
Objectifs :
- Savoir qu’une pile est un réservoir d'énergie chimique.
- Savoir que lors de son fonctionnement l’énergie chimique est transférée sous d'autres formes.
- Savoir que l’énergie mise en jeu dans une pile provient d’une réaction chimique ; et que la consommation de
réactifs entraîne l’usure de la pile.
- Savoir réaliser, décrire et schématiser la réaction entre une solution aqueuse de sulfate de cuivre et de la
poudre de zinc : - par contact direct
- en réalisant une pile.
Objectifs :
- Savoir qu’une pile est un réservoir d'énergie chimique.
- Savoir que lors de son fonctionnement l’énergie chimique est transférée sous d'autres formes.
- Savoir que l’énergie mise en jeu dans une pile provient d’une réaction chimique ; et que la consommation de
réactifs entraîne l’usure de la pile.
- Savoir réaliser, décrire et schématiser la réaction entre une solution aqueuse de sulfate de cuivre et de la
poudre de zinc : - par contact direct
- en réalisant une pile.
 6
6
 7
7
1
/
7
100%