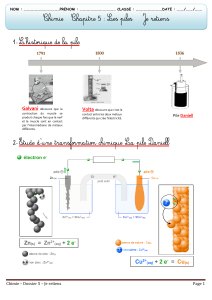
TP : Pile électrochimique

Objectif n°1: Une réaction chimique peut-elle produire de l’énergie?
Liste du matériel: - bécher
- sulfate de cuivre
- zinc
- thermomètre.
- Hydroxyde de soium
- Tube à essai.
Protocole: Dans un bécher, introduire la solution de sulfate de cuivre.
Peser l’ensemble.
Introduire le zinc préalablement pesé.
Placer un thermomètre et noter la temprérature.
Observer les changements d’aspects du mélange et noter la température toutes les
minutes.
Peser l’ensemble à la fin de la réaction.
Schéma de l’expérience:
Observations:
………………………………………………………………………………………………………
………………………………………………………………………………………………………
………………………………………………………………
Tableau de mesures:
Temps en
min
Température
en °C
Questions:
1) Quels sont les réactifs ? ……………………………………………………
2) Comment met-on en évidence l’ion cuivre?.....................................................
3) A la fin de la réaction, placer un peu de solution présente dans le bécher, dans un tube à
essai et verser de l’hydroxyde de sodium. Que constate-t-on?
………………………………………………………………………………….
4) Après observations, quels sont les produits formés?
…………………………………………………………………………………….
On a pésé les réactifs avant la réaction et l’ensemble des produits aprés la réaction
5) Que constate-t-on? ………………………………………………………………………
6) Que libère la réaction chimique? ……………………………………………………….
Conclusion: Ecrire sur ce qui se passe lors d’une réaction chimique.
………………………………………………………………………………………………………
………………………………………………………………………………………………
La Pile Electrochimique

Objectif n°2: Que se passe-t-il dans une pile électrochimique?
Liste du matériel: - bécher
- cuivre
- zinc
- sulfate de cuivre en solution
- pinces crocodile
- multimètres
- fils de connexion
- résistor ( “résistance”)
Protocole: Placer dans un bécher environ 100mL d’eau et deux cuillièrées de sulfate de cuivre.
Introduire les lames de cuivre et de zinc dans la solution de sulfate de cuivre.
Mesurer la tension aux bornes de ces deux lames.
Puis réaliser un circuit, en placant en série, les deux lames, une résistance et un
ampéremètre.
Schéma de l’expérience :
Observations:
1. Quelle est la valeur de la tension mesurée entre les deux plaques?..........................................
2. Quelle est la valeur de l’intensité mesurée dans le circuit? ………………………………….
3. Quelles modifications d’aspect observe-t-on dans le bécher?
………………………………………………………………………………………………………
………………………………………………………………………………………………………
Interprétation:
1. Pourquoi peut-on dire que le montage constitue un générateur? Identifer les bornes de la
pile.
………………………………………………………………………………………………………
………………………………………………………………………………………………………
2. Quel est le sens du courant? Placer sur le schéma le sens du courant et le sens de
déplacement des électrons dans le circuit.
3. Montrer que la pile est le siège d’une réaction chimique. Quels sont les réactifs et les
produits?
………………………………………………………………………………………………………
………………………………………………………………………………………………………
………………………………………………………………………………………………………
Conclusion: répondre à l’objectif.
………………………………………………………………………………………………………
………………………………………………………………………………………………………
………………………………………………………………………………………………………
1
/
2
100%