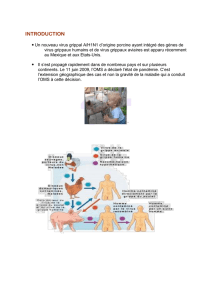
Virus de la grippe: deux pistes pour de nouveaux traitements

Revue Médicale Suisse
–
www.revmed.ch
–
11 mars 2009 605
Virus de la grippe: deux pistes
pour de nouveaux traitements
Lapandémie de grippe à virus
H5N1 n’a beau rester qu’une me-
nace, ce virus continue à faire des
victimes, en Asie principalement, et les
épidémies saisonnières de grippe tuent
toujours des milliers de personnes dans
le monde. Deux nouvelles voies vien-
nent de s’ouvrir pour améliorer les trai-
tements contre la grippe. La première
est de bloquer les mécanismes préco-
ces d’entrée du virus dans les cellules
humaines, en dirigeant des anticorps vers
une cible déjà classique: l’hémaggluti-
nine. La seconde vise quant à elle les
virus ayant déjà pénétré à l’intérieur des
cellules, en les empêchant de détour-
ner la machinerie de la cellule-hôte pour
se multiplier. Ces nouvelles pistes ap-
paraissent au moment où les Centres
américains pour la surveillance et le
contrôle des maladies annoncent que
sur les 325 virus H1N1 testés prove-
nant de la saison de grippe 2008-2009
aux Etats-Unis, 321 (98,8%) étaient ré-
sistants à l’oseltamivir (Tamiflu).1
Découverte d’anticorps à large
spectre
La difficulté de mettreau point un
vaccin durablement efficace contre la
grippe est liée à la variabilité des
hémagglutinines présentes à la surface
des virus. Ces protéines sont néces-
saires à la reconnaissance des cellules
et à l’endocytose du génome viral dans
le cytoplasme cellulairegrâce à la fu-
sion des membranes virale et cellulaire.
Des chercheurs américains dirigés par
Wayne Marasco, du Département de
médecine de la HarvardMedical School,
ont isolé à partir de dizaines de millions
d’anticorps monoclonaux humains une
petite famille de protéines capables de
contrer les quatre souches majeures
de H5N1 et tous les virus de la grippe
de type A, dont celui de la grippe es-
pagnole et des grippes saisonnières
(H1N1).2Ils ont ensuite déterminé la
structure atomique de la zone où se
fixent les anticorps: il s’agit d’une poche
située à la base des hémagglutinines
au niveau du peptide de fusion, dont la
séquence est très conservée entre les
virus. Lorsque les anticorps se fixent à
cette poche, les virus ne peuvent chan-
ger de forme, une étape requise pour la
fusion membranaire qui est alors inhi-
bée. In vivo, des souris infectées par
des doses létales de virus ont survécu
grâce à l’injection de ces anticorps. Ces
découvertes pourraient ainsi permettre
de rediriger la réponse immunitaire des
vaccins, qui ciblent jusqu’à présent la
tête des hémagglutinines en constante
mutation, pour obtenir une immunité dé-
finitive.
La technique du vol de coiffe élucidée
Le mécanisme par lequel le virus de
la grippe se réplique à l’intérieur des
cellules est bien connu:la polymérase
du virus de la grippe, composée de trois
chaînes PA, PB1 et PB2, réplique dans
le cytoplasme de la cellule hôte les huit
fragments d’ARN qui composent le gé-
nome du virus. C’est également elle qui
initie la traduction de l’ARN viral en pro-
téines:elle coupe les coiffes des ARN
messagers de la cellule hôte, un méca-
nisme littéralement appelé «cap-snat-
ching» ou «vol de coiffe», et en revêt les
ARN viraux. Leurrée, la machinerie cel-
lulaire reconnaît les coiffes et synthétise
les protéines virales.
Si l’on sait que c’est la sous-unité
PB2 qui reconnaît la coiffe à subtiliser
et s’y fixe, on supposait que soit PB1,
soit PB2 permettait de la cliver. C’est
en fait la sous-unité PA qui joue ce rôle
endonucléasique, comme l’ont notam-
ment démontré des études biochimiques
menées au sein du Laboratoire euro-
péen de biologie moléculaire (EMBL)
de Grenoble.3L’obtention de la struc-
ture tridimensionnelle de cette sous-
unité a permis de repérer le site actif de
cette sous-unité, qui est conservé chez
les trois souches virales utilisées, dont
deux humaines (Victoria et Johannes-
burg) et une aviaire. «PAest une cible
thérapeutique antivirale prometteuse.
L’inhibition du clivage de la coiffe est
un moyen efficace d’enrayer l’infection
car dans ce cas, le virus n’est plus en
mesurede se multiplier.Nous savons
désormais où concentrer nos efforts en
matière de développement de médica-
ments», précise Stephen Cusack, res-
ponsable de l’EMBL et qui a participé à
l’une des études.
Marina Casselyn
1www.cdc.gov/flu/weekly/
2Sui J, Hwang W,Perez S, et al. Structural and functio-
nal bases for broad-spectrum neutralization of avian and
human influenza A viruses. Nat Struct Mol Biol 2009;
édition en ligne du 22 février.
3Dias A, Bouvier D, Crépin T, et al. The cap-snatching
endonuclease of influenza virus polymerase resides in
the PAsubunit. Nature2008; édition en ligne du 4 février.
actualité, info
0Revue Médicale Suisse
–
www.revmed.ch
–
12 janvier 2008
Représentation 3D de la polymé-
rase du virus de la grippe
Structure du virus de la grippe
Adroite: un des trois monomères de l’hémagglutinine
Crédit:Wang T. et Palese P., Nat Struct Mol Biol 2009, édition en ligne du 22 février
Site de liaison
aux récepteurs
cellulaires
Génome viral (ARN)
et protéines
Hémagglutinine
Neuraminidase
M1 M2
Membrane
lipidique
Peptide
de fusion
33999_605.qxp 6.3.2009 8:57 Page 1
1
/
1
100%