pratique quotidienne Nécrose médullaire chez deux patients atteints

pratique quotidienne
Nécrose médullaire chez deux patients atteints
de maladies cancéreuses
Bone marrow necrosis in two patients with neoplastic disorders
J. Gérard
1
B. Berdin
2
G. Portier
3
A. Godon
1
A. Tessier-Marteau
1
F. Geneviève
1
M. Zandecki
1
1
Laboratoire d’hématologie biologique,
Centre hospitalo-universitaire, Angers
2
Département de biologie,
Centre hospitalier, Laval
3
Service de chirurgie viscérale,
Centre hospitalier, Laval
Article reçu le 6 juin 2007,
accepté le 27 juillet 2007
Résumé.L’observation d’une nécrose du tissu myéloïde et du stroma médul-
laire dans de larges régions de la moelle osseuse hématopoïétique correspond à
la définition de l’état de nécrose médullaire. Le diagnostic se réalise sur
l’aspect cytologique particulier du myélogramme et/ou de la biopsie ostéo-
médullaire. Nous en rapportons ici deux observations. Le premier patient est
âgé de 75 ans et hospitalisé pour hyperthermie, asthénie et lombalgies bilatéra-
les. Une hémopathie est évoquée par l’existence de quelques blastes sanguins,
mais le myélogramme montre un aspect de nécrose médullaire et ne permet pas
de diagnostic complémentaire. Dans les jours suivants, l’hyperleucocytose et la
blastose se majorent, permettant le diagnostic de leucémie aiguë monoblasti-
que. Une chimiothérapie est instaurée mais le patient décède rapidement. Le
second patient, âgé de 28 ans, présente une tumeur gastrique métastasée dont
l’exploration avant traitement se termine lorsque son état général se dégrade
brusquement. Le myélogramme réalisé pour explorer une thrombopénie mon-
tre une nécrose médullaire massive. L’état général du patient se dégrade très
rapidement et il décède quelques jours après son hospitalisation. Dans la litté-
rature la nécrose médullaire est secondaire dans la majorité des cas à une
hémopathie (60 % des cas) ou à une tumeur solide (30 % des cas), plus rare-
ment à d’autres causes. Les douleurs osseuses et la fièvre sont fréquemment
mentionnées, associées à des cytopénies d’importance variable avec augmenta-
tion des lactates déshydrogénases et phosphatases alcalines sériques, toutes
anomalies non spécifiques, surtout dans le cadre de maladies cancéreuses.
L’examen médullaire permet le diagnostic : les cellules sont pycnotiques, non
identifiables, au sein d’un matériel grisâtre ou orangé, et l’histologie quand elle
est réalisée montre une disparition des espaces graisseux avec préservation du
tissu osseux. L’hypoxémie tissulaire après défaillance de la microcirculation
est le mécanisme le plus souvent mis en avant pour expliquer la nécrose, quelle
que soit la maladie causale. Outre un traitement symptomatique adapté, le
traitement rapide de la maladie causale est nécessaire. Le pronostic, bien que
lié à maladie sous-jacente, est souvent péjoratif quand la nécrose médullaire est
étendue.
Mots clés :
nécrose médullaire, lyse cellulaire, pancytopénie, leucémie, cancer
Abstract.Bone marrow necrosis is defined by extensive necrosis of the mye-
loid tissue and bone marrow stroma. Diagnosis is done on characteristic cytolo-
gical pattern of the bone marrow aspiration and/or biopsy. We report two
observations. The first patient, aged 75, has been hospitalized for fever, asthe-
nia and lower back pain. An haematological malignancy was suspected after
observation of a few peripheral blood blast cells, but necrosis was found on the
bone marrow aspiration and could not lead to further haematological diagnosis.
Within next days, the white blood cell count and the number of blasts
increased, leading to the diagnosis of acute monoblastic leukaemia. A chemo-
therapy was started but the patient died 20 days after admission. The second
abc
Ann Biol Clin 2007 ; 65 (6) : 636-42
doi: 10.1684/abc.2007.0173
Ann Biol Clin, vol. 65, n° 6, novembre-décembre 2007636
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 25/05/2017.

patient, aged 28, has been hospitalized for severe bleeding a few days after the
diagnosis of a metastatic gastric tumour. The bone marrow aspiration, made for
the evaluation of a thrombocytopenia, showed a massive necrosis. The patient
deceased shortly after hospitalization. According to literature, bone marrow
necrosis is in most instances secondary to either an haematological malignancy
(60%) or to a solid tumour (30%), but only at times observed with a non-
malignant disorder. Bone pain, fever, cytopenias and elevated serum lactic
dehydrogenase and alkaline phosphatase are frequently reported, but are
mostly non specific of the diagnosis in these malignant conditions. Examina-
tion of the bone marrow leads to the diagnosis: cells are pycnotic, scarcely
recognizable in a background of amorphous extracellular eosinophilic protei-
naceous material, and histology shows disappearance of fat spaces with preser-
vation of the bone tissue. Tissue hypoxemia due to microcirculation failure
may be the main mechanism leading to the necrosis, whatever the related
disorder. Supportive care together with specific therapy of the causal disease
must be started promptly. The prognosis depends on the underlying illness and
is generally very poor when extensive necrosis is observed.
Key words:bone marrow necrosis, cellular lysis, pancytopenia, leukaemia,
neoplasia
L’observation 1
Un homme de 75 ans est hospitalisé pour hyperthermie
(38 °C), asthénie et lombalgies bilatérales. Il a comme
antécédent notable une neurofibromatose de Recklinghau-
sen diagnostiquée 20 ans auparavant. L’examen clinique
est sans particularité et il n’y a pas de point d’appel infec-
tieux évident. L’hémogramme montre une hyperleucocy-
tose (25 G/L) avec polynucléose neutrophile (14 G/L),
monocytose (3 G/L), érythromyélémie (3 % d’érythro-
blastes et 8 % de granulocytes immatures), 5 % de blastes
et une thrombopénie (96 G/L). L’anémie est initialement
absente (hémoglobine = 13,5 g/dL ; N = 13-17 g/dL).
Dans les jours suivants, l’état du patient se dégrade et
nécessite le transfert en réanimation médicale. On observe
des crépitants bilatéraux des bases pulmonaires et une
hépato-splénomégalie, et sur le plan biologique on trouve
une augmentation des phosphatases alcalines sériques
(PAL = 780 UI/L ; N = 33-125 UI/L), de la gamma gluta-
myl transpeptidase (880 UI/L ; N = 11-69 UI/L) et des
lactates déshydrogénases (LDH = 2 800 UI/L ; N = 210-
390 UI/L), avec une discrète cytolyse hépatique
(ALAT = 88 UI/L ; N = 12-60 UI/L ; ASAT normales).
Une anémie apparaît en quelques jours (hémoglo-
bine = 9,4 g/dL) en partie liée à l’hémodilution secondaire
au remplissage vasculaire. La ponction sternale est réali-
sée et le myélogramme montre des altérations morpholo-
giques majeures des cellules myéloïdes, avec contour
indistinct, taille réduite, noyau lytique et cytoplasme en
dégénérescence (figure 1A et B). Les quelques cellules
identifiables correspondent à des blastes d’aspect monocy-
toïde : l’aspect oriente vers un état de nécrose médullaire
(NM) dans le cadre d’une probable leucémie aiguë mono-
cytaire. L’évolution sur le plan hématologique est mar-
quée par une augmentation rapide de la leucocytose (de 13
à 84 G/L en 6 jours), constituée majoritairement de mono-
blastes (figure 2), et d’une majoration des cytopénies. Un
traitement par Hydrea
®
est débuté immédiatement, mais la
détresse respiratoire s’aggrave et l’évolution devient pro-
gressivement défavorable avec décès 20 jours après le
début de l’hospitalisation.
L’observation 2
Un homme de 28 ans, sans antécédent particulier, consulte
un gastro-entérologue pour douleur épigastrique résistant
aux inhibiteurs de la pompe à protons. Une gastroscopie et
une biopsie gastrique sont réalisées et permettent le
diagnostic d’adénocarcinome peu différencié à cellules
indépendantes. L’examen clinique montre également de
nombreuses adénopathies évocatrices de métastases gan-
glionnaires. L’hémogramme est normal. Un site implanta-
ble sous-cutané est installé en prévision d’une chimiothé-
rapie. Trois jours plus tard, alors que la chimiothérapie n’a
pas encore débuté, le patient est hospitalisé pour l’appari-
tion d’un hématome au niveau du bras et de l’épaule gau-
ches. L’hémogramme montre une anémie modérée
(hémoglobine = 11,5 g/dL) et une thrombopénie (74 G/L ;
N = 150-400 G/L). Les LDH sont très élevés (2 875 UI/L)
et les PAL discrètement augmentés (146 UI/L). Le taux de
prothrombine abaissé (38 %), le facteur V à 32 % (N = 70-
Nécrose médullaire
Ann Biol Clin, vol. 65, n° 6, novembre-décembre 2007 637
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 25/05/2017.

130 %), et le fibrinogène à 0,6 g/L (N = 2-4 g/L) orientent
vers une coagulation intravasculaire diffuse. Le myélo-
gramme est richement cellulaire, mais toutes les cellules
sont inidentifiables. L’aspect est celui d’une NM (figure
3A et B), probablement dans le cadre d’une dissémination
de la maladie initiale, bien que l’examen attentif des frot-
tis ne permette pas d’affirmer avec certitude la présence
d’amas métastatiques. L’évolution est rapidement défavo-
rable, avec défaillance polyviscérale et aggravation des
cytopénies : malgré la mise en place d’une réanimation
adaptée le décès du patient survient 7 jours après son
admission au centre hospitalier.
Commentaires
La NM répond à la définition de « nécrose extensive du
tissu myéloïde et du stroma médullaire dans de larges
régions de la moelle osseuse hématopoïétique ». C’est sur
l’examen de la moelle osseuse (ponction ou biopsie) que
le diagnostic sera évoqué. Selon les séries, sa prévalence a
été rapportée comme variant de 0,3 à 37 % [1-4], mais
cette grande amplitude s’explique en premier lieu par les
critères de définition retenus, et notamment l’importance
de son extension au sein du tissu myéloïde. La première
étude documentée sur le sujet avait montré que chez 316
patients décédés de leucémie aiguë l’interprétation initiale
de la biopsie ostéomédullaire n’avait reconnu cette
nécrose que dans 4 cas (1,3 %), mais que la relecture
histologique retrouvait des foyers de nécrose dans 34 cas
(10,7 %) [5]. La population étudiée a également son
importance : les prélèvements autopsiques montrent plus
fréquemment des images de nécrose, et les séries les plus
anciennes s’adressent à des patients pour lesquels les res-
sources thérapeutiques contre la maladie sous-jacente
étaient plus limitées qu’aujourd’hui (chimiothérapie anti-
cancéreuse notamment). En ne retenant que les aspects
typiques au myélogramme ou à la biopsie ostéomédullaire
(voir plus loin) et en se limitant aux patients vivants il
semble qu’une prévalence de 0,3-0,4 % doive être retenue
[6].
La NM est secondaire à une maladie sous-jacente, presque
toujours de nature cancéreuse (plus de 90 % des cas) [6]
(tableau 1). Les hémopathies malignes sont au premier
plan, correspondant à des leucémies aiguës lymphoïdes ou
myéloïdes (tous types), à des syndromes myéloproliféra-
tifs (essentiellement la leucémie myéloïde chronique) ou à
des lymphomes (maladie de Hodgkin, ou lymphomes non
B
A
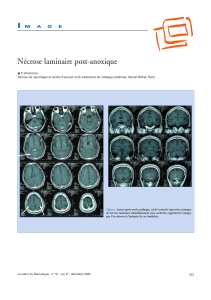
Figure 1. A : observation 1. L’étalement médullaire est richement
cellulaire, mais toutes les cellules ont un contour indistinct, et
l’espace intercellulaire est plus ou moins de coloration grisâtre ou
orangée (myélogramme, coloration MGG ; X 200). B: observa-
tion 1. Au fort grossissement les cellules ne sont pas identifia-
bles : elles ont une taille réduite dépassant à peine la taille d’une
hématie, avec un noyau pycnotique, des contours externes mal
délimités, et on note la présence de fines ponctuations autour
des cellules (myélogramme, coloration MGG ; X 500).
Figure 2. Observation 1. Dans les jours qui suivent l’hospitalisa-
tion l’hyperleucocytose se majore, constituée essentiellement de
monoblastes (frottis sanguin, coloration MGG ; X 1 000).
pratique quotidienne
Ann Biol Clin, vol. 65, n° 6, novembre-décembre 2007638
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 25/05/2017.

hodgkiniens de faible ou forte malignité). La pratique fré-
quente de l’examen de la moelle osseuse (myélogramme
ou biopsie ostéomédullaire) en situation hématologique
est peut-être une explication de cette représentation éle-
vée. L’existence d’une tumeur solide est la seconde situa-
tion fréquente de NM. La tumeur primitive n’est pas tou-
jours identifiée, même après une recherche approfondie
(25 % des cas), mais on remarque une surreprésentation
des cancers gastriques (30 % des cas) [6], comme pour
l’observation 2. Selon les cas, la NM est décrite au dia-
gnostic de la maladie, après chimiothérapie ou à la rechute
[6].
Dans quelques cas la NM s’observe au cours des maladies
non cancéreuses (tableau 1). La drépanocytose a été la
première décrite comme associée à la NM [7, 8]. Parmi les
infections sévères, celle associée au VIH semble dominer
actuellement [4]. Ponctuellement la NM a été rapportée au
cours de traitements médicamenteux, notamment en
contexte hématologique (interféron alpha, acide tout
transrétinoïque ou ATRA, fludarabine), et dans d’autres
pathologies, ayant un lien avec des anomalies de la micro-
circulation (microangiopathies thrombotiques, CIVD
associée ou non à une maladie métastatique, syndrome
des antiphospholipides) ou non (hyperparathyroïdie)
(tableau 1). Au cours de l’anorexie mentale la NM est
parfois rapportée, mais moins fréquemment qu’une situa-
tion proche et discutée plus loin, la transformation gélati-
neuse de la moelle osseuse [9].
Le point de vue du clinicien
Il n’existe pas de signes cliniques particuliers à la NM.
Celle-ci survient en outre le plus souvent dans un contexte
de maladies cancéreuses, avec leurs spécificités propres ou
qui ont déjà bénéficié d’un traitement adapté. C’est dans
ce contexte qu’il faudra savoir évoquer la possibilité d’une
NM. Les douleurs osseuses sont retrouvées dans 80 % des
cas, aiguës, intenses, disséminées ou localisées dans le bas
du dos, et constituent la principale cause d’hospitalisation
des patients [6]. Elles sont plus fréquentes quand la NM
est secondaire à une leucémie aiguë, mais les douleurs
osseuses sont en elles-mêmes fréquentes au cours des leu-
cémies aiguës, notamment lymphoblastiques chez
l’enfant, indépendamment d’une NM. La fièvre, retrouvée
dans environ 70 % des cas, peut être reliée au processus de
nécrose tissulaire aussi bien qu’à la neutropénie parfois
observée [4]. La fatigue, souvent mentionnée, peut être
reliée à l’anémie secondaire à la NM tout comme à la
maladie préexistante. Finalement la pancytopénie est pos-
sible, mais ne permet pas d’orientation particulière dans
un contexte où les maladies cancéreuses sont fréquentes.
Tout signe hémorragique devra être recherché avec atten-
tion, la thrombopénie pouvant être aussi bien centrale
(maladie initiale, nécrose) que périphérique (CIVD
notamment), comme c’était le cas pour l’observation 2. La
présence d’un ictère, clinique ou biologique, est égale-
ment mentionnée dans 40 % des cas de la littérature, mais
pas chez nos 2 patients. Quelques observations de la litté-
rature signalent l’existence d’une embolie pulmonaire et
d’une embolie graisseuse secondaires à la dégénérescence
médullaire [6].
Le bilan étiologique des douleurs osseuses et de la fièvre
amène à réaliser des explorations complémentaires,
incluant l’imagerie et la réalisation d’un myélogramme
après ponction sternale, éventuellement suivi d’une biop-
sie ostéomédullaire, qui va permettre le diagnostic : même
en l’absence d’affirmation concernant la maladie causale,
la recherche d’une maladie cancéreuse (tumeur solide,
hémopathie) doit être privilégiée. L’imagerie convention-
B
A
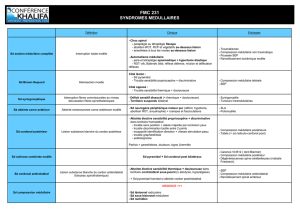
Figure 3. A : observation 2. L’aspect de nécrose médullaire est
superposable à celui de l’observation 1 (figure 1) ; les cellules
sont pycnotiques sur un fond de matériel granulaire (myélo-
gramme, coloration MGG ; X 200). B: observation 2. La dégéné-
rescence du stroma est vraisemblablement responsable de
l’aspect granulaire de l’espace intercellulaire (myélogramme,
coloration MGG ; X 500).
Nécrose médullaire
Ann Biol Clin, vol. 65, n° 6, novembre-décembre 2007 639
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 25/05/2017.

nelle peut montrer des anomalies osseuses en rapport avec
une localisation tumorale, mais elle ne visualise pas
l’existence de la NM, même étendue, car il n’y a pas de
remaniement osseux, au moins les premiers temps. Si une
scintigraphie osseuse est réalisée, elle montre une absence
de fixation de l’isotope dans tous les espaces osseux
nécrosés, visualisant l’extension de la nécrose et permet-
tant d’apprécier l’existence de territoires encore hémato-
gènes ; elle permettra d’observer la réapparition de
l’hématopoïèse chez les patients évoluant favorablement.
L’imagerie par résonance magnétique permet elle aussi
d’évaluer l’étendue de la nécrose, par le changement de
l’intensité du signal secondaire aux variations des propor-
tions de lipides et d’eau contenus dans les éléments cellu-
laires : dans les NM extensives on peut observer au niveau
des cavités osseuses hématogènes (vertèbres, pelvis) une
image caractéristique correspondant à une zone centrale
d’intensité variable entourée par une couronne périphéri-
que distincte hyperdense [10].
Outre le traitement symptomatique, la transfusion de
concentrés érythrocytaires et/ou plaquettaires est parfois
nécessaire, avec une antibiothérapie adaptée devant toute
suspicion d’infection. Selon l’étiologie le traitement spé-
cifique sera instauré au plus vite, et concernant notamment
les tumeurs malignes la chimiothérapie doit être débutée
dès que possible. La survie des patients dépend essentiel-
lement de la maladie primitive et aucune publication ne
prouve statistiquement que la NM soit un facteur indépen-
dant de mauvais pronostic [6]. Il apparaît cependant que le
pronostic dépend principalement de la pathologie sous-
jacente lorsque la NM est modérée, alors que l’issue est
plus souvent fatale quand elle est étendue (plus de 50 %
du tissu hématopoïétique atteint) [4, 6]. Dans les deux
observations présentées l’évolution a été rapidement défa-
vorable, mais il s’agissait pour un patient d’une leucémie
aiguë monoblastique du sujet âgé, dont il n’existe pas
actuellement de traitement efficace, et pour l’autre patient
d’une tumeur maligne avec métastases multiples. Quand
un traitement symptomatique et un traitement spécifique
de la maladie causale se révèlent efficaces, la reconstitu-
tion du tissu hématopoïétique est observée et le pronostic
général rejoint celui de la maladie initiatrice [4, 6].
Le point de vue du biologiste
La NM correspond à diverses altérations cytologiques et
histologiques de la moelle osseuse hématopoïétique. Elle
est secondaire à une maladie cancéreuse (tumeur solide ou
hémopathie) dans 90 % des cas : les anomalies hématolo-
giques et biochimiques observées au niveau du sang péri-
phérique sont autant celles de la maladie sous-jacente que
liées à la NM en elle-même. L’anémie et la thrombopénie
sont presque constantes (91 % et 78 % des cas, respective-
ment). L’anémie s’installe rapidement, souvent dans les
jours qui suivent les douleurs osseuses : outre qu’elle peut
être préexistante à la nécrose, elle sera souvent majorée
par l’hémodilution en cours de réanimation. Le nombre
des leucocytes est augmenté (25 % des cas), normal (40 %
des cas) ou abaissé, et correspond souvent à des variations
du nombre des neutrophiles, avec parfois neutropénie
sévère [4]. Une érythromyélémie est rapportée dans la
moitié des cas [6], mais il s’agit également d’un signe non
spécifique d’une localisation métastatique osseuse. La
présence de blastes est presque constante quand il s’agit
d’une NM dans le cadre d’une leucémie aiguë (comme
c’était le cas pour l’observation 1), ce qui justifie une
étude attentive de l’hémogramme, même rétrospective,
surtout lorsqu’une NM est diagnostiquée sans orientation
concernant la maladie sous-jacente. Les anomalies biochi-
miques, essentiellement une augmentation des LDH, des
PAL sériques ou/et des transaminases, sont retrouvées
dans 40 à 50 % des cas, mais là encore elles peuvent
correspondre à la NM aussi bien qu’à la maladie sous-
jacente [6]. Un bilan d’hémostase doit être systématique-
ment réalisé car une CIVD est parfois retrouvée, primitive
ou secondaire (à la dissémination métastatique en premier
lieu), comme dans l’observation 2.
La ponction aspiration médullaire est parfois un échec
(ponction « blanche ») et il peut être nécessaire de répéter
Tableau 1. Maladies sous-jacentes ou associées aux nécroses médullaires. Les maladies cancéreuses (hémopathies et tumeurs
solides) sont les plus fréquemment citées.
Pathologies malignes (90 %) Maladies non cancéreuses (10 %)
Hémopathies (60 %)
Leucémies aiguës lymphoïdes
Leucémies aiguës myéloïdes (tous types)
Leucémie myéloïde chronique (plus rarement un autre syndrome
myéloprolifératif)
Lymphomes (maladie de hodgkin et lymphomes non-hodgkiniens)
Drépanocytose (2 %)
Infections (3 %)
Sepsis sévère
Tuberculose
Virales (Parvovirus, VIH)
Tumeurs solides (30 %)
Tumeur primitive non identifiée (25 % des cas)
Tumeur gastrique (30 % des cas)
Autres types, avec métastases médullaires
(poumon, ovaires, autres...)
Divers (5 %)
Médicaments (interféron alpha, ATRA...)
Microangiopathies thrombotiques ou coagulation intravasculaire disséminée
Syndrome des antiphospholipides
Anorexie mentale
pratique quotidienne
Ann Biol Clin, vol. 65, n° 6, novembre-décembre 2007640
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 25/05/2017.
 6
6
 7
7
1
/
7
100%