Lire l`article complet

70 | La Lettre du Neurologue • Vol. XIII - n° 3 - mars 2009
MISE AU POINT
Motivation et récompense :
le point de vue
des neurosciences cognitives
Motivation and reward: views from cognitive neuroscience
M. Pessiglione*
* Chargé de recherche Inserm, hôpital
de la Pitié-Salpêtrière, Paris.
“
Bonjour monsieur, comment vous sentez-
vous ?”
– Je me sens bien physiquement, mais… j’ai des diffi-
cultés à… faire beaucoup de choses… à part la routine…
je n’arrive pas à me stimuler assez… pour y arriver.
- Et vous madame, pouvez-vous nous expliquer ce
qui se passe avec votre mari ?
- Ben, il est motivé pour rien, faut toujours lui dire
de faire les choses, être toujours derrière lui.”
Comme dans cet exemple, l’entretien clinique
fait parfois apparaître un manque de motivation,
c’est-à-dire une apathie, chez les patients atteints
de pathologie neurologique, ici la maladie de
Parkinson. Comment, au-delà des échelles et des
questionnaires, objectiver ce symptôme et aborder
les mécanismes sous-jacents ?
La motivation est d’abord un concept du sens
commun, que l’on comprend intuitivement mais qui
est difficile à définir. Comme l’épouse de notre patient,
on aura tendance à dire de quelqu’un qui ne fait pas
d’effort qu’il n’est pas motivé. On se demande aussi
parfois quelle est la motivation (ou le motif) d’une
action : pourquoi s’engager dans telle tâche plutôt
que dans telle autre ? Une explication en termes moti-
vationnels doit donc rendre compte non seulement
de l’ “énergisation” (combien d’effort) mais aussi de
l’orientation (quels choix) du comportement.
Ainsi, la motivation provient d’une inférence sur
la raison d’un comportement. De fait, on ne peut
pas l’observer directement, on n’en observe que les
effets, ce qui soulève plusieurs problèmes pour l’ap-
proche expérimentale.
Le premier est celui de la circularité : s’agit-il
seulement d’une façon de parler ? Si je dis qu’un
patient en a agressé un autre en raison de ses
pulsions agressives, est-ce que je n’ai pas dit deux
fois la même chose ? Existe-t-il réellement une
chose qu’on puisse appeler motivation et dont on
puisse étudier les bases cérébrales ? Un deuxième
problème est celui du particularisme : tous les indi-
vidus ne se comportent pas de la même façon, tous
les comportements ne procèdent pas des mêmes
désirs. Peut-on parler de motivation dans un sens
général ? Il faut aussi mentionner le problème du
réductionnisme : peut-on trouver une correspon-
dance entre les causes inférées à un niveau psycho-
logique et les causes mécaniques étudiées au niveau
neuronal ? C’est le sujet qui désire ; y a-t-il un sens
à dire qu’une région cérébrale est responsable de
la motivation du comportement ? Enfin, troisième
problème : comment s’assurer que l’inférence est
correcte, c’est-à-dire que le mécanisme cérébral
mis en avant est bien responsable de l’effort ou des
choix engagés par l’individu ? La méthode expé-
rimentale consiste à manipuler les causes pour
reproduire les effets. Mais si la motivation est une
chose interne au sujet qui le pousse à agir, comment
la manipuler ?
Ayant mis ces difficultés en relief, nous allons dans un
premier temps tenter de comprendre comment les
neurosciences cognitives ont réussi à les contourner.
Ensuite, nous passerons en revue quelques para-
digmes permettant d’étudier les bases cérébrales
de la motivation et de ses troubles, en commençant
par les mécanismes les plus basiques pour aller vers
les plus sophistiqués.

La Lettre du Neurologue • Vol. XIII - n° 3 - mars 2009 | 71
Points forts
Motivation et neuroscience :
bref historique
Les sciences cognitives ont émergé au milieu du
siècle dernier. Avant cela, la plupart des scientifi-
ques se méfiaient des représentations mentales,
justement parce qu’elles n’étaient pas observables.
Le cerveau était considéré comme une boîte noire, et
les chercheurs se contentaient de décrire les entrées
et les sorties. L’étude du comportement animal
se résumait alors à la recherche de lois stimulus-
réponse, suivant le programme dit béhavioriste.
Un écueil majeur pour le béhavioriste est l’explo-
sion combinatoire : lorsque plusieurs manipulations
peuvent générer plusieurs comportements, le nombre
de liens possibles devient vite astronomique. Par
exemple, la privation d’eau, une température élevée
ou une nourriture salée peuvent toutes conduire un
animal à boire davantage d’eau, à travailler plus pour
une gorgée, ou à consentir d’absorber des boissons
amères. Plutôt que de tracer tous les liens possi-
bles, il paraît économique de relier les différentes
manipulations à la soif, puis la soif aux différents
comportements. La soif apparaît donc comme une
variable intermédiaire, une commodité de notation.
On peut considérer ces variables intermédiaires (par
exemple la soif, la faim, l’agressivité ou la libido), que
les Anglo-Saxons appellent drive, ce que nous tradui-
rons par “besoin”, comme les premiers concepts
opérationnels de motivation.
Il revient aux béhavioristes d’avoir découvert que
certains stimuli influencent le comportement parce
qu’ils interviennent en conséquence d’une action,
ce que E.L. Thorndike a appelé la loi de l’effet. On
dit que ces stimuli renforcent le comportement, et
on les qualifie de récompenses (1). Ainsi, dans la
fameuse cage de Skinner, on récompense le rat par
de la nourriture chaque fois qu’il appuie sur la bonne
pédale, ce qui se produira de plus en plus souvent
au fil du temps. La dynamique du renforcement est
bien décrite par la loi de Rescorla et Wagner, selon
laquelle la vitesse d’apprentissage est proportion-
nelle à l’erreur de prédiction de la récompense, soit la
récompense obtenue moins la récompense attendue.
Si l’on obtient plus de récompenses que prévu, le
comportement va être renforcé ; si l’on en obtient
moins, il sera au contraire affaibli.
Mais pourquoi les récompenses ont-elles cette capa-
cité de renforcer le comportement ? Parce qu’elles
viennent réduire le besoin. Et d’où vient le besoin ?
De la nécessité de maintenir certaines variables
internes à un niveau constant. Les récompenses font
alors partie intégrante d’un mécanisme de régulation
homéostatique, selon l’expression de W. Cannon. Ces
mécanismes fonctionnent sur le modèle du ther-
mostat, qu’on peut appliquer au comportement
alimentaire. Pour maintenir les réserves d’énergie
disponible, l’organisme dispose d’indicateurs, par
exemple le taux de glucose sanguin. On a donc des
capteurs qui vont signaler les écarts entre les valeurs
mesurées et les valeurs de références, un gramme par
litre dans le cas de la glycémie. Ces signaux d’erreur
vont ensuite déclencher des mécanismes compensa-
teurs, dont certains passent par le comportement,
par exemple, une hypoglycémie va pousser à la prise
alimentaire.
L’idée du besoin homéostatique est si élégante et
si intuitive que les recherches sur la motivation se
sont longtemps focalisées sur l’étude de points de
référence, de signaux d’erreur et de mécanismes
compensateurs. Cette théorie a pourtant été mise
à mal par de nombreuses observations, et elle a
progressivement été abandonnée (2). Il a d’abord
été objecté qu’une stabilité des variables internes
n’implique pas nécessairement l’existence d’une
régulation. Par exemple, un poids corporel stable ne
signifie pas qu’il existe un point de référence ni des
mécanismes régulateurs pour maintenir le poids au
niveau de référence. Il s’agit peut-être plutôt d’un
point d’équilibre entre systèmes antagonistes, les
uns favorisant l’amaigrissement et les autres la prise
de poids. Si l’obésité s’est répandue ces dernières
décennies aux États-Unis, ce n’est pas que le poids
de référence a changé, mais que la réclame a rendu
les aliments plus appétissants et disponibles. Ce
que l’on peut éprouver soi-même face à un bol de
cacahuètes salées : on n’en éprouvait pas le besoin
et pourtant on n’arrête pas d’en manger. Ainsi, la
prise alimentaire n’est pas forcément proportionnée
aux besoins, et les aspects hédoniques semblent
déterminants.
Ces remarques rejoignent d’autres observa-
tions montrant que les récompenses ne viennent
pas satisfaire un besoin mais donner du plaisir.
Mots-clés
Apathie
Apprentissage
Compulsion
Cortex préfrontal
Dopamine
Ganglions de la base
Modèle computationnel
Motivation
Neuropsychologie
Les neurosciences cognitives définissent la motivation comme un processus permettant aux récompenses
»
désirées d’activer et d’orienter le comportement.
Ces processus traitant des récompenses sont pris en charge par un système cérébral particulier, reliant cortex »
orbitofrontal et structures limbiques sous-corticales.
Le champ émergent de la neuro-économie propose de nouveaux paradigmes pour caractériser les troubles de
»
la motivation en termes de sensibilité à l’effort, à la récompense, à la punition, au risque, au délai, etc.
Ainsi, certaines formes d’apathies liées à une atteinte des ganglions de la base s’expliquent par une perte de »
sensibilité aux récompenses, et certains comportements compulsifs liés aux traitements dopaminergiques par un
gain de sensibilité aux récompenses.
Summary
Patients with neurological
conditions can exhibit disor-
ders where motivation is
either deficient (apathy) or
out of control (compulsion). At
first sight, it may seem uneasy
to tell whether the deficit
is primarily linked to brain
damage or secondary to motor
or cognitive disability. Cogni-
tive neuro science provides
conceptual and empirical tools
to explore the neural substrates
of motivational processes.
A large brain network, within
the prefrontal cortex and the
basal ganglia, has been impli-
cated in representing expected
rewards so as to energise and
direct be haviour. Damage
to this network results in
primary motivational disor-
ders, in which reward-seeking
behaviour specifically deviates
from normality. Depending on
the specific brain structure
impaired, motivational disor-
ders can thus be characterised
in terms of sensitivity to effort,
reward, punishment, risk or
delay.
Keywords
Apathy
Learning
Compulsion
Prefrontal cortex
Dopamine
Basal ganglia
Computational model
Motivation
Neuropsychology
Functional neuroimaging
Decision making
Reward

72 | La Lettre du Neurologue • Vol. XIII - n° 3 - mars 2009
Motivation et récompense :
le point de vue des neurosciences cognitives
MISE AU POINT
On cite souvent le cas d’un patient souffrant d’oc-
clusion œsophagienne, et nourri directement par
sonde gastrique. Ce patient insistait pour passer
les aliments en bouche avant de les placer dans son
estomac. De même, des chiens nourris par intra-
veineuse continuent à ingérer la nourriture dispo-
nible et, de ce fait, prennent du poids. Ou encore,
les rats peuvent fournir de gros efforts pour obtenir
une solution de saccharine, qui ne peut pas être
digérée et donc utilisée comme source d’énergie
pour l’organisme. Tous ces exemples montrent que
la prise alimentaire n’est pas seulement une question
de régulation homéostatique. Dans bien des cas, si
les animaux mangent, ce n’est pas pour refaire leur
stock d’énergie, c’est parce qu’ils aiment ça.
D’ailleurs, si la théorie du besoin homéostatique
peut s’appliquer à la prise alimentaire, on voit mal
comment la généraliser à des récompenses moins
primaires, telle que la reconnaissance sociale ou le
sentiment d’avoir agi selon sa morale. En outre, l’acti-
vation d’un lien stimulus-réponse appris par renfor-
cement paraît trop pauvre pour que l’on puisse parler
d’un comportement réellement motivé. L’intuition
veut qu’un comportement motivé s’accompagne
d’une certaine participation affective, sinon émotion-
nelle. Selon la distinction de K.C. Berridge (3), un
contexte associé à une récompense devient à la fois
apprécié sur le plan affectif (effet liking) et recherché
sur le plan comportemental (effet wanting). De plus,
le comportement doit être flexible : par exemple,
selon le contexte, le sujet doit pouvoir élaborer de
nouvelles stratégies pour obtenir sa récompense.
Enfin, et surtout, l’animal doit agir en vertu de la
récompense recherchée et non de façon automa-
tique. On peut le vérifier en variant la valeur de la
récompense, par exemple en amenant l’animal à
satiété : si, en présence du stimulus, il reproduit
la réponse, alors il s’agissait d’un comportement
automatique ; s’il ne le fait pas, il s’agissait d’un
comportement dirigé vers un but.
Ainsi, alors que dans les premières conceptions
scientifiques de la motivation tout partait des
besoins internes, dans les conceptions plus actuelles
tout commence avec l’expérience hédonique des
récompenses. La motivation reste en partie liée aux
nécessités de la survie, dans la mesure où la valeur
hédonique dépend des besoins, par exemple de la
faim pour la nourriture, et plus généralement de
l’état de notre appareil cognitif. Les récompenses
évaluées positivement par notre appareil cognitif
seront à la fois appréciées et désirées, de même
que les éléments du contexte qui leur sont asso-
ciés. Ainsi, par apprentissage associatif, la valeur
positive des récompenses se propage aux indices de
notre environnement qui les annoncent. Les indices
annonciateurs de récompense prennent alors une
valeur incitative : ils acquièrent le double pouvoir
d’orienter le comportement (vers l’alternative la
mieux récompensée) et d’augmenter son intensité
(lorsqu’il y a davantage de récompense en vue).
Cette théorie de la motivation peut être considérée
comme une réinterprétation cognitiviste des lois
béhavioristes. Elle offre beaucoup d’avantages pour
une approche expérimentale. Elle définit tout d’abord
ce qu’on doit chercher dans le cerveau : comment se
construit la représentation des buts (les récompenses
espérées), et comment ceux-ci peuvent activer et
orienter le comportement. Ensuite, elle indique
comment manipuler la motivation : en variant les
récompenses en jeu dans le contexte, on joue sur
leur représentation dans le cerveau. On dira que les
récompenses espérées sont les raisons du compor-
tement, et que leurs représentations cérébrales en
sont les causes. Enfin, elle fournit une hypothèse
de travail, selon laquelle toute situation associée à
une expérience hédonique positive prendra le statut
de récompense (sera appréciée et désirée), qu’elle
soit primaire comme un repas ou plus secondaire
comme des applaudissements.
Quelques troubles de la motivation
bien caractérisés
La théorie a été féconde, y compris chez l’homme.
En particulier, l’hypothèse dite de la monnaie neuro-
nale commune, selon laquelle différents types de
récompenses chez différents sujets sont représentés
par les mêmes régions cérébrales, a été largement
vérifiée (4-6). À tel point qu’on appelle système
de récompense les régions qui, chez la plupart des
individus, répondent aux récompenses et aux indices
qui les annoncent. Ces structures, qui donnent donc
une valeur aux éléments du contexte, comprennent
notamment le cortex orbitofrontal, le cortex cingu-
laire antérieur, l’amygdale et la partie ventrale des
ganglions de la base. Une même région (le striatum
ventral) peut représenter à la fois le plaisir de recevoir
une somme d’argent et celui de donner cette somme
à une œuvre de charité (7). L’argent est sans doute la
récompense la plus largement utilisée, d’abord pour
des raisons pratiques. Au-delà de l’universalité, il a
l’avantage de ne pas générer de satiété : les partici-
pants ont beau gagner de l’argent, ils continueront à
en empocher s’ils en ont l’occasion. Il offre aussi la
possibilité de quantifier dans une même métrique les
▶▶▶

AAN 2OO9
American Academy of Neurology
E-mail
Café
Téléphone
Cartes
postales
Magazines
Le Rendez-vous Français
Seattle, États-Unis
25 avril - 2 mai 2009
stand n° 839
Nous serons heureux
de vous recevoir sur notre stand
et de vous offrir les services suivants :
Partenaire
LN AAN annonce RVF 1 12/03/09 15:08:05
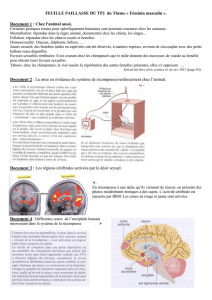
Figure 1. Caractérisation d’un cas d’apathie. Le patient présente un déficit d’auto activation
consécutif à une lésion bilatérale du pallidum (IRM anatomique en haut à droite). Dans le
test d’effort sur instruction (colonne de gauche), le patient doit serrer la pince de façon
à faire monter le curseur jusqu’à la ligne rouge, placée suivant les conditions à 40, 80 ou
120 % de sa force maximale. Les résultats montrent la force produite en moyenne au cours
d’un essai. On voit que le patient, tout comme le sujet témoin, est capable de moduler
sa force en fonction de l’instruction. Dans le test d’effort sur incitation, on met en jeu
différentes sommes d’argent : 1, 10 ou 50 euros selon les conditions. On laisse le patient
libre de serrer la pince comme il le souhaite, mais on lui fait comprendre que plus il serre
fort, plus il gagnera d’argent. On voit que le patient ne module pas sa force (colonne du
milieu), contrairement au sujet témoin qui appuie plus fort et plus longtemps lorsqu’on
augmente les récompenses en jeu. Enfin, on vérifie que le patient différencie bien les
enjeux sur le plan affectif en mesurant la réponse électrodermale (colonne de droite).
Il ne s’agit donc ni d’un trouble purement moteur (le patient module sa force sur consigne)
ni d’un trouble purement affectif (le patient réagit aux récompenses proposées). On peut
conclure que, chez ce patient, la représentation des récompenses en jeu n’active plus le
comportement.
La Lettre du Neurologue • Vol. XIII - n° 3 - mars 2009 | 75
MISE AU POINT
récompenses (gains monétaires) et leur contraire, les
punitions (pertes monétaires). Enfin l’utilisation de
l’argent a permis de croiser les paradigmes issus de
l’expérimentation animale avec les théories écono-
miques de la décision. Ces théories présument que
l’on choisit l’option qui maximise la valeur attendue,
une notion qui peut être identifiée au concept de
récompense espérée.
Le processus motivationnel le plus basique est sans
doute l’énergisation du comportement en proportion
de la récompense espérée. Nous avons imaginé pour
l’étudier un test très simple (8) : on présente au sujet
une certaine somme d’argent, et on lui demande
de serrer la pince d’un dynamomètre, sachant que
plus il serre fort, plus grande sera la fraction de la
somme en jeu qu’il pourra mettre dans sa poche. En
moyenne, les sujets témoins produisent plus de force
lorsqu’il y a davantage d’argent en jeu, et cet effet
s’accompagne en IRM fonctionnelle d’une activation
des régions ventrales des ganglions de la base. Nous
avons donc testé des patients présentant des lésions
bilatérales des ganglions de la base et, sur le plan
clinique, un déficit d’autoactivation. Ce déficit se
caractérise par une sévère réduction des compor-
tements spontanés, partiellement réversible via la
sollicitation d’un tiers (9). Les résultats montrent que
ces patients ne modulent pas leur force en fonction
de la récompense en jeu (figure 1). Pourtant, leur
réponse électrodermale, qui reflète les réactions
émotionnelles, est bien proportionnelle aux enjeux
monétaires. Tout se passe chez ces patients comme
si l’activation motrice (le wanting) était déconnectée
de l’évaluation affective (le liking). Chez les patients
déprimés, il n’y a pas de dissociation : la conductance
cutanée comme la force manuelle restent insensibles
aux récompenses proposées. Pour une même force
produite, ces patients ont l’impression de fournir
plus d’effort que les sujets témoins. Chez les sujets
sains, en effet, la sensation d’effort semble diminuée
par les récompenses promises : plus on est motivé,
moins on ressent l’effort.
Un second processus motivationnel concerne
l’orientation du comportement en fonction des
récompenses attendues. Au plus simple, il s’agit
de deux réponses motrices entre lesquelles le sujet
doit choisir. On peut associer les réponses à des
indices, dont le sujet doit apprendre la valeur par
essai et erreur, comme dans la cage de Skinner. Pour
que la tâche ne soit pas triviale, les associations entre
indices et récompenses sont en général probabi-
listes : certains indices font gagner (ou perdre) plus
souvent que d’autres. La loi de Rescorla et Wagner
est alors utile pour générer les valeurs théoriques
sur lesquelles est censée se fonder la décision des
sujets. L’IRM fonctionnelle a montré que ces valeurs
sont représentées essai après essai dans le striatum
ventral (10, 11). De plus, l’erreur de prédiction de
la récompense, qui selon cette loi guide l’appren-
tissage, est codée par les populations dopaminer-
giques du mésencéphale (12, 13). Il devenait donc
particulièrement intéressant d’étudier le compor-
tement des patients parkinsoniens dans ce type de
tâche. Il apparaît dans l’étude de M.J. Frank et al.,
que lorsqu’ils sont sans traitement, ces patients
apprennent mieux sous renforcement négatif (au
bâton) que sous renforcement positif (à la carotte),
alors qu’ils présentent les performances inverses
▶▶▶

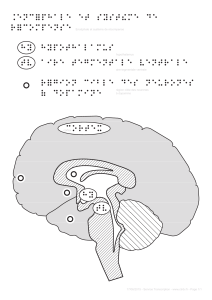
Figure 2. Le modèle acteur-critique. Le schéma représente une implémentation possible
d’un modèle computationnel permettant de rendre compte à la fois des données d’imagerie
et du comportement des sujets dans une tâche d’apprentissage instrumental. Il y a deux
systèmes d’apprentissage, l’un fondé sur le critique et l’autre sur l’acteur, qui vont extraire
différentes dimensions du contexte, représenté dans le cortex. Le critique, représenté par
le striatum ventral, prédit la quantité de récompense qu’on peut attendre dans le contexte.
L’acteur, représenté par le putamen, va sélectionner l’action pour laquelle la prédiction est
maximale, via les sorties des ganglions de la base (globus pallidus interne et substance noire
réticulée). Lorsque le résultat de l’action est connu, les neurones dopaminergiques de la
substance noire compacte et de l’aire tegmentale ventrale vont calculer la différence entre
la récompense prédite par le critique et la récompense réellement obtenue. Ils renvoient
cette différence, c’est-à-dire l’erreur de prédiction de la récompense (δ), vers le critique
pour qu’il améliore sa prédiction, et vers l’acteur pour qu’il améliore sa sélection. Sur le
plan mathématique, les valeurs du contexte et de l’action sont mises à jour en proportion
de l’erreur de prédiction, selon la loi de Rescorla et Wagner. Sur le plan neuronal, il s’agit
de modifier le poids des synapses cortico-striatales, pour faciliter un choix optimal si le
même contexte se représente. Dans un environnement stable (dont les contingences ne
changent pas), le système nigro-striatal va ainsi optimiser ses prédictions et ses choix
jusqu’à ce que l’erreur devienne nulle.
76 | La Lettre du Neurologue • Vol. XIII - n° 3 - mars 2009
Motivation et récompense :
le point de vue des neurosciences cognitives
MISE AU POINT
lorsqu’ils sont traités par L-dopa (14). Pour expli-
quer ce résultat, M.J. Frank et al. ont proposé une
variante du modèle acteur-critique représenté sur
la figure 2, qui implémente la loi de Rescorla et
Wagner au sein des circuits striato-frontaux. Selon
ce modèle, la décharge de dopamine (lorsqu’il y a
plus de récompense que prévu) renforce les circuits
d’approche, tandis que la dépression en dopamine
(lorsqu’il y a moins de récompense que prévu)
renforce les circuits d’évitement. Il est possible que
ce modèle explique les comportements compulsifs,
notamment le jeu pathologique, observés chez les
patients sous agonistes dopaminergiques. L’idée
serait que le médicament crée un déséquilibre, de
sorte que les récompenses renforcent davantage le
comportement que les punitions ne l’affaiblissent.
Ainsi, les paradigmes d’incitation à l’effort ou
au choix simple mobilisent principalement les
ganglions de la base (striatum ventral, pallidum
ventral et dopamine). C’est encore le cas lorsque
l’on masque les indices annonçant les récompenses,
de façon que leur perception reste subconsciente
(15, 16). Les sujets peuvent alors être amenés,
même lorsqu’ils ne perçoivent pas consciemment
les enjeux, à produire plus d’effort pour plus de
récompense (motivation subliminale), ou à choisir
l’option la mieux récompensée (apprentissage
subliminal). Ces paradigmes subliminaux permet-
tent de tester l’intégrité de processus motiva-
tionnels basiques sans brouiller les résultats par
l’intervention de rationalisations conscientes qui
peuvent être altérées chez le patient. On a ainsi
pu mettre en évidence dans la maladie de Gilles
de la Tourette une double dissociation, en miroir
de celle observée dans la maladie de Parkinson,
avec un meilleur apprentissage par renforcement
positif lorsque les patients ne sont pas traités, et
par renforcement négatif lorsqu’ils sont traités par
des neuroleptiques.
Dans une certaine mesure, les atteintes des territoires
corticaux (orbitofrontal et cingulaire antérieur), qui
forment avec les régions ventrales des ganglions de
la base des circuits fonctionnels, affectent égale-
ment les fonctions motivationnelles rudimentaires.
Mais ces territoires semblent intervenir plus spéci-
fiquement lorsqu’il faut apprendre ou inverser des
règles associatives plus complexes, et lorsque
les récompenses sont différées dans le temps.
A.R. Damasio a appelé “myopie du futur” la forme
d’impulsivité qui consiste à rechercher les récom-
penses à court terme au détriment des conséquences
négatives à long terme. Elle s’observe notamment
en cas de lésions du cortex préfrontal ventromédian,
qui empêcheraient les patients d’évoquer par antici-
pation les marqueurs somatiques associés aux consé-
quences de leurs choix (17, 18). Mais la gambling task
utilisée pour la démonstration confond en fait de
nombreux phénomènes tels que l’apprentissage par
renforcement, l’extraction de règle, la recherche
 6
6
1
/
6
100%