Les cytokines en thérapeutique anti-infectieuse

La Lettre de l’Infectiologue - Tome XV - n° 9 - novembre 2000
393
MISE AU POINT
a meilleure connaissance de la physiopathologie des
infections (choc septique, infections à germes intra-
cellulaires, infection à VIH…) ainsi que la limite de
nos thérapeutiques anti-infectieuses actuelles amènent à recher-
cher d’autres stratégies de traitement, orientées vers la réponse
immune aux infections.
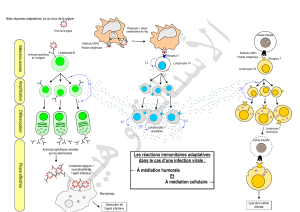
La réponse de notre système immunitaire à tout processus infec-
tieux est, de ce fait, essentielle à connaître. Dans la majorité des
cas, l’hôte répond par une activation salutaire de son système
immunitaire, ce qui permet l’éradication du germe, avec ou sans
thérapeutique anti-infectieuse spécifique (antibiotiques, antivi-
raux, antifongiques et antiparasitaires). Parfois, le micro-orga-
nisme va persister dans l’organisme comme dans le cas des infec-
tions à germes intracellulaires (infection à mycobactéries,
aspergillose…), ce qui nécessitera l’intervention d’un traitement
spécifique long et dont l’efficacité dépendra de la qualité de la
réponse immune sous-jacente ; d’où le premier concept d’aug-
menter la réponse immune. Enfin, l’infection peut entraîner une
réponse immune délétère, engageant, à elle seule, le pronostic
vital du patient. C’est le cas du choc septique ou du neuro-
paludisme, où la symptomatologie est liée aux effets directs
des cytokines qui sont sécrétées en réponse à la stimulation
antigénique du micro-organisme. Dans cette situation, il est
possible, du moins en théorie, d’intervenir sur la modulation
de la réponse immune, en stimulant ou à l’inverse en inhibant
l’action de certaines cytokines.
CYTOKINES : GÉNÉRALITÉS ET CONCEPT D’UTILISATION
Les cytokines sont des petites protéines (8-80 kDa) qui inter-
viennent comme médiateurs solubles de la communication inter-
cellulaire. Les anciens termes lymphokines ou monokines reflé-
taient l’origine respectivement lymphocytaire ou monocytaire
de ces protéines, mais l’immense diversité des cellules à l’ori-
gine de la production de ces protéines immuno-actives a fait
généraliser ce terme sous le nom de cytokines. Les cytokines
envoient des signaux de communication entre les cellules du
système immunitaire, et interviennent ainsi dans la régulation
de la réponse immune en déterminant l’intensité de la réponse
et en orientant celle-ci selon le facteur déclenchant (selon le
germe). Elles ont une action de proximité, autocrine et para-
crine, et agissent en réseau avec un système de régulation très
complexe (récepteurs, antagonistes des récepteurs, récepteurs
Les cytokines en thérapeutique anti-infectieuse
!
C. Amiel*
RÉSUMÉ.
Les cytokines sont des petites glycoprotéines utilisées dans la communication intercellulaire, qui agissent en réseau et présentent de
nombreuses interactions. Elles participent à l’équilibre de deux grands systèmes de l’immunité : cytokines pro-inflammatoires et anti-inflam-
matoires, ou cytokines de type Th1 et de type Th2. L’utilisation des cytokines en pathologie infectieuse pourrait répondre à deux objectifs :
–réduire la réponse inflammatoire à l’infection (choc septique, neuropaludisme) en modulant la balance inflammatoires/anti-inflammatoires ;
–augmenter la réponse immune à l’infection, soit directement en orientant vers une réponse en cytokines de type Th1 et vers une activation
des cellules cytotoxiques, soit indirectement en augmentant le nombre de cellules immunocompétentes (interleukine 2, facteurs de croissance
hématopoïétiques [FCH]).
Les principales cytokines actuellement utilisées en pathologie infectieuse sont représentées par les FCH lors des neutropénies (G-CSF, GM-
CSF), l’interféron αdans le cadre des hépatites chroniques B et C et l’IL2 dans la pathologie VIH. Les FCH augmentent la prolifération, l’ac-
tivation et la capacité fonctionnelle des cellules phagocytaires (macrophages, polynucléaires), ce qui pourrait faire élargir leurs indications
en thérapeutique. L’érythropoïétine est rarement utilisée dans les anémies liées au VIH, et son efficacité est essentiellement rattachée à un taux
d’érythropoïétine bas (anémie réfractaire). L’IL2 présente une efficacité et une toxicité dose-dépendantes ; elle est actuellement utilisée chez
les patients VIH+ en cas de lymphopénie CD4 malgré un traitement antirétroviral combiné bien conduit. D’autres cytokines comme l’IL12
sont intéressantes. L’IL12 stimule la réponse innée et la réponse cellulaire spécifique de type Th1 et représenterait un excellent adjuvant de
vaccination, mais sa toxicité limite actuellement son utilisation en thérapeutique. Des chimiokines ou analogues sont également à l’étude dans
l’infection à VIH. De nombreuses études cliniques doivent être mises en place afin d’utiliser ces cytokines de façon optimale, que ce soit en
termes de schéma posologique ou d’indication thérapeutique.
Mots-clés :
Cytokine - Infection - Immunothérapie - IL2.
*Service du Pr W. Rozenbaum, hôpital Rothschild, 75571 Paris Cedex.
L

solubles, cytokines antagonistes). Elles peuvent avoir entre elles
des effets synergiques, additifs, indifférents ou antagonistes,
avec de nombreux rétrocontrôles positifs ou négatifs. Les études
faites in vitro isolent les cytokines de leur contexte, et l’inter-
prétation des résultats reste donc très délicate.
On peut distinguer les cytokines en cinq groupes : les interfé-
rons (IFN) α,βet γ; les interleukines (IL) [18 sont actuelle-
ment connues] ; les facteurs de croissance hématopoïétiques
(CSF : G, M, GM-CSF, érythropoïétine), les chimiokines
(RANTES, MIP1 αet β,IL16), et les autres (TNF, TGF…).
Les cytokines sont utilisées de façon indirecte depuis longtemps,
la première génération d’immunomodulateurs étant représentée
par les glucocorticoïdes qui diminuent la synthèse de cytokines
pro-inflammatoires, augmentent les cytokines anti-inflamma-
toires et diminuent l’immunité à médiation cellulaire
(IL2, IFNγ). La thalidomide et la pentoxyfilline ont
également été utilisées pour leur activité anti-TNF. Actuelle-
ment, la plus grande utilisation des cytokines en infectiologie
concerne l’IFNαdans le traitement des hépatites virales B et C.
L’utilisation des cytokines en thérapeutique repose sur deux
concepts :
!Réduire la réponse inflammatoire à l’infection (choc sep-
tique, neuropaludisme) en modulant la balance molécules pro-
inflammatoires/molécules anti-inflammatoires : diminution de
l’expression des cytokines inflammatoires, augmentation de
l’expression des molécules anti-inflammatoires par des anta-
gonistes des cytokines inflammatoires ou de leurs récepteurs.
!Augmenter la réponse immune à l’infection, soit directement
en orientant vers une réponse en cytokines de type Th1 (en par-
ticulier lors des infections à germe intracellulaire) et vers une
activation des cellules cytotoxiques (IFN, IL12…), soit indi-
rectement en augmentant le nombre de cellules immunocom-
pétentes (IL2 et lymphocytes ; CSF et polynucléaires neutro-
philes et/ou macrophages…).
Les principales cytokines actuellement utilisées en pathologie
infectieuse sont représentées par les CSF lors des neutropénies
(G-CSF, GM-CSF), l’IL2 en cas de lymphopénie CD4 lors de
l’infection par le VIH , et l’IFNαdans le cadre des hépatites
chroniques B et C. D’autres cytokines comme l’IL12 sont inté-
ressantes, mais leur toxicité limite actuellement leur utilisation
en thérapeutique (tableau I).
LES GRANDS ÉQUILIBRES DANS LA RÉPONSE IMMUNE
Pour les interventions thérapeutiques au niveau du système
immunitaire, il faut tenir compte des grands équilibres qui
existent au sein du réseau des cytokines et qui sont souvent
perturbés lors des infections.
Équilibre cytokines pro-inflammatoires/cytokines
anti-inflammatoires
Les cytokines pro-inflammatoires sont essentiellement repré-
sentées par l’IL1, le TNFα,l’IL6, l’IFNγet l’IL12. Elles sont
principalement sécrétées par les macrophages et sont à l’ori-
gine de la fièvre, de la synthèse de prostaglandines et de pro-
téines de l’inflammation, mais présentent aussi, à l’inverse, de
394
La Lettre de l’Infectiologue - Tome XV - n° 9 - novembre 2000
MISE AU POINT
Cytokine IFNααIFNββIFNγγG-CSF GM-CSF Érythropoïétine IL2
Nom commercial Roféron®AAvonex®Imukin®Neupogen®Leucomax®Eprex®Proleukin®
(IFNα-2a) (IFNβ-1a) (IFNγ-1b) (RmetHuG-CSF) (GM-CSF) NéoRecormon Macrolin
Introna®Rebif®Granocyte
(IFNα-2b) (IFNβ-1a) (RHuG-CSF)
Viraféron Betaféron®
(IFNα-2b) (IFNβ-1b)
Laroféron
(IFNα-2a)
Indications Roféron®ARéduire Réduire Réduire Réduire "Anémie Proleukin®:
et Introna : la progression la fréquence la durée la durée d’origine "adénocarcinome
"hépatite B du handicap des infections et les compli- et les compli- rénale rénal métastasé
"hépatite C et la fréquence graves cations cations "Anémie
"Kaposi des rechutes chez des neutropénies : des neutropénies : de chimiothérapie Macrolin :
"leucémie aiguë et des poussées les patients "chimiothérapies "chimiothérapies contenant "en ATU : patient
myéloblastique de sclérose atteints de cytotoxiques cytotoxiques cisplatine VIH+
" leucémie en plaques granulomatose "auto/allogreffes et myélosuppressives "Production ayant moins de
à tricholeucocytes septique "mobilisation "neutropénie de sang 200 lymphocytes
"lymphome cellules souches induite autologue CD4/mm3
folliculaire "neutropénies par le ganciclovir "Anémie
"myélome chroniques : lors des rétinites du prématuré
"tumeur Neupogen®à CMV
carcinoïde
Viraféron :
"hépatite B et C
Laroféron :
"hépatite C
Tableau I. Cytokines ayant reçu une autorisation de mise sur le marché et leurs indications.

multiples effets bénéfiques comme par exemple l’IFNγqui a
une action antivirale, antitumorale et immunomodulatrice.
Les cytokines anti-inflammatoires sont l’IL4, l’IL10, l’IL13 (et
le G-CSF) ; d’autres molécules anti-inflammatoires intervien-
nent également comme le récepteur soluble du TNF (sTNFR)
et l’antagoniste du récepteur de l’IL1 (IL1Ra).
Réduire la réponse inflammatoire à un processus infectieux ne
doit être envisagé que lorsqu’elle présente un caractère mor-
bide, voire mortel. Ainsi, la réduction de l’inflammation se jus-
tifie lors du neuropaludisme, ou du choc septique. À l’inverse,
inhiber toute réponse inflammatoire comme, par exemple, inhi-
ber la réponse en TNFαpourrait devenir très délétère chez
l’homme. Ainsi, on sait que l’inhibition du TNFαsécrété par
les macrophages lors d’infections à mycobactéries atypiques
empêche l’apoptose de ces macrophages infectés, et donc favo-
rise la pullulation microbienne (1).
Équilibre cytokines de type Th1/cytokines de type Th2 (2)
"Les cytokines de type 1 (Th1) sont l’IL2, l’IFNγ,l’IL12
et le TNFα.Elles favorisent l’immunité à médiation cellulaire
et stimulent les CTL et macrophages. La réponse de type 1,
induite par certaines bactéries (mycobactéries, endotoxines)
et par les virus, peut être délétère (la majorité des cytokines
de type 1 sont des molécules inflammatoires) ; la réponse
de type 1 serait en particulier impliquée dans l’ulcère lié à
Helicobacter pylori, dans la maladie de Crohn, dans certaines
maladies auto-immunes et dans des avortements à répétition.
"Les cytokines de type 2 sont l’IL4, IL5, IL6, IL10, IL13.
Elles orientent vers une réponse immune à médiation humo-
rale, favorisent la synthèse d’anticorps (dont les IgE) et acti-
vent les polynucléaires éosinophiles. Cette réponse est induite
par certaines helminthiases (en particulier les nématodes gas-
tro-intestinaux), et pourrait être responsable d’atopie, de fibrose
pulmonaire idiopathique, de sclérose en plaques…
L’orientation d’un micro-organisme vers une réponse de type 1 ou
2 modifie la réponse à l’infection. Ainsi, dans la lèpre tuberculoïde,
la réponse est de type 1, avec des granulomes florides et peu de
micro-organismes ; dans la lèpre lépromateuse où la réponse est
de type 2, les granulomes inflammatoires sont rares mais les micro-
organismes pullulent (3). D’une manière générale, les infections
à mycobactéries (tuberculose ou autres) doivent faire intervenir
l’immunité de type 1 pour obtenir une éradication du germe. Cette
réponse immune est difficilement obtenue, en particulier chez les
patients immunodéprimés, c’est pourquoi certains auteurs préco-
nisent une “cytokinothérapie” pouvant faire intervenir l’IL2,
l’IL12, l’IFNγou le GM-CSF (4).
CHOC SEPTIQUE
Les cytokines ont été largement utilisées dans le choc septique,
dont la physiopathologie est partiellement connue : les lipopo-
lysaccharides (LPS) de la paroi des bacilles à Gram négatif
déclenchent la sécrétion par les monocytes et macrophages
d’IL1, de TNFα,d’IL6 et d’IL8, responsables du choc sep-
tique ; les bactéries à Gram positif, par le biais de certaines
toxines (exotoxine B du streptocoque…), activent la réponse
lymphocytaire T et augmentent la sécrétion d’IFNγqui peut
également être délétère.
Une vingtaine d’essais cliniques de phase II/III ont été effec-
tués avec l’IL1Ra, le sTNF-R, des anticorps anti-TNF, anti-pla-
telet activating factor (PAF) ou anti-prostaglandines (ibupro-
fène), ou de la méthylprednisolone (5-8). Les résultats,
globalement négatifs (pas d’amélioration de la survie des
patients), peuvent s’expliquer par la méconnaissance de
la physiopathologie du choc septique, l’utilisation d’une seule
cible évoluant dans un réseau de cytokines, un volume de dis-
tribution très réduit, un schéma thérapeutique inadéquat dans
le temps, un polymorphisme génétique avec variabilité inter-
individuelle des réponses aux pathogènes et au traitement.
INTERFÉRONS
Les interférons sont des cytokines immunomodulatrices, anti-
tumorales et antivirales. L’IFNγ,en particulier, augmente l’ex-
pression des molécules HLA de classe I et II et la fonction des
lymphocytes T cytotoxiques (CTL), des cellules natural killer
(NK), des polynucléaires neutrophiles (PNN) et des macro-
phages. De nombreux modèles animaux ont démontré l’intérêt
de l’IFNγ,par son action sur le système phagocytaire, dans les
infections à germes intracellulaires (leishmanioses dissémi-
nées ; lèpre lépromateuse ; infection à Mycobacterium avium)
(9). Chez l’homme, les résultats restent décevants, l’immuno-
thérapie par IFNγentraînant une restauration immune insuffi-
sante. Son intérêt a néanmoins été prouvé dans les infections
associées à la granulomatose septique (aspergillose, mycobac-
téries, entérobactéries) et a conduit à une autorisation de mise
sur le marché (4, 9).
L’IFNαest utilisé dans le traitement de l’hépatite virale chro-
nique B et C (10-12). Pour l’hépatite B, l’IFNαest utilisé
selon des critères bien précis, à la posologie de 5 à 10 MU/j
trois fois par semaine pendant plus de six mois. Le taux de
réponse définie par la séroconversion Ag Hbe-Ac anti-HBe
est de 40 %. L’IFNαpeut être associé à des analogues nucléo-
sidiques, en particulier la lamivudine, mais aussi au famci-
clovir (11). Les facteurs prédictifs d’une bonne réponse sont :
l’infection récente, l’origine caucasienne, la contamination
hétérosexuelle, la forte élévation des transaminases, l’im-
portance des lésions histologiques, le faible taux d’ADN cir-
culant, l’absence de co-infection VIH et les virus des hépa-
tites C et D. Pour l’hépatite C, le traitement associe
généralement la ribavirine à l’IFNα; la posologie d’IFN est
de 3 MU/j pendant 6 à 12 mois, ce qui peut induire une
réponse virologique soutenue de l’ordre de 30-40 % (12). Les
facteurs prédictifs d’une bonne réponse sont : le jeune âge,
le sexe féminin, l’infection récente, le score d’activité histo-
logique faible, l’absence de cirrhose, la normalité des γGT,
le génotype viral (génotype 1b non sensible à l’IFN), le faible
taux d’ARN circulant. Enfin, de nouveaux essais apparais-
sent avec le GM-CSF (13).
La Lettre de l’Infectiologue - Tome XV - n° 9 - novembre 2000
395
MISE AU POINT

INTERLEUKINE 2
L’IL2 stimule l'activation et la prolifération des cellules CD4
et CD8, l’activité des CTL et la production d’IFN. La première
utilisation de l’IL2 en thérapeutique humaine remonte à 1983.
Il s’agissait alors d’une préparation purifiée contenant de l’IL2
obtenue à partir de surnageant de leucocytes stimulés par la
PHA, utilisé chez deux patients atteints de mélanome (14). Dès
1985, l’IL2 est proposée dans l’infection à VIH, en particulier
pour les patients présentant une maladie de Kaposi (15).
Depuis, l’IL2 a fait l’objet de différents essais thérapeutiques,
dont le but était d’augmenter le taux de lymphocytes CD4.
Toutes ces études cliniques concernaient des patients présen-
tant un statut immunitaire et thérapeutique varié et traités avec
des schémas posologiques d’IL2 différents (tableau II)
(16-26). Ainsi, ni le schéma posologique ni les indications ne
peuvent être définis de façon optimale. Néanmoins, ces études
permettent de préciser plusieurs points :
"la réponse à l’IL2 est meilleure si le taux de lymphocytes
CD4 est élevé ;
"il existe une toxicité dose-dépendante ;
"les schémas thérapeutiques retenus sont des cures de 5 jours,
par voie sous-cutanée, espacées de 4 à 8 semaines, avec des
doses journalières allant de 3 à 15 MU/j.
En France, les différents essais utilisent une IL2 recombinante
à la posologie de 2 x 4,5 MU/j par voie sous- cutanée, toutes
les 6 à 8 semaines.
La toxicité dose-dépendante de l’IL2 se traduit par des effets
secondaires fréquents, principalement représentés par un
syndrome pseudogrippal avec fièvre (presque constante),
céphalées, myalgies, arthralgies, voire un syndrome de fuite
capillaire avec hypotension, rétention d’eau, troubles cardio-
vasculaires, un rash, des désordres thyroïdiens, une polyarthrite
rhumatoïde, une néphrite interstitielle...
Cette toxicité a été confirmée, en particulier par Davey et al.,
qui rapportent 59 % de toxicité de grade III [malaise/fatigue :
32 % ; myalgies : 21 % ; arthralgies : 12 % ; trouble du som-
meil : 11 %] (25), avec cinq fois plus d’épisodes de fatigue et
de malaise dans le groupe à 15 MU/j par rapport au groupe à
3MU/j. Le principal effet secondaire est le syndrome pseudo-
grippal, avec fréquemment une toxicité de grade III ou IV pour
la fièvre. Ainsi, l’utilisation systématique d’antipyrétiques
(paracétamol) est préconisée.
L’efficacité de l’IL2 dans l’augmentation quantitative du
nombre de lymphocytes CD4 est connue, mais la capacité fonc-
tionnelle de ces cellules est de connaissance plus réduite.
L’équipe italienne de de Paoli a montré pour la première fois
que les cellules de patients traités par IL2 présentaient in vitro
une capacité accrue de sécrétion d’IL2, d’IFNγet d’IL4 (17).
Depuis, les résultats restent contradictoires, en particulier sur
la capacité endogène de production d’IL2 chez les patients trai-
tés, et sur l’efficacité réelle de l’IL2 en termes d’élévation du
nombre de lymphocytes CD4 chez les patients mis sous traite-
ment antirétroviral combiné hautement actif (HAART) (23, 24).
Imani, dans une étude portant seulement sur trois patients très
immunodéprimés, soulève néanmoins quelques points intéres-
sants : l’IL2 augmente plus l’activité et le nombre des cellules
NK que celui des lymphocytes CD4 ; elle augmente l’activa-
tion cellulaire (augmentation d’expression de CD38 et de CD95
[Fas]), d’où le risque, du moins théorique, d’apoptose ; elle
pourrait réverser le profil de sécrétion de cytokine des patients
d’un type 2 vers un type 1 (diminution de l’IL4 en réponse
aux antigènes, et augmentation de l’IFNγspécifique ou non du
VIH). Enfin, il existe un intérêt potentiel de la “bithérapie”
GM-CSF + IL2 avec apparition d’une réponse proliférative
spécifique ou non du VIH (non objectivée sous IL2 seule) et
augmentation de la production endogène d’IL2 (24).
En France, l’IL2 a fait l’objet de deux essais soutenus par
l’Agence nationale de recherche sur le sida (ANRS) :
"L’ANRS 048 concernait des patients mis sous zidovudine
et didanosine, ayant un taux de lymphocytes CD4 situé entre
250 et 500/mm3et traités par IL2 par voie intraveineuse, sous-
cutanée (2 x 4,5 MU-5 j/8 sem. pendant 48 semaines) ou par
PEG-IL2 : l’IL2 par voie sous-cutanée a permis d’obtenir un
gain de 564 CD4 à un an et une augmentation de plus de 80 %
des CD4 à un an chez 77 % de ces patients (26). L’augmenta-
tion du nombre de lymphocytes CD4 sous IL2 concerne non
seulement les cellules mémoires, mais aussi les cellules naïves
associées à un élargissement du répertoire de reconnaissance
des antigènes.
"L’ANRS 082 concernait des patients sous trithérapie conte-
nant un inhibiteur de protéase depuis plus de 6 mois, et ayant
un taux de lymphocytes CD4 inférieur à 200/mm3(IL2 à
2x4,5 MU-5 j/6 sem.- 4 cycles) : l’IL2 par voie sous-cutanée
a permis d’obtenir un gain modéré mais significatif de 65 CD4
à 6 mois (contre 18 CD4 sans IL2) ; 41 % des patients sous IL2
contre 3 % ont un gain de plus de 80 cellules. L’étude fonc-
tionnelle des lymphocytes CD4 dans l’essai ANRS 082 est en
cours.
Ces résultats sont à l’origine de l’autorisation temporaire d’uti-
lisation de l’IL2 chez les patients ayant moins de 200 CD4/mm3.
Elle est essentiellement proposée aux patients sous HAART,
avec réponse virologique mais échec immunologique.
Aucune de ces études ne permet de savoir s’il existe un béné-
fice clinique à l’utilisation de l’IL2. Deux essais à venir per-
mettront de répondre à cette question (ESPRIT : CD4 > 300
et SILCAT : CD4 < 300), pour lesquels ni la charge virale
plasmatique ni les traitements antirétroviraux n’entrent dans
les critères de sélection.
INTERLEUKINE 12
L’IL12 est un hétérodimère, produit principalement par les cel-
lules présentatrices d’antigènes (macrophages, cellules den-
dritiques, cellules de Langerhans). Elle stimule la réponse innée
396
La Lettre de l’Infectiologue - Tome XV - n° 9 - novembre 2000
MISE AU POINT
.../...

La Lettre de l’Infectiologue - Tome XV - n° 9 - novembre 2000
397
MISE AU POINT
Tableau II. Résumé de différents essais cliniques utilisant l’IL2 chez les patients VIH+.
Auteur (année) Nombre de patients et posologie IL2 ARV CD4 Résultats CD4
Kovacs n = 29 : ARV seul ARV > 200 Gain moyen : + 69 CD4/mois contre -4,8 (gain aussi en %)
(1995 et 1996) n = 31 : ARV + IL2 i.v. : 18 MU/j-5 j stratification : corrélation avec CD4 de base
6 cycles/2 mois < strate > 500
strate < 500
De Paoli n = 6 : ARV seul AZT/ddI en même temps 200-500 n = 6 : AZT/ddI : J0 CD4 = 320 S24 = 392
(1997) n = 10 : ARV + IL2 n = 10 : ARV + IL2 : J0 CD4 = 331 S24 = 650
6MU/j : J1-J5 et J8-J12 ; 6 cycles/28 j #production IFNγ,IL2 et IL4 in vitro
Simonelli n = 12 AZT/ddI 200-500 moyenne CD4 344 (± 81),
(1998) 6 MU/j : J1-J5 et J8-J12 ; charge virale = 34 800 (± 47 600) ;
6 cycles/28 j #CD4 (2 à 5 x CD4 dès début injections ; #CD4/CD25
#CD45RO/RA ; $ charge virale plasma et ADN proviral
3 grade III (hématotox.) ; 0 grade IV ; surtout fièvre...
et réaction locale
Arno n = 25 ARV non modifié < 250 #CD4 = + 105 versus + 30 (groupe contrôle)
(1999) 1 x 3 MU/j-24 sem. Charge virale < 500 copies/ml #CD4 mémoires puis CD4 naïfs (> contrôles)
Bartlett 1 : n = 5 à 1 MU/j-5 j/sem.-4 sem. de suite AZT 5 x 200 seul 8 sem. > 400 1 : CD4 S (0-8) = 711 ; S (9-12) = 1 235 ; S (13-20) = 778
(1998) 2 : n = 5 à 3 MU/j-5 j/sem.-4 sem. de suite puis + IL2 S9-S12 2 : CD4 S (0-8) = 828 ; S (9-12) = 1 567 ; S (13-20) = 990
HLADR id ; #CD38 et LPA ; 15 AE grade III/IV
Khatri n = 8 sida pas variation CD4 ; $ expression gène IL10
(1998) 1,2 MU/m2/j (2 M/j)-90 j de suite #expression endogène gène IFNγ(NK/CD8) et Il12
Hengge 1 : 9 MU/j-5 j ;1 cycle/6 sem.-52 sem. (n = 21) AZT/3TC/SQV 3 mois 200-500 Nombre Groupe 1 Groupe 2 Groupe 3
(1998) 2 : IL2 si CD4 $ < 1,25 x valeur base (n = 19) (avant = AZT + 3TC) de cycles médian 85–
3 : HAART seul (n = 18) CD4 J0 363 358 369
répondeurs = > 20 % #CD4 S52 485 (+ 34 %) 462 (+ 29 %) 375 (+ 7 %)
répondeurs partiels = entre 0 et 20 % #57 % ont un gain maximal en CD4 après le 1er cycle (médiane 767 CD4)
non-répondeurs = $
Zanussi n = 10 Naïfs ou 2 RTI > 200 à S24 : même #CD4 avec ou sans IL2 (350 à 550 CD4)
(1999) 6 MU/j : J1-J5 et J8-J12 ; 6 cycles/28 j Charge virale > 500 (moyenne 350) pas # endogène d’IL2, mais #IL4, IL13 et IFNγet $ MCP1
(moyenne 50 000 copies/ml)
mis sous HAART ± IL2
Imani n = 3, dont 1 avec MAC HAART CD4 < 100 #activité et nombre NK ; faible #CD4 (56 %63)
(1999) IL2 : 2 x 5 MU-5 j/6 sem.-3 cycles $ IL4 en réponse aux Ag, #IFNγspécifique ou non VIH (Elispot)
+ GM-CSF 3ecycle (60 000 U/kg/j) #CD38, #CD95 (Fas)
sous GM-CSF : #réponse proliférative et #production IL2
Davey n = 49 ; 4 schémas posologiques : ARV > 6 sem. > 500 #nombre de CD4/mois #% CD4/mois #% CD4 à M6
(1999) 1 : 2 x 1,5 MU/j-5 j/4 sem. 1 : + 30 + 1,7 % + 19 %
2 : 2 x 1,5 MU/j-5 j/8 sem. 2 : + 24 + 0,9 % + 19 %
3 : 2 x 7,5 MU/j-5 j/4 sem. 3 : + 146 + 3,4 % + 95 %
4 : 2 x 7,5 MU/j-5 j/8 sem. 4 : + 86 + 2,1 % + 44 %
3 cycles minimum ; 12 mois maximum 59 % patients toxicité grade III &73 événements ;
liés à la dose (5 fois moins de fatigue/malaise à 3 MU)
Levy 1 : AZT/ddI (n = 26) Mis sous AZT/ddI 250-550 #nombre de CD4 à S56, #80 % CD4 à S56, $ charge virale
(1999) 2 : AZT/ddI + IL2 en intraveineuse ± IL2 1 : +55 + 9 %- 1,37
(12 MU/j) (n = 22)
3 : AZT/ddI + IL2 en sous-cutanée 5 j 2 : + 676 + 68 % - 0,88
(2 x 3 MU/j) (n = 24)
4 : AZT/ddI + PEG-IL2 3 : + 564 + 77 % - 1,20
(2 M/m2bolus en intraveineuse)
Tous les 2 mois de S2 à S50 4 : + 105 – - 1,29
$ CD38, #CD45RA+, #réponse Ag de rappel (S56) pour groupes 2 et 3
ARV : antirétroviraux ;
#
: augmentation (entre 0 et 20 % d’augmentation des CD4).
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
1
/
13
100%