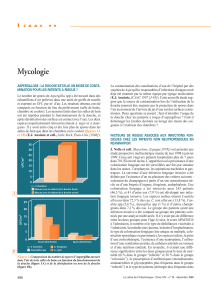
Triple infection fongique chez un patient avec cirrhose hépatique

doi:10.1684/abc.2011.0654
89
Pour citer cet article : Alidjinou K, Mathieu D, Colombel JF, Franc¸ois N, Poulain D, Sendid B. Triple infection fongique chez un patient avec cirrhose hépatique. Ann Biol
Clin 2012 ; 70(1) : 89-92 doi:10.1684/abc.2011.0654
Biologie au quotidien
Ann Biol Clin 2012 ; 70 (1) : 89-92
Triple infection fongique chez un patient
avec cirrhose hépatique
Triple fungal infection in a patient with liver cirrhosis
Kazali Alidjinou1
Daniel Mathieu2
Jean Frédéric Colombel3
Nadine Franc¸ois1
Daniel Poulain1
Boualem Sendid1
1Laboratoire
de parasitologie-mycologie,
Institut de microbiologie,
Centre de biologie pathologie,
2Service de réanimation médicale,
Pôle de réanimation,
3Service de gastro-entérologie
et hépatologie, Pôle de spécialités
médicales, CHRU de Lille
Article rec¸u le 29 juillet 2011,
accept´
e le 3 octobre 2011
Résumé. L’incidence des mycoses invasives est en augmentation significa-
tive, notamment chez les sujets immunodéprimés ou ayant des pathologies
sous-jacentes sévères. Elles sont responsables d’une lourde morbidité et d’une
mortalité importante. Ces infections nécessitent donc un diagnostic rapide et
une thérapeutique adéquate mais aussi une prévention optimale chez les sujets
avec des facteurs de risque. Nous rapportons un cas de triple infection fon-
gique associant une aspergillose pulmonaire invasive à Aspergillus fumigatus,
une candidémie à Candida albicans et une pneumocystose à Pneumocystis jiro-
vecci. Le contexte clinique de ce patient est une cirrhose hépatique avec des
antécédents de traitement immunosuppresseur pour une maladie de Crohn et
un lymphome non hodgkinien. Le patient n’a pas rec¸u de prophylaxie antifon-
gique. Sous traitement l’évolution a été défavorable avec décès dans un tableau
de défaillance multiviscérale.
Mots clés : triple infection fongique, Candida albicans, Aspergillus fumigatus,
Pneumocystis jirovecci, cirrhose hépatique
Abstract. The prevalence of invasive mycoses is increasing, especially among
patients who are immunocompromised or hospitalized with serious underlying
diseases. Such infections are associated with a high morbidity and significant
mortality, requiring early diagnosis and appropriate treatment but also an opti-
mal prophylaxis in patients with high risk factors. We report a case of triple
fungal infection including an invasive pulmonary aspergillosis by Aspergillus
fumigatus, a candidemia by Candida albicans and a Pneumocystis pneumonia.
The overall clinical picture of this patient was liver cirrhosis with medical history
of immunosuppressive treatment for Crohn disease and a non-hodgkin lym-
phoma. There was no antifungal prophylaxis for this patient. Under treatment,
the issue was unfavourable with multivisceral failure.
Key words: triple fungal infection, Candida albicans, Aspergillus fumigatus,
Pneumocystis jirovecci, liver cirrhosis
L’observation
Monsieur C, âgé de 58 ans est admis le 9 juillet 2010 à
l’unité de soins intensifs de gastro-entérologie et hépato-
logie pour ictère cutanéo-muqueux. Les antécédents de ce
patient sont marqués par un asthme dans l’enfance ; une
maladie de Crohn évoluant depuis 1966 avec atteinte du
grêle et du côlon ayant nécessité de multiples interven-
tions de réduction et plusieurs lignes de traitement médical
avec corticoïdes, azathioprine et infliximab ; un lym-
phome malin non hodgkinien de type B de l’intestin grêle
compliquant le traitement immunosuppresseur en 2007,
traité par chirurgie et chimiothérapie ; une exogénose non
sevrée et une hépatite virale B ancienne guérie. Le diag-
nostic d’hépatite aiguë alcoolique et virale B avec cirrhose
débutante a été posé et le patient traité par ténofovir et
corticothérapie, avec corticorésistance et absence de pro-
jet de transplantation hépatique. L’évolution est marquée
par l’apparition d’un sepsis évoluant vers un choc sep-
tique et la découverte d’une pleuropneumopathie droite. Le
malade a bénéficié d’une antibiothérapie probabiliste asso-
ciant pipéracilline-tazobactam et ciprofloxacine, et d’une
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 25/05/2017.

90 Ann Biol Clin, vol. 70, n◦1, janvier-février 2012
Biologie au quotidien
expansion volémique. Devant l’instabilité persistante, il a
été transféré en réanimation le 20 août 2010.
L’examen clinique montre une température à 37,5 ◦C, un
ictère cutanéo-muqueux majeur, une pression artérielle à
96/39 mmHg, une fréquence cardiaque à 130 min, une fré-
quence respiratoire à 26 cycles/min, des râles bronchiques
bilatéraux et une saturation à 93 % sous 9 L/min d’oxygène.
L’examen neurologique est normal en dehors d’un discret
astérixis et on note également une hépatomégalie avec des
angiomes stellaires.
Sur le plan paraclinique, l’ECG est normal, la radiogra-
phie du thorax objective un épanchement pleural droit de
moyenne abondance et une opacité alvéolaire de la base
droite (figure 1). Le bilan biologique initial montre des leu-
cocytes à 23 G/L, la concentration en hémoglobine à 76 g/L,
des plaquettes à 62 G/L, le TCA à 100 s (témoin à 32 s), le
TP à 17 %, les monomères de fibrine à 150 g/mL et les
D-dimères à 4,5 g/mL. L’urée était à 23 mmol/L, la créa-
tinine à 371 mol/L, la kaliémie à 4,5 mmol/L, la natrémie
à 130 mmol/L, la calcémie à 1,75 mmol/L, la phospho-
rémie à 1,58 mmol/L, la bilirubine totale à 508 mol/L
(avec une bilirubine directe à 349 mol/L) et les valeurs
des enzymes de cytolyse à 3 fois la normale. La protéine C
réactive est à 53 mg/L et la procalcitonine à 0,8 ng/L. La
mesure des gaz du sang réalisée sous 12 L/min d’oxygène
retrouve un pH à 7,17, une PaCO2à 36 mmHg, une PaO2à
104 mmHg, des bicarbonates à 13 mmol/L et une lactatémie
à 7 mmol/L.
Documentation microbiologique
Dès l’admission, un examen bactériologique standard et
la recherche de bacilles acido-alcoolo-résistants (BAAR)
dans le liquide broncho-alvéolaire (LBA) et dans le
liquide pleural sont négatifs. Les recherches d’antigénurie
Legionella (BinaxNOW®) et d’anticorps sériques anti-
Chlamydia pneumoniae sont également négatives. La
recherche de virus respiratoires (Adenovirus, Influenza,
Parainfluenza,virus respiratoire syncitial, Herpes simplex
virus, Varicelle-zona virus, Cytomegalovirus) en immu-
nofluorescence directe et en culture est restée négative
dans le LBA. L’examen direct du LBA en mycologie
a révélé la présence de rares filaments mycéliens sep-
tés (figure 2). La mise en culture a permis l’isolement
d’Aspergillus fumigatus. La sensibilité aux antifongiques
a été réalisée par la méthode E-test®permettant d’estimer
les concentrations minimales inhibitrices (CMI) pour
les principaux antifongiques systémiques : itraconazole
(0,38) ; voriconazole (0,125) ; caspofungine (0,023) posa-
conazole (0,094) ; amphotéricine B (3). Le diagnostic
d’aspergillose invasive a été conforté par la mise en
évidence d’antigène aspergillaire (Platelia®) dans le LBA
(index = 5,5) et dans le sérum (index = 4,8). Bien que
l’examen microscopique du LBA n’ait pas permis de révé-
ler des formes trophiques ou kystiques de Pneumocystis,
l’immunofluorescence directe (kit Bio-rad) a permis de
révéler de très rares formes kystiques de P. jirovecci. Ces
résultats ont été confirmés par PCR en temps réel (amplifi-
cation du gène mt LSU RNAr).
Deux hémocultures et des urines ont été également pré-
levées. Candida albicans a été isolée à la fois dans les
hémocultures et dans les urines. Son profil de sensibilité aux
antifongiques a permis de révéler des CMI (E-test®) très
faibles vis-à-vis de flurocytosine (0,06), amphotéricine B
(0,25), fluconazole (1), voriconazole (0,06), caspofungine
(0,03), posaconazole (0,125) anidulafungine (0,015) mica-
fungine (0,03), à l’exception de l’itraconazole (0,25). Le
ABC
DFE
Figure 1. Radiographie du thorax à l’admission du patient en gastro-entérologie le 10 juillet 2010 montrant un parenchyme pulmonaire
normal (A), puis le 18 août 2010 quand le patient avait présenté une pleurésie et des opacités alvéolaires irrégulières de la base droite
(B). Les radiographies ultérieures (C-F) réalisées respectivement les 20, 21, 22 et 23 août 2010 après admission du patient en réanimation
montrent une aggravation rapide des lésions précédentes et une extension au poumon controlatéral.
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 25/05/2017.

Ann Biol Clin, vol. 70, n◦1, janvier-février 2012 91
Triple infection fongique chez un patient avec cirrhose hépatique
B
A
Figure 2. Frottis du liquide de lavage broncho-alvéolaire après coloration au giemsa (A) ou au bleu de toluidine (B) mettant en évidence
de rares filaments mycéliens septés et à bords parallèles (x 500).
diagnostic de candidémie a été conforté par la mise en évi-
dence d’une antigénémie Candida à 311 pg/mL (Platelia®).
La présence de ßD-1,3-glucanes (Fungitell®) à 1 608 pg/mL
est compatible avec le diagnostic d’une ou plusieurs infec-
tion(s) fongique(s) invasive(s).
La prise en charge initiale a consisté en la poursuite de
l’oxygénothérapie puis intubation et ventilation mécanique,
expansion volémique et transfusions, une corticothérapie
et un traitement anti-infectieux fait de pipéracilline-
tazobactam, ciprofloxacine et fluconazole puis introduction
le 21 août 2010, de caspofungine et voriconazole après
découverte de filaments aspergillaires dans le LBA.
L’évolution clinique a été défavorable avec persistance
d’une instabilité hémodynamique majeure, un syndrome
de défaillance multiviscérale malgré un traitement optimal.
La réanimation et les thérapeutiques actives ont été arrêtées
après 48 h avec constatation du décès du patient.
Le point de vue du clinicien
L’incidence des mycoses invasives est en forte progres-
sion. Les principaux agents en cause sont représentés par
Candida spp., Cryptococcus neoformans,Pneumocystis
jirovecii et Aspergillus sp. [1]. Les maladies fongiques inva-
sives (MFI) en l’absence d’une prise en charge rapide et
adéquate sont d’un mauvais pronostic. Les patients de soins
intensifs avec une défaillance multiple d’organes ainsi que
les patients immunodéprimés de manière sévère ou prolon-
gée sont particulièrement à risque. Les MFI chez les patients
immunocompétents sont extrêmement rares. De ce point
de vue, les MFI peuvent être toutes considérées comme
des maladies opportunistes [2]. Dans notre observation, le
patient présentait une combinaison de facteurs de risque
incluant, d’une part, une thérapeutique immunosuppressive
pour la maladie de Crohn associant de l’azathioprine, des
corticoïdes et un anti-TNF␣, l’infliximab et, d’autre part, le
lymphome non hodgkinien et la cirrhose hépatique.
La survenue d’infections opportunistes au cours de thé-
rapeutiques immunosuppressives est bien connue. Plus
particulièrement l’utilisation des anti-TNF␣qui a révo-
lutionné la prise en charge de plusieurs pathologies
inflammatoires chroniques, a été associée à un risque
accru d’infections opportunistes dont notamment à champi-
gnons. Les infections fongiques rapportées dans ce contexte
sont diverses et les agents en cause peuvent être des
levures, des champignons filamenteux ou des champignons
dimorphiques endémiques [3]. La cirrhose hépatique a été
rapportée comme un facteur favorisant d’infections fon-
giques chez des patients n’ayant pas d’autres pathologies
sous-jacentes [4]. Les sujets ayant une défaillance hépatique
présentent en effet une atteinte profonde de l’immunité
même en l’absence de thérapeutiques immunosuppressives
et leur taux de lymphocytes est inversement proportionnel
à la défaillance hépatique [5]. Les candidémies surviennent
fréquemment sur ce terrain et sont greffées d’une très forte
mortalité [6]. L’aspergillose pulmonaire invasive a été éga-
lement rapportée chez ces patients avec une issue souvent
fatale et même une cirrhose non décompensée est un facteur
de risque d’aspergillose invasive [7]. Le clinicien doit donc
y penser devant une fièvre persistante, sans étiologie bacté-
rienne documentée. Il se pose également la question de la
prévention de ces infections chez le patient ayant une cir-
rhose hépatique. À notre connaissance, aucune prophylaxie
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 25/05/2017.

92 Ann Biol Clin, vol. 70, n◦1, janvier-février 2012
Biologie au quotidien
antifongique spécifique n’est actuellement recommandée
chez ce type de patient. Une prophylaxie efficace et stan-
dardisée des MFI est difficile à mettre en œuvre en raison
de la multiplicité des agents pathogènes incriminés.
Le point de vue du biologiste
La prise en charge des maladies fongiques invasives reste
un véritable défi pour les cliniciens s’occupant de patients
avec des facteurs de risque. La non-spécificité des symp-
tômes représente un obstacle pour le diagnostic précoce de
certitude, nécessaire pour un choix judicieux des antifon-
giques tenant compte du spectre d’activité et du risque de
résistance. De plus, les cultures mycologiques, gold stan-
dard pour le diagnostic, peuvent être négatives surtout aux
stades précoces de l’infection. Par ailleurs, obtenir un pré-
lèvement d’un site normalement stérile pour la culture ou
l’histopathologie peut nécessiter des techniques invasives,
et il est difficile de déterminer si une culture positive pro-
venant d’un site non-stérile est due à une contamination ou
à une véritable infection [8]. De nouveaux marqueurs séro-
logiques ont donc été développés pour tenter de répondre à
l’exigence de rapidité du diagnostic. Le ßD-1,3-glucane est
un composant commun de la paroi fongique qui permet la
détection avec de bonnes performances de divers champi-
gnons à l’exception de Cryptococcus et des zygomycètes.
L’exclusion d’une candidose invasive dans les cas suspects
est par exemple une bonne indication de ce test, vu sa bonne
valeur prédictive négative, mais une standardisation reste
encore nécessaire. La détection du galactomannane dans
le diagnostic de l’aspergillose invasive est de plus en plus
fréquente et ce test sérologique présente une bonne sensi-
bilité et une bonne spécificité. La recherche de l’antigène
mannane peut être également très intéressant dans le
diagnostic précoce de candidose invasive. Ces marqueurs
n’ont pas été encore suffisamment évalués pour les autres
liquides biologiques [9, 10]. Les méthodes de biologie
moléculaire peuvent également être d’une grande utilité
pour affirmer la présence d’un agent fongique et pour
l’identifier, mais elles restent limitées par l’indisponibilité
de tests commerciaux standardisés [9].
La rapidité du diagnostic au cours des infections fongiques
invasives, notamment chez les sujets à risque, reste une pré-
occupation majeure. En dépit de leurs limites, les nouveaux
marqueurs antigéniques apportent parfois des réponses
utiles mais ils doivent être encore améliorés, mieux évalués
et standardisés.
Conflits d’intérêts : aucun.
Références
1. Pfaller MA, Diekema DJ. Epidemiology of invasive mycoses in North
America. Crit Rev Microbiol 2010 ; 36 : 1-53.
2. Pappas PG. Opportunistic fungi : a view to the future. Am J Med Sci
2010 ; 340 : 253-7.
3. Marie I, Guglielmino E. Non tuberculous anti-TNF associated oppor-
tunistic infections. Rev Med Interne 2010 ; 31 : 353-60.
4. Rolando N, Harvey F, Brahm J, Philpott-Howard J, Alexander G, Case-
well M, et al. Fungal infection : a common, unrecognised complication of
acute liver failure. J Hepatol 1991 ; 12 : 1-9.
5. Lombardo L, Capaldi A, Poccardi G, Vineis P. Peripheral blood CD3
and CD4 T-lymphocyte reduction correlates with severity of liver cirrhosis.
Int J Clin Lab Res 1995 ; 25 : 153-6.
6. Safdar A, Bannister TW, Safdar Z. The predictors of outcome in immu-
nocompetent patients with hematogenous candidiasis. Int J Infect Dis
2004;8:180-6.
7. Lipke AB, Mihas AA. Non-decompensated cirrhosis as a risk factor for
invasive aspergillosis : a case report and review of the immune dysfunction
of cirrhosis. Am J Med Sci 2007 ; 334 : 314-6.
8. Stevens DA. Diagnosis of fungal infections : current status. J Antimi-
crob Chemother 2002 ; 49(Suppl. 1) : 11-9.
9. Chandrasekar P. Diagnostic challenges and recent advances in the early
management of invasive fungal infections. Eur J Haematol 2009 ; 84 : 281-
90.
10. Kedzierska A, Kochan P, Pietrzyk A, Kedzierska J. Current status of
fungal cell wall components in the immunodiagnostics of invasive fungal
infections in humans : galactomannan, mannan and (1–>3)-beta-D-glucan
antigens. Eur J Clin Microbiol Infect Dis 2007 ; 26 : 755-66.
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 25/05/2017.
1
/
4
100%