TP de chimie

CH 14 : LA REACTION CHIMIQUE
Activité expérimentale : Etude de quelques réactions chimiques
Notion contenu
Compétences expérimentales
- Décrire l’état d’un
système avant et après
transformation.
- Savoir justifier ses réponses de manière rigoureuse à
partir de données précises.
- Ecrire l’équation bilan d’une réaction.
- Savoir rédiger
CONSIGNE : Rédigez vos réponses sur une feuille réponse A4.
INTRODUCTION :
Au cours du TP, il vous sera demandé de faire un schéma descriptif de la
transformation. Ce schéma est basé sur le modèle suivant : il faudra simplement
adapter les termes en italique à chaque expérience.
1. COMBUSTION DU CARBONE DANS LE DIOXYGENE
Expérience : Un morceau de carbone chauffé au rouge est introduit dans un flacon
contenant du dioxygène. Observer l’expérience. Par la suite, vous introduirez de
l’eau de chaux dans le flacon.
Répondre aux questions sur votre feuille réponse :
a) Qu’observez-vous au cours de la réaction ?
b) Quelle espèce chimique est mise en évidence par le test à l’eau de chaux ?
c) Reste-il du carbone solide ? Quelle peut-être alors la cause de l’arrêt de
l’évolution du système ?
d) Pouvez-vous affirmer qu’il y a eu transformation chimique du système ?
Pourquoi ?
e) Faire un schéma descriptif de la transformation.
2.SOLUTION DE SULFATE DE CUIVRE ET D’HYDROXYDE DE SODIUM
expérience préliminaire : Introduire un (petit) morceau de sulfate de sodium dans
un tube à essais contenant de l’eau. Agiter. Les ions sulfate et sodium peuvent-ils
coexister en solution aqueuse ?
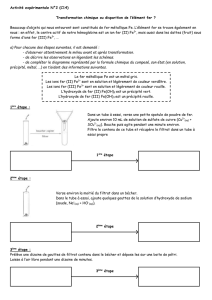
expérience étudiée : Dans un bécher, introduire 10,0 mL de solution de sulfate de
cuivre à 0,1 mol/L.
Dans un autre bécher, verser le même volume de solution d’hydroxyde de sodium
(soude) à 0,1 mol/L. Décrire les deux solutions (couleur, état physique).
Verser le contenu d’un bécher dans l’autre. Décrire ce que vous avez observé lors
du mélange.
Etat initial (
T,P
)
Espèces présentes
Etat final (
T,P
)
Espèces formées
Espèces restantes
Transformation
chimique
T et P sont respectivement
la température et la
pression de la salle que
l’on précisera pas
aujourd’hui.

Répondre aux questions sur votre feuille réponse :
a) D’après l’expérience préliminaire, pouvez-vous dire si les ions sulfates et sodium
sont intervenus lors de l’évolution du système étudié ? Justifiez votre réponse.
b) En vous appuyant sur la conservation de la matière, proposer une formule pour
l’espèce solide neutre qui a été formée. Expliquez votre raisonnement.
c) Y a-t-il eu transformation chimique ? Pourquoi ?
d) Donner l'équation chimique de la réaction.
e) Faire un schéma descriptif de la transformation.
f) Quelles sont les espèces présentes en début de réaction et qui le sont encore en
fin de réaction ? Proposez des tests qui pourraient confirmer vos hypothèses.
Décrire précisément ce que vous proposez.
Pour vous aider.
Voici quelques renseignements pour mettre en évidence quelques ions en solution. S’il y a un précipité dans la
solution, il faut l’éliminer avant toute autre manipulation en le filtrant.
L'ion sodium est incolore et ne peut pas être mis en évidence.
L'ion sulfate peut être mis en évidence par ajout de quelques gouttes d'une solution de chlorure de baryum :
on obtient un précipité blanc de BaSO4 (s).
L'ion cuivre peut être mis en évidence par ajout de quelques gouttes de soude : on obtient un précipité bleu
roi de Cu(OH)2 (s).
3. Une autre réaction
Expérience : Introduire :
dans un tube à essais noté A, 5 mL d’une solution aqueuse de chlorure de calcium (Ca2+ ; Cl-)
dans un tube à essais noté B, 5 mL d’une solution aqueuse d’oxalate d’ammonium (NH4+ ; C2O42-)
dans un tube à essais noté C, 5 mL d’une solution aqueuse de chlorure d’ammonium (NH4+ ; Cl-)
Mélanger dans un bécher, les deux solutions contenues dans les tubes à essais A et B, puis observer.
Répondre aux questions sur votre feuille réponse :
a) Quel est l’aspect de chacune des solutions contenues dans les tubes à essais,
avant le mélange ?
b) Qu’observe t’on lors du mélange ? Une nouvelle espèce chimique s’est elle
formée ? Quel est son état physique ?
c) Compte tenu des espèces chimiques présentes dans l’état initial et de l’aspect du
tube à essais C, quelle est la formule de l’espèce chimique électriquement neutre
apparue ?
d) Quelles sont les espèces chimiques présentes dans le bécher en fin de réaction ?
e) Faire un schéma descriptif de la transformation.
Justifier ses réponses
Ecrire les équations bilans
Savoir rédiger
1
/
2
100%