CH 12 L`ACIDE CHLORHYDRIQUE ET LES MÉTAUX

CH 12 L’ACIDE CHLORHYDRIQUE ET LES MÉTAUX
I- UNE EXPLOSION SURPRENANTE (Démarche d'investigation)
Matériel par groupe : 3, tubes à essais + bouchons, un portoir, paires de lunettes, 1 petit
erlenmeyer
Matériel au bureau : poudre de Cu, Zn et Fe, acide chlorhydrique 1 mol/L, allumettes.
Une violente explosion est survenue hier au soir à la Société KISTOCTOU. Cette explosion a eu
lieu dans un entrepôt de matériaux métalliques causant quelques blessures à un employé de
l’entreprise.
M Le Grix, la victime de cet accident, est
chargé de vérifier en fin de journée si le
matériel est correctement rangé et de noter
tout ce qui lui semble être anormal avant de
fermer les locaux pour la nuit. Le drame
aurait eu lieu lorsque l’employé aurait
voulu visiter le dernier entrepôt où sont
stockés plusieurs types de métaux. D‘après
son témoignage, l’explosion est survenue
lorsqu’il a actionné l’interrupteur de la
lumière afin qu’il puisse y voir plus clair :
<< Dès que j’ai appuyé sur le bouton, j’ai
été soufflé par l’explosion ! Les murs ont
vibré dans un fracas d’enfer !!! J’ai eu la
trouille de ma vie >>
Heureusement, M Le Grix s’en sort avec un bon mal de crâne et quelques côtes fêlées.
La police scientifique chargée de faire toute la lumière sur l'origine de l'explosion a retrouvé sur les
lieux de l'explosion plusieurs éléments : différents métaux éparpillés un peu partout, la présence
d'un liquide, un mégot de cigarette, le mur séparant les 2 entrepôts est éventré et le carnet de M Le
Grix où sont notées ses diverses observations. L'employé aurait signalé, il a plusieurs semaines,
que plusieurs bidons d’acide chlorhydrique dans le local voisin de celui des métaux étaient très mal
<< calés >> et risquaient alors de tomber et de se briser.
Le directeur de l’entreprise n’explique pas encore l’origine de cet accident : << C’est
incompréhensible. Dans ce local seuls des métaux inoffensifs sont stockés : du cuivre, du zinc, du
fer et de l’aluminium. Dans l'autre local, il n'y avait que des bidons d'acide chlorhydrique mais
l'acide chlorhydrique n'est pas un liquide explosif !! >>.
Enfin, des échantillons d'ADN ont été prélevé sur l'ensemble des employés et du directeur de la
société KISTOCTOU. Il s'avère que l'ADN retrouvé sur le mégot de cigarette appartient à M Le
Grix.
Vous êtes un enquêteur membre de la police scientifique. Le commissaire a chargé votre équipe
d'élucider ce mystère. A vous de mener l'enquête …
Votre commissaire attend des résultats rapides.
Votre rapport doit être sur son bureau dans 45 min … sinon vous serez dessaisit de l'affaire !!!
1

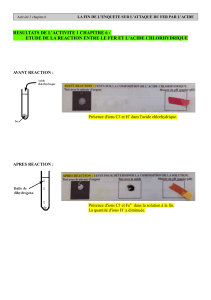
II- ATTAQUE DU FER PAR L'ACIDE CHLORHYDRIQUE
21- Expérience
Matériel élèves : 3 tubes à essais, deux bouchons, une solution d’acide
chlorhydrique, des allumettes, une coupelle, une solution de
nitrate d’argent, une solution de soude, de la poudre de fer
On filtre la solution B. Le filtrat incolore est partagé en 2 tubes (C et D) et dilué
avec de l’eau.
Dans C, on ajoute quelques gouttes de nitrate d’argent.
Dans D, on ajoute quelques gouttes de soude.
22- Observations
En B, on observe : Il y a une détonation
En C, on observe un précipité blanc qui noircit à la lumière.
En D, on observe un précipité vert
2
Solution B
D
C
Solution B
Soude
Nitrate d’argent
Acide chlorhydrique
Poudre de fer
Allumette
Solution obtenue
B
A

23- Interprétation
Livre Bordas, Collection ESPACE, 2008, p 81, Activité 1
A l’aide des expériences et du livre, répondre aux questions 6,7 et 8 du livre p81.
Aide :
- Le dioxyde de carbone est un gaz qui est produit lors d’une combustion (4ème).
- Le dioxygène est un comburant : c'est un gaz qui permet de fiare brûler (4ème)
- Quand on approche une allumette enflammée d'un tube à essais contenant du
dihydrogène. Il se produit un bruit caractéristique appelé « jappement ».
- Le dichlore est un gaz jaune vert, très toxique. Quand on associe du dichlore à du
dihydrogène, on produit de l’acide chlorhydrique
Q6a : On doit exclure obligatoirement le CO2 car il n’y a pas de carbone dans les
réactifs. On peut penser aux autres gaz car on dans les réactifs des atomes de Cl,
O et H.
Q6b : Seuls les ions Fe2+ et Fe3+ peuvent se former car on a dans les réactifs des
atomes de fer.
Q6c : C’est du dihydrogène (H2) car on a un jappement quand on approche une
allumette enflammée du tube à essais.
Q7 : Le test au nitrate d’argent donne un précipité blanc qui noircit à la lumière : on
présence d’ions chlorure (Cl- ).
Le test à la soude (ou hydroxyde de sodium) donne un précipité vert : on
présence d’ions Fe2+
Q8 : La solution ionique formée est composée d’ions Fe2+ et d’ions Cl-, donc on a une
solution de chlorure de fer II : Fe2+ + 2 Cl-
3

24- Conclusion
Q9a : Le bilan de la réaction entre le fer et l’acide chlorhydrique est :
Fer + acide chlorhydrique → chlorure de fer II + dihydrogène
Q9b : L’équation de réaction (ou bilan) entre le fer et l’acide chlorhydrique est :
Fe + 2 (H+ + Cl-) → (Fe2+ + 2 Cl-) + H2
Pour équilibrer une équation de réaction, il faut :
- que chaque solution ionique soit électriquement neutre (on
les met entre parenthèses)
- qu'il y ai le même nombre de chaque espèce dans les
réactifs et les produits
Dans cette réaction, les ions Cl- sont en même nombre dans les réactifs et les
produits. On en déduit que ces ions n'interviennent pas dans le bilan de la
réaction: on dit que ce sont des ions spectateurs.
Dans une équation de réaction simplifiée, on élime les ions spectateurs et on a :
Fe + 2 H+ → Fe2+ + H2
III- ATTAQUE DU ZINC PAR L’ACIDE CHLORHYDRIQUE ?
Le zinc réagit de manière analogue au fer avec l'acide chlorhydrique. A l'aide des même test,
on met en évidence la formation de : dihydrogène et de chlorure de zinc
Bilan :
zinc + acide chlorhydrique dihydrogène + chlorure de zinc
Equation bilan :
Zn + 2 (H+ + Cl -) H2 + (Zn 2+ + 2 Cl -)
Equation bilan simplifiée :
Dans l’équation bilan simplifiée, on enlève les ions chlorures (Cl -) car ils n’interviennent
pas dans la réaction chimique : on dit qu’ils sont spectateurs
Zn + 2 H+ H2 + Zn 2+
4

IV- EXERCICES
BORDAS ESPACE 2008 : EX7 P 87 ; EX 8 ET 13 P 88 ; EX 14 ET 15 P 89
Ex 7 p 87
1- Fer + acide chlorhydrique → chlorure de fer II + dihydrogène
2- a- La 1ère est fausse car il y a Fe2+ dans les réactifs
b- La 2ème est fausse car il y a H2 dans les réactifs
c- La 3ème est fausse car elle n'est pas équilibrée
d- La 4ème est bonne (bien équilibrée)
3- Les ions chlorures (Cl-) n'apparaissent pas dans les équations de réaction
simplifiée car les ions chlorures sont ici des ions spectateurs
4- Les ions Cl- permettent que la solution soit électriquement neutre
Ex 8 p 88
Tube A : On une détonation donc on a mis en évidence du dihydrogène
Tube B : On a précipité blanc quand on ajoute une solution de nitrate d'argent ; on a
donc présence d'ions chlorure
Tube C : On a un précipité vert quand on ajoute de la soude ; on a donc présence
d'ions Fe2+.
Ex 13 p 88
1- zinc + acide chlorhydrique → chlorure de zinc + dihydrogène
2- métal + acide chlorhydrique → chlorure du métal + dihydrogène
3- Non, on n'aurait pas obtenu le même bilan. En échange, il suffit juste de remplacer
les ions Cl- par des ions SO42-.
4- fer + acide sulfurique → sulfate de fer II + dihydrogène
Fe + ( 2 H+ + SO42-) → (Fe2+ + SO42-) + H2
Si on supprime les ions spectateurs (donc ici les ions SO42-), alors on l'équation de
réaction simplifiée :
Fe + 2 H+ → Fe2+ + H2
Ex 14 p 88
1- Le cuivre n'est pas attaqué par l'acide chlorhydrique
2- Le cuivre est attaqué par l'acide nitrique
3- Les ions H+ ne sont pas responsables de l'attaque du cuivre l'acide nitrique
car il y a des H+ dans l'acide chlorhydrique et pourtant il n' y a pas d'attaque
du cuivre par l'acide chlorhydrique.
4- Il faut exclure le dihydrogène car les ions H+ ne réagissent pas avec le
cuivre.
5- C'est l'ion cuivre II (Cu2+)
6- L'atome de cuivre s'est transformé en ion cuivre II
Ex 15 p 89
1- Le cuivre n'est pas attaqué par l'acide chlorhydrique alors que le zinc est
attaqué par l'acide chlorhydrique. Donc il ne reste en surface que du cuivre
métal car le zinc s'est transformé en Zn2+ , d'où la couleur rougeâtre.
2- Le cuivre est attaqué par les ions nitrates de l'acide nitrique et le zinc est
attaqué par les ions H+ de l'acide nitrique. Le cuivre et le zinc étant attaqué
en même temps, le laiton apparaitra ainsi toujours jaune.
5
 6
6
1
/
6
100%