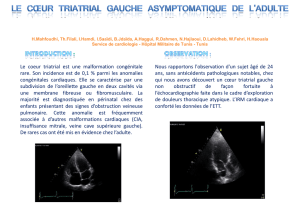
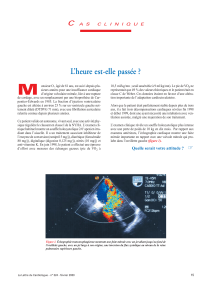
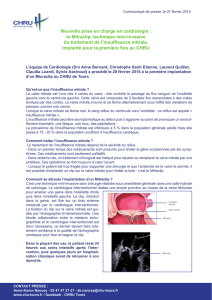
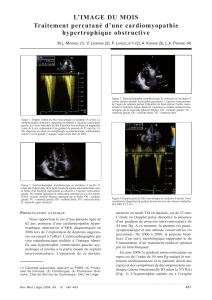
Hypertrophic Obstructive Cardiomyopathy

"And he said to me, you must have
made a mistake. I left the operating
room very humbled."
1959
Eugene Braunwald Andrew G. Morrow
1859 H. LIOUVILLE
Hypertrophic
Cardio
Myopathy

1-EH 4 0566 01 11/2010 2

Morrow Procedure (Sixties)

Morrow Procedure (Sixties)
« the incisions are made quite close to the seat of the soul »
5 / 10 gr

Morrow Procedure (Results)
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
1
/
36
100%