Surveillance du virus Schmallenberg en France : une circulation peu

Bulletin épidémiologique, santé animale et alimentation no72 – Décembre 2015 27
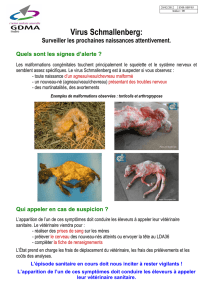
La surveillance événementielle des formes congénitales de
l’infection par le virus Schmallenberg (« SBV congénital ») a été
initiée en France au début du mois de janvier 2012 par la Direction
générale de l’Alimentation, dans le cadre de la Plateforme nationale
d’épidémiosurveillance en santé animale (Plateforme ESA), à la suite de
l’alerte européenne relative à l’émergence de ce virus (note de service
DGAL/SDSPA/N2012-8007 du 4 janvier 2012). Les naissances de veaux,
d’agneaux et de chevreaux malformés ont ainsi révélé des infections
ayant eu lieu pendant la période d’activité des vecteurs (Culicoides) au
cours de l’été et de l’automne 2011. À la clôture de cette première saison
de surveillance (31 août 2012), des foyers de SBV congénital avaient
été confirmés dans 2 976 exploitations (1 817 bovines, 1 139 ovines et
20 caprines) principalement localisées dans la moitié nord du pays
(centre ouest et nord est) (Dominguez et al., 2012).
Le virus SBV ayant réussi à « passer l’hiver », la surveillance du SBV
congénital s’est poursuivie à partir du 1er septembre 2012 dans le cadre
de la Plateforme ESA, coordonnée à partir de cette date par GDS France.
La deuxième saison de surveillance s’est étalée du 1er septembre 2012
au 31 août 2013, révélant des infections ayant eu lieu au printemps/
été/automne 2012 (Gache et al., 2013). Au total, 1 834 exploitations
principalement localisées dans l’ouest et la moitié sud du pays ont été
confirmées atteintes lors de cette deuxième saison de surveillance
dont 1 531 exploitations bovines, 271 ovines et 32 caprines.
En 2013/2014, la surveillance du SBV congénital s’est logiquement
poursuivie dans l’objectif de continuer à suivre l’évolution de
la distribution géographique de la maladie. Après deux années
de circulation intense sur le territoire, cette troisième saison de
surveillance a permis d’identifier 110 exploitations atteintes. La
diminution du nombre de foyers rapportés en 2013/2014 par rapport
aux deux premières saisons de surveillance a été attribuée à une forte
proportion d’animaux devenus immuns suite à une infection naturelle
et à une diminution de la sensibilité du dispositif de déclaration, la
maladie étant considérée comme une maladie d’élevage (ne faisant
pas, à ce titre, l’objet d’une règlementation) à la clinique évocatrice
(malformations caractéristiques ne nécessitant pas de confirmation
biologique).
À la clôture de la saison 2013/2014 s’est ainsi naturellement posée la
question de l’évolution de la circulation virale en France et de la suite à
donner au dispositif de surveillance. En s’appuyant sur les propositions
avancées dans l’avis de l’Anses publié en février 2014 « Évaluation de
risques liés à la diffusion du virus Schmallenberg en France : bilan et
perspectives » (Anses, 2014), et après avoir recueilli le sentiment des
acteurs concernés, le groupe de suivi de la Plateforme ESA a considéré
qu’il était opportun de maintenir une surveillance minimale en
matière de SBV congénital. Ainsi, l’objectif de la surveillance du SBV
congénital pour la saison 2014/2015 était exclusivement qualitatif :
savoir si le virus SBV continuait à circuler en France métropolitaine.
Les modalités organisationnelles de cette surveillance sont présentées
dans l’Encadré 1.
Cet article présente les résultats de la surveillance des formes
congénitales du SBV du 1er septembre 2014 au 31 août 2015,
conséquences de la circulation virale en France au printemps/été/
automne 2014.
Résultats
Participation des départements
D’après une enquête réalisée auprès des GDS, onze départements n’ont
pas souhaité participer à la surveillance du SBV congénital pour la
saison 2014/2015 selon les modalités proposées par la Plateforme ESA
(Figure 1). Ceux qui ont participé ont souhaité maintenir la surveillance
jusqu’à concurrence des vingt suspicions (selon les modalités définies
par le groupe de suivi de la Plateforme ESA (Encadré 1)).
Résumé
Les résultats de surveillance des formes congénitales de
l’infection par le virus Schmallenberg (« SBV congénital »)
lors de la saison 2014/2015 indiquent que le virus a très
probablement circulé à bas bruit en 2014 sur une grande
partie du territoire métropolitain : des cas cliniques de SBV
congénital ont été confirmés biologiquement dans sept
départements et des suspicions cliniques non confirmées
ont été enregistrées dans quatorze autres départements.
Après une circulation massive en 2011 et 2012, il semblerait
qu’une forte proportion d’animaux réceptifs soient devenus
résistants (suite à une infection naturelle pour une grande
partie, le recours à la vaccination étant resté limité) et que le
virus ait ainsi circulé de façon moins intense en 2013 et 2014.
Des réflexions sont en cours pour améliorer la sensibilité
globale du dispositif et pouvoir détecter une éventuelle
reprise de circulation « massive » du virus sur le territoire
dans les prochaines années.
Mots-clés
Virus Schmallenberg, ruminants, surveillance
épidémiologique
Abstract
Schmallenberg virus surveillance in France: low
circulation in 2014
The results of congenital Schmallenberg disease surveillance
(“congenital SBV”) for the 2014-2015 season indicate that
the virus probably circulated with low prevalence in 2014
throughout a large part of metropolitan France. Indeed,
confirmed SBV cases were reported in seven
départements
and clinical suspicions were reported in another fourteen
départements
. Following massive viral circulation in 2011
and 2012, it seems that the virus then circulated with
lower intensity in 2013 and 2014, probably due to the high
proportion of animals that had become immune following
natural infection in 2011 or 2012 (use of vaccination
remained limited). Discussions are underway to improve
the scheme’s overall sensitivity in order to detect a possible
return to massive viral circulation in France over the next few
years.
Keywords
Schmallenberg virus, Ruminants, Epidemiological
surveillance
Surveillance du virus Schmallenberg
en France :
une circulation peu intense en 2014
Kristel Gache (1)* (kristel.gache.fngds@reseaugds.com), Soline Hosteing (2)*, Jean-Baptiste Perrin (3)*, Stephan Zientara (4), Laure Bournez (5)*,
Anne Touratier (1)
(1) GDS France, Paris, France
(2) SNGTV, Paris, France
(3) Direction générale de l’Alimentation, Bureau de la santé animale, Paris, France
(4) Anses, Laboratoire de santé animale, Maisons-Alfort, France
(5) Anses, Unité de coordination et d’appui à la surveillance (UCAS), Maisons-Alfort, France
* Membre de l’Équipe opérationnelle de la Plateforme nationale d’épidémiosurveillance en santé animale (Plateforme ESA)
Surveillance du virus Schmallenberg en France : une circulation peu intense en 2014

28 Bulletin épidémiologique, santé animale et alimentation no72 – Décembre 2015
Situation départementale
Du 1er septembre 2014 au 31 août 2015, des cas cliniques de SBV
congénital ont été confirmés biologiquement dans sept départements.
Des suspicions non confirmées ont été enregistrées dans quatorze
autres départements (Figure 1).
Description des foyers et des suspicions non confirmées
Espèces concernées
Du 1er septembre 2014 au 31 août 2015, le dispositif a enregistré
dix élevages confirmés atteints (élevages bovins) et 49 élevages (43
élevages bovins, quatre élevages ovins et deux élevages caprins)
dans lesquels des suspicions ont été enregistrées sans avoir été
confirmées biologiquement (observation clinique d’au moins une des
malformations caractéristiques, mais analyses de laboratoire négatives
(pour 46 élevages) ou ininterprétables (pour trois élevages)). Le nombre
de foyers confirmés biologiquement et le nombre d’élevages suspects
non confirmés par département sont présentés dans les Figures 2 et 3.
Le nombre d’élevages suspects par département est inférieur au vingt
suspicions maximum définies par le dispositif.
Fréquence d’observation des malformations
L’anomalie la plus fréquemment observée dans les élevages identifiés
dans le cadre de cette surveillance est l’arthrogrypose, que ce soit dans
les foyers confirmés biologiquement (malformation observée dans
60 % des élevages foyers) mais également dans les élevages suspects
non confirmés (75 %). Cette malformation était déjà la malformation
la plus fréquemment observée lors des saisons de surveillance
précédentes (malformation observée dans 70 % des élevages en
2013/2014, dans 85 % en 2012/2013 et dans 88 % en 2011/2012)
(Dominguez et al., 2012 ; Gache et al., 2013 ; Gache et al., 2015).
La fréquence d’observation des autres malformations dans les élevages
identifiés dans le cadre de cette surveillance est présentée en Figure 4
(à noter que plusieurs malformations peuvent être observées sur le
même animal, par ex. arthrogrypose et brachygnathie). Les fréquences
d’observation des différentes malformations sont proches entre
élevages confirmés et non confirmés.
Taux de confirmation par type d’analyse
Le taux de confirmation des suspicions selon la méthode diagnostique
utilisée est présenté dans le Tableau 1 :
• aucune analyse PCR réalisée dans le cadre de cette surveillance ne
s’est révélée positive en 2014/2015 ;
• le taux de confirmation avec l’outil sérologique sur nouveau-nés
en 2014/2015 s’élève à 21 % (n= 42). Ce taux est inférieur à celui
observé lors de la saison 2013/2014 (37 % (n=41), différence non
significative, khi-deux, p=0,12), et inférieur à celui observé lors de la
saison 2012/2013 (62 % (n=658), différence significative, khi-deux,
p<0,05). Ce taux de confirmation est également inférieur au taux de
confirmation présenté dans certaines publications scientifiques (taux
Encadré 1. Modalités organisationnelles de la surveillance du SBV congénital
Les modalités organisationnelles de cette surveillance ont été définies
par le groupe de suivi de la thématique « Surveillance du virus
Schmallenberg » de la Plateforme ESA, pour répondre à l’objectif de
la surveillance.
Champ de la surveillance et population surveillée
Comme lors des précédentes saisons de surveillance, seules les formes
congénitales de la maladie de Schmallenberg ont fait l’objet d’une
surveillance (Encadré 2). Cette surveillance a concerné l’ensemble des
ruminants domestiques (bovins, ovins et caprins) présents dans les
départements français ayant choisi de participer à la surveillance.
Définition du cas suspect
Les critères cliniques définis dans le cadre de la surveillance
correspondaient à l’observation sur des agneaux, veaux ou chevreaux
d’une ou plusieurs des malformations suivantes :
• déformation ou blocage de l’articulation d’un ou plusieurs membres
(arthrogrypose) ;
• malformation de la colonne vertébrale (scoliose, cyphose) ;
• anomalie du port de la tête (torticolis) ;
• raccourcissement de la mâchoire inférieure (brachygnathie) ;
• « grosse tête » (hydrocéphalie).
Modalités diagnostiques
La surveillance était de nature événementielle (clinique) avec
confirmation biologique des suspicions. En effet, l’objectif de la
surveillance consistant à savoir si le virus circulait sur le territoire, la
confirmation biologique était exigée et permettait, le cas échéant, de
savoir de façon certaine que le virus circulait dans un département, à
partir des suspicions enregistrées.
Dans chaque département participant à la surveillance, les cas suspects
ont fait l’objet de la réalisation par le vétérinaire d’un prélèvement
transmis au laboratoire à fin d’analyse, jusqu’à concurrence de
vingt suspicions au maximum par département. En cas de résultats
négatifs, la surveillance était maintenue jusqu’à concurrence des
vingt suspicions. Lorsqu’un résultat positif était obtenu en cours de la
campagne de surveillance, le choix était laissé au département : soit
de continuer la surveillance jusqu’à concurrence des vingt suspicions,
soit d’arrêter la campagne de surveillance.
Les tests de diagnostic retenus étaient les suivants :
• sérologie sur sang de l’avorton, du mort-né ou du nouveau-né
malformé, avant prise de colostrum : tests ELISA indirect ;
• PCR sur encéphale de l’avorton, du mort-né ou du nouveau-né
malformé.
Le virus Schmallenberg ayant très largement circulé sur le territoire au
cours des trois précédentes années, il est impossible de déterminer les
dates d’infection de femelles séropositives. Les analyses sérologiques
sur femelles ayant mis bas des produits malformés n’ont donc pas été
intégrées à ce protocole de surveillance.
Saisie des données de surveillance
La saisie des données de surveillance (fiche de commémoratifs et
résultats d’analyse) était réalisée par les groupements de défense
sanitaire (GDS) en ligne, via une interface web dédiée.
Financement
La grande majorité des animaux malformés étant non viables et
mourant rapidement après la naissance, ils étaient considérés comme
des avortons. Dans ce cas, la visite et le déplacement du vétérinaire
étaient pris en charge par l’État dans le cadre de la surveillance de
la brucellose. Les frais supplémentaires spécifiquement liés à la
surveillance du SBV congénital étaient pris en charge par les GDS dans
les départements participant à la surveillance.
Figure 1. Situation départementale vis-à-vis du SBV congénital
lors de la saison 2014/2015 (du 1er septembre 2014 au 31 août
2015)
Départements dans lesquels au moins une suspicion confirmée par
analyse de laboratoire a été enregistrée
Départements dans lesquels au moins une suspicion a été enregistrée
mais aucune confirmée
Départements ne participant pas à la surveillance selon les modalités
proposées par la Plateforme ESA

Bulletin épidémiologique, santé animale et alimentation no72 – Décembre 2015 29
de confirmation de 74 % sur 348 agneaux et 111 veaux (Van Maanen
et al., 2012)). Dans ce contexte, des tests de séroneutralisation ont
été réalisés par le Laboratoire de santé animale de l’Anses Maisons-
Alfort sur seize prélèvements sanguins qui étaient négatifs en ELISA
(prélèvements issus d’avortons ou de nouveau-nés présentant des
malformations caractéristiques). Ces analyses n’ont pas révélé de
divergences entre les résultats d’ELISA et les séroneutralisations ;
• à noter que les deux types d’analyses (sérologie et PCR) ont été réalisés
dans trois élevages : pour deux élevages, les résultats se sont révélés
négatifs à la fois en sérologie et en PCR, pour un élevage le résultat
PCR s’est avéré négatif, alors que le résultat sérologique a été positif.
Discussion
Les résultats de surveillance du SBV congénital lors de la saison
2014/2015 indiquent que le virus a circulé de façon certaine dans sept
départements. Dans quatorze autres départements, les suspicions n’ont
pas été confirmées par un test diagnostique. Le taux de confirmation
a été faible pour la saison 2014/2015. Ce résultat apparaît étonnant,
étant donné que les signes cliniques observés (malformations de
type arthrogrypose, scoliose, cyphose, torticolis, brachygraphie ou
hydrocéphalie) sont très spécifiques de l’infection par le virus SBV.
Ce résultat, qui n’est pour l’instant pas expliqué, est à interpréter avec
beaucoup de prudence étant donné le nombre restreint de suspicions
enregistrées. Cependant, les résultats des séroneutralisations réalisées
par le laboratoire de santé animale de Maisons-Alfort (Anses)
permettent d’exclure une dérive de sensibilité de l’outil sérologique
ELISA. On ne peut pas exclure qu’il puisse s’être produit, entre 2012
et aujourd’hui, des mutations du virus SBV qui modifient les épitopes
de neutralisation virale. En effet, il existe, dans la glycoprotéine Gc
du virus, une zone à degré élevé de variabilité et qui possède ce
type d’épitopes (Fischer et al., 2013). Pour vérifier cette hypothèse,
il serait nécessaire d’isoler le virus SBV, pour savoir si la souche qui
circule actuellement a ou non ce type de mutation. À noter que les
conséquences en termes d’immunité de ce genre de mutations ne sont
pour l’instant pas connues.
Figure 4. Fréquence d’observation des différentes
malformations dans les élevages identifiés dans le cadre de la
surveillance du 1er septembre 2014 au 31 août 2015 (données
sur 59 élevages)
0%
10%
20%
30%
40%
50%
60%
70%
80%
Hydrocéphalie
Brachygnathie
Torticolis
Malformations
de la colonne
vertébrale
Arthrogrypose
Foyers confirmés Élevages suspects non confirmés
Figure 2. Nombre de foyers de SBV congénital (confirmés
biologiquement) enregistrés lors de la saison 2014/2015 par
département (du 1er septembre 2014 au 31 août 2015) (les
départements grisés sont les départements ne participant pas
à la surveillance selon les modalités proposées par la
Plateforme ESA)
Figure 3. Nombre de suspicions de SBV congénital (non
confirmées biologiquement) enregistrées lors de la saison
2014/2015 par département (du 1er septembre 2014 au
31 août 2015) (les départements grisés sont les départements
ne participant pas à la surveillance selon les modalités
proposées par la Plateforme ESA)
Nombre
de foyers
3
2
1
Nombre
de suspicions
non confirmées
14
4
3
2
1
Tableau 1. Taux de confirmation des suspicions selon la
méthode diagnostique utilisée (du 1er septembre 2014 au
31 août 2015)
Taux de confirmation des suspicions (en %)
Sérologie du nouveau-
né avant prise de
colostrum
21
(sur n= 42 nouveau-nés malformés
(41 veaux et 1 agneau))
PCR sur encéphale
0
(sur n= 22 nouveau-nés malformés
(17 veaux, 3 agneaux et 2 chevreaux))

30 Bulletin épidémiologique, santé animale et alimentation no72 – Décembre 2015
Le dispositif de surveillance mis en place lors de la saison 2014/2015
avait pour objectif de déterminer si le virus circulait en France sans
avoir l’objectif de quantifier l’intensité de cette circulation. Étant
donné le faible nombre de suspicions déclarées dans les départements
participants (même s’il est fort probable qu’un certain nombre de cas
suspects n’ont pas fait l’objet d’une déclaration), confortées par les
informations remontées par les acteurs locaux (très peu de naissances
d’animaux malformés lors de l’automne/hiver 2014/2015), il semblerait
que le nombre de cas cliniques dus au virus SBV ait été faible sur
le territoire en 2014/2015. Au vu de la répartition géographique de
ces départements, on peut émettre l’hypothèse que le virus a très
probablement circulé à bas bruit en 2014 dans une grande partie du
territoire métropolitain. Après une circulation massive en 2011 et 2012,
il semble donc que le virus ait circulé de façon moins intense en 2013
et 2014.
Ceci peut s’expliquer par une proportion actuellement élevée d’animaux
devenus immuns à la suite d’une infection naturelle en 2011 ou 2012
(le recours à la vaccination est resté limité). En effet, même si la durée
d’immunité post-infectieuse est encore mal connue, les données de
surveillance des animaux précédemment atteints et les connaissances
sur les virus proches du virus Schmallenberg incitent à supposer que
l’immunité est longue (EFSA, 2013).
Cela fait maintenant quatre années que le virus SBV est présent sur
le territoire et il est probable que le virus continue de circuler à bas
bruit. Cette circulation a également été objectivée dans d’autres pays
européens ((Balmer et al., 2015 ; Veldhuis et al., 2015 ; Wernike et al.,
2015). Similairement à ce qui est observé pour le virus Akabane en
Australie (virus proche du SBV), il n’est pas exclu que des flambées
épizootiques pluriennales surviennent dans les prochaines années, si
une grande partie de la population réceptive est de nouveau naïve
au virus SBV (fonction de la durée de l’immunité des animaux, de
la vitesse de renouvellement des populations et de l’intensité de la
circulation virale). Des conditions météorologiques particulières
entrainant une augmentation de l’abondance et/ou de la survie des
vecteurs pourraient également favoriser l’apparition de ces flambées
épizootiques.
Conclusion et perspectives
Le SBV congénital est aujourd’hui considéré comme une maladie
d’élevage et ne fait pas, à ce titre, l’objet d’une réglementation. De ce
fait, sa surveillance est basée sur la déclaration volontaire des éleveurs
et des vétérinaires. Les caractéristiques du SBV congénital, à savoir un
tableau clinique très évocateur et l’absence de solution thérapeutique,
n’incitent pas les éleveurs et les vétérinaires à déclarer cette maladie
désormais bien connue. Dans ce cadre, des réflexions sont en cours
sur les modifications à apporter au dispositif de surveillance pour
2015/2016 pour améliorer sa capacité à détecter si le virus continue
de circuler et s’il y a une augmentation massive de la survenue de cas
cliniques. Une des pistes envisagées est de s’appuyer sur un réseau
de vétérinaires sentinelles, à raison d’un vétérinaire par région. Il
serait demandé à ces vétérinaires de faire part des suspicions de SBV
congénital observées dans leur clientèle, en renseignant une fiche de
commémoratifs et en envoyant une photographie des malformations
observées.
Remerciements
Les auteurs remercient l’ensemble des partenaires impliqués dans la
surveillance du SBV congénital, ainsi que les membres du groupe de suivi
de cette thématique au niveau de la Plateforme ESA.
Références bibliographiques
Anses, 2014. Évaluation de risques liés à la diffusion du virus Schmallenberg
en France : bilan et perspectives. http://www.anses.fr/sites/default/files/
documents/SANT2013sa0047Ra.pdf
Balmer S., Gobet H., Nenniger C., Hadorn D., Schwermer H., Vögtlin A.,
2015. Schmallenberg virus activity in cattle in Switzerland in 2013. Vet.
Rec. doi : 10.1136/vr.103238
Dominguez M., Hendrikx P., Zientara S., Calavas D., 2012. Bilan de la
surveillance de l’infection congénitale par le virus Schmallenberg (SBV)
chez les petits ruminants, 37pp.
http://plateforme-esa.fr/?q=filedepot_download/35495/245
Dominguez M., Hendrikx P., Zientara S., Calavas D., 2012. Bilan de la
surveillance de l’infection congénitale par le virus Schmallenberg (SBV)
chez les bovins, 20pp.
http://plateforme-esa.fr/?q=filedepot_download/35495/244
Efsa, 2 013. Schmallenberg virus: analysis of the epidemiological data (May
2013) European Food Safety Authority, Parma, Italy
http://www.efsa.europa.eu/sites/default/files/scientific_output/files/
main_documents/429e.pdf
Fischer M., Hoffmann B., Goller KV., Höper D., Wernike K., Beer M., 2013.
A mutation ‘hot spot’ in the Schmallenberg virus M segment. J Gen Virol.
94, 1161-1167.
Gache K., Dominguez M., Touratier A., Calavas D., 2013. Bilan de la
surveillance de l’infection congénitale par le virus Schmallenberg Saison
II, 23pp. http://plateforme-esa.fr/?q=filedepot_download/35496/246
Gache K., Hosteing S., Perrin J-B., Zientara S., Touratier A., 2015. Surveillance
de l’infection congénitale par le virus Schmallenberg en France : une
circulation moins intense en 2013. Bull. Epid. Santé Anim. Alim.67, 15-18.
Note de service DGAL/SDSPA/N2012-8007 du 04 janvier 2012. Emergence
orthobunyaviridé (Schmallenberg virus) – surveillance du territoire pendant
l’hiver 2011/2012 http://agriculture.gouv.fr/IMG/pdf/DGALN20128007Z.
pdf
Van Maanen C., Van der Heijden H., Wellenberg GJ., Witteveen G.,
Luttikholt S., Bouwstra R., Kooi B., Vellema P., Peperkamp K., Mars J., 2012.
Schmallenberg virus antibodies in bovine and ovine fetuses. Vet. Rec. 171,
299.
Veldhuis AMB., Mars MH., Roos CAJ., Van Wuyckhuise L., Van Schaik
G., 2015. Two years after the Schmallenberg virus epidemic in the
Netherlands: does the virus still circulate? Transbound. Emerg. Dis. doi:
10.1111/tbed.12349
Wernike K., Hoffmann B., Conraths FJ., Beer M., 2015. Schmallenberg virus
recurrence, Germany, 2014. Emerg. Infect. Dis. 21(7), 1202-4.
Wernike S., Hoffmann B., Bréard E., Botnerc A., Ponsart C., Zientara S.,
Lohsec L., Pozzid N., Viarouge C., Sarradin P., Leroux-Barce C., Rioue M.,
Laloy E., Breithauptf A., Beer M. 2013 Schmallenberg virus experimental
infection of sheep. Vet. Microbiol. 166(3-4), 461-466.
Encadré 2. Les deux formes cliniques de la maladie de
Schmallenberg
SBV congénital :
manifestation différée de l’infection fœtale par
le virus SBV conduisant à la naissance de produits le plus souvent
non viables chez les bovins, ovins et caprins, et se traduisant par
des avortements, de la prématurité et de la mortinatalité associés
à des malformations congénitales diverses (arthrogrypose,
raccourcissement des tendons du jarret, torticolis, torsion du sternum
et du rachis, déformations de la mâchoire et de la tête) ; des troubles
nerveux peuvent également être observés.
SBV aigu :
manifestation aiguë de l’infection par le virus SBV
caractérisée chez les bovins par des épisodes de diarrhée, de baisse
de production laitière et d’hyperthermie, associés éventuellement à
des retours en chaleurs et à des avortements de début de gestation.
Cette forme clinique n’a pas été rapportée chez les petits ruminants
(Wernike et al. 2013). Le SBV aigu n’a pas fait l’objet d’une surveillance
organisée en France.
1
/
4
100%