symptome biochimique

Enzymologie
Intéret de lʼenzymologie :
Activité enzymatique dʼun liquide biologique :
- symptome biochimique (lyse cellulaire) : les enzymes sont intracellulaires
- surveillance dʼune maladie
- explication pathogénique de la maladie
- détection de la présence dʼune enzyme
Outil analytique permettant le dosage dʼun substrat.
I- Définition- Nomenclature
Définitions : cʼest un catalyseurs biologiques qui a une vitesse de réaction élevée et une
spécificité qui va lui permettre dʼéliminer la formation de sous-produits. Pratiquement
toutes les réactions biochimiques sont catalysées par les enzymes.
Classification et nomenclature :
Par le substrat de lʼenzyme :
- Amidon Amylase
- Lipides Lipase
- Protéines Protéases
Par le type de réaction catalysée :
- Déshydorgénases
- Oxydases
- Décarboxylases
Classification internationale (UIBBM)
Classe 1 : oxydo-réductases (un substrat va sʼoxyder et une autre molécule va se réduire
et inversement : réaction dʼoxydo-réduction)
Classe 2 : transférases (enzymes qui vont transférer des groupements chimiques)
Classe 3 : hydrolases (hydrolyse dʼun substrat, intervention de lʼeau)
Classe 4 : lyases (enzymes qui vont enlever au substrat un groupe et vont créer une
double liaison et inversement)
Classe 5 : isomérases (transformation dʼun substrat en son isomère)
Classe 6 : ligaes (liaisons C-S, C-C, C-N, C-O)
Ces classes sont divisées en sous-classes et en sous-sous-classes.
EX : Créatine Kinase : CK
Réaction catalysée :
ATP + Créatine ADP + Créatine phosphate
Enzyme : ATP Créatine Phosphotransférase (EC 2 7 3 2) CK
2 : classe des transférases
7 : sous classe des phosphotransférases
3 : sous classe des phos fonctionnant avec un accepteur azoté (la créatine)
2 : numéro de lʼenzyme à lʼintérieur de la sous-sous classe
L-lactate deshydrogénase : LDH
Réaction catalysée :
S-lactate + NAD+ pyruvate + NADH + H+
Enzyme : L-lactate desyhdrogénase (EC 1 1 1 27) ldh

1 : classe des oxydoréductases
1 : agissant sur les groupe : CH-OH
1 : sous sous classe fonctionnant avec la NAD+ (NADP+) comme accepteur
27 : numéro de lʼenzyme à lʼintérieur de la sous-sous classe
II- Constitution dʼune enzyme
Enzyme entièrement protéiques (ribunucléase)
Enzyme formées en deux partie :
- Apoenzyme (nature protéique)
- Coenzyme (nature non protéique-
Apoenzyme + coenzyme = holoenzyme
Coenzyme :
Second substrat :
- Récation stoechiométrique entre substrat et coenzyme
- Physiologie : la réaction avec le coenzyme est souvent plus importante que celle avec le
substrat
Les sites de fixation du substrat - Le site catalytique de lʼenzyme
Les sites de fixation du substrat
/HVLWHFDWDO\WLTXHGHO¶HQ]\PH
!"#$%&'(#')!#*+,-.+/+0#
Il faut que ces molécules se rencontrent donc quʼelles soient solubles dans lʼeau.
III- Propriétés générales des enzymes
Lʼactivité enzymatique
EX : Une mole de catalase décompose 5 000 000 moles de H2O2 en une minute et à 0°C.
Anhydrase carbonique : CO2 + H2O H2CO3
Catalyse enzymatique : 10^7 fois plus rapide

La catalyse enzymatique
La catalyse enzymatique
A
B
Gf
(WDWILQDOjO¶pTXLOLEUH
%DUULqUHpQHUJpWLTXHG¶DFWLYDWLRQ
Avancement de la réaction
Energie libre du système
Energie libre
G¶DFWLYDWLRQ
de la réaction
non
Catalysée
S
P
Gi
Etat initial
Modification
JOREDOHG¶pQHUJLH
libre 'G
Energie libre
G¶DFWLYDWLRQ
de la réaction
catalysée
!"#$%&'(#')!#*+,-.+/+0#
On va fournir au système moins dʼénergie.
Spécificité :
- Spécificité de la réaction
- Spécificité de substrat
Spécificité de réaction
C
H
N H 2
R
C
O O H
!"#$%&'(#')!#*+,-.+/+0#
: Spécificité de réaction (décarboxylase et désaminase)
Spécificité de substrat :
Etroite : trypsine
Large : pronase
Stéréospécificité :
- Acides aminés de série L ou D
- Saturation des doubles liaisons (cis ou trans) (Fumarase : catalyse lʼhydratation de
lʼacide fumarique (trans) en acide L-malique, inactive sur lʼacide maléique (isomère cis
de lʼacide fumarique))
Les unités :
Dans les conditions optimales de réaction :
- Unité usuelle : U = μmole/min
- Lʼunité internationale : 1 kat = 1 mole/seconde
- Lʼactivité spécifique : activité / mg de protéine. Plus lʼactivité sera élevée plus lʼenzyme
sera à lʼétat pur.

Cinétique enzymatique :
E + S ES → E + P
Cinétique enzymatique
(6ļ(6ĺ(3
!"#$%&'(#')!#*+,-.+/+0#
Au cours du temps le substrat va diminuer et le produit va augmenter, on a donc bien eu
un complexe enzyme-substrat, et ce complexe se dissocie pour revenir à lʼétat initial.
Cette réaction doit etre rapide et la plus faible possible. La réaction enzyme-substrat est
réversible, on va donc avoir un équilibre.
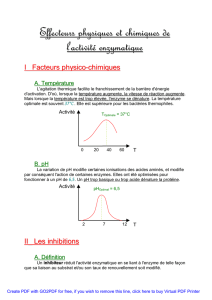
Influence de la température :
Influence de la température
Activation
Dénaturation
(Vitesse de la réaction)
!"#$%&'(#')!#*+,-.+/+0#
(enzyme = protéine)
Quand on augmente la température, lʼagitation moléculaire du milieu augmente, augmente
donc les chances de collision entre enzyme et substrat et sa va passer par un maximum
qui sera la température optimale de la réaction. A un moment donné on a une dénaturation
de la protéine, lʼenzyme perd son activité, donc la courbe de la vitesse de la réaction à
partir de cette température va décroitre.
On observe la résultante de ces 2 courbes (phénomène dʼactivation et de dénaturation).

Influence du pH
Influence du pH
!"#$%&'(#')*#+,-./,0,1#
pH dʼarret qui va stopper la réaction.
Influence des concentrations : réactif : enzyme
Conditions optimales : pH optimum et T optimale
Influence des concentrations:
réactif: enzyme
Conditions optimales, [S] = constante
!"#$%&'(#')"#*+,-.+/+0#
Les réactifs sont le substrat et lʼenzyme. Concentration en substrat constante. On va faire
varier la concentration en enzyme. Le produit P en fonction du temps. Pour une première
concentration en enzyme E1 on a une première courbe si on double la concentration en
enzyme la courbe est haute, si on triple ... On considère quʼau temps t0 on a aucun
produits formés, donc la vitesse initiale est proportionnelle a la concentration en enzyme.
Influence des concentrations : réactif : substrat
Influence des concentrations:
réactif: substrat
Conditions optimales, [E] = constante
!!"#$%&'"&()"*+,-.+/+0"
Lorsquʼon double la concentration substrat la pente de la réaction va augmenter au fur et
à mesure que la concentration augmente. La vitesse est proportionnelle a la concentration
substrat. Lʼasymptote correspond a la vitesse maximum, on sera alors à une concentration
saturante, on peut donc évaluer la concentration en enzyme.
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
1
/
11
100%