Cinétique enzymatique - ASSO-ETUD

Travaux pratiques de chimie physique I
Fournier Coralie, Chappuis Emilie
Groupe E 08.10.2009
- 1 -
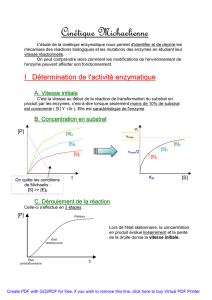
CINÉTIQUE ENZYMATIQUE
1. RÉACTION TRYPSINE - BAPNA
1.1 But
Le but de cette expérience est de déterminer la cinétique, c’est à dire la vitesse, d’une réaction enzymatique,
grâce à la spectroscopie d’absorption optique. L’enzyme étant la trypsine et le substrat de la BAPNA. A l’aide
du Lineweaver-Burk plot KM et Vmax peuvent être déterminés.
1.2 Théorie
Lors d’une réaction enzymatique, il y a deux étapes importantes. La première est la formation d’un complexe
enzyme – substrat, puis, lors de la deuxième étape, il y a formation du produit et la libération de l’enzyme.
PEESSE baa kkk +!→!!! →←+)'(
On admet qu’au début, la vitesse de réaction est constante :
][
0ESkV b
=
Cependant on ne peut connaître la concentration en complexe enzyme – substrat, il faut donc trouver une
relation avec la concentration en substrat et en enzyme qui est connue.
Si on considère que le complexe ES est formé et consommé à la même vitesse « steady state » on a :
- pour la formation du complexe :
]][[ ESEka
- pour la consommation du complexe :
]['][ ESkESkab +
- « steady state »
]][[)']([ SEkkkES aab =+
Au final on trouve donc :
ba
a
kk
SEk
ES
+
='
]][[
][
La concentration totale en enzyme vaut
][][][ ESEE total +=
, qu’on substitue dans l’équation précédente :
( )
ba
totala
kk
SESEk
ES
+
−
='
][][][
][
On regroupe les constantes en une seule et même constante KM appelée constante de Michaelis :
a
ba
Mk
kk
K+
='

Travaux pratiques de chimie physique I
Fournier Coralie, Chappuis Emilie
Groupe E 08.10.2009
- 2 -
Alors on obtient :
][][]][[][ SESESKES totalM =+
et
][
][
][][ SK
S
EES
M
total +
=
Substituons cette dernière équation à l’équation de la vitesse V0 :
][
][
][
0SK
S
EkV
M
totalb +
=
D’après cette équation, on remarque que si la concentration en substrat est beaucoup plus grande que la
valeur de la constante de Michaelis, on peut approximer V0 par :
max0][ VEkV totalb ==
Finalement on trouve l’équation de Michaelis – Menten :
][
][
max0SK
S
VV
M+
=
Dans ce travail pratique, on déterminera expérimentalement la vitesse initiale d’une réaction enzymatique à
diverses concentrations de substrat afin de calculer la constante de Michaelis et la vitesse maximale de cette
réaction. En réarrangeant l’équation de Michaelis – Menten, on remarque que la vitesse initiale est reliée
linéairement à la concentration en substrat :
maxmax0
1
][
11
VSV
K
V
M+⋅=
En faisant un graphique de 1/V0 en fonction de 1/[S], on aura 1/Vmax comme ordonnée à l’origine et et -1/KM
sera l’intersection de la droite avec l’axe des x, i.e., y = 0.
1.3 Partie pratique
La Nα-benzoyl-arginine-p-nitroanilide (BAPNA) est utilisée dans cette expérience comme substrat. Sa liaison
amide sera rompue par l’hydrolyse ce qui génèrera un produit de couleur jaune, la p-nitroaniline. Le DMSO
sera utilisé comme solvant car la BAPNA n’est pas soluble dans l’eau.
L’évolution de la réaction pourra être observée grâce à l’absorption optique de la p-nitroaniline, cela est
possible car le substrat (BAPNA) et le deuxième produit de la réaction sont incolores.
Réaction du substrat (BAPNA) dans la solution d’enzyme (Trypsine) :
H
N
O
N
H
ONO2
(H2C)3
HN
NH2
HN
NH2
N+
O
-O
H
N
O
OH
O
(H2C)3
HN
NH2
HN
+
BAPNA p-nitroaniline
Trypsin
H20
Huit solutions, de concentrations différentes, de substrat (BAPNA+DMSO) sont préparées. Le volume de
chaque solution est de 5 mL. La trypsine (solution d’enzyme) est placée dans une petite cuvette à raison de
2.5 mL auxquels sont ajouté 0.5 mL de solution de substrat. La cuvette est recouverte avec de la paraffine,

Travaux pratiques de chimie physique I
Fournier Coralie, Chappuis Emilie
Groupe E 08.10.2009
- 3 -
pour pouvoir mélanger correctement la solution et le tout est placé dans le spectromètre d’absorption. Ce
dernier est préalablement réglé à 400nm (zéro d’absorbance) grâce à une solution tampon de trypsine à pH 8.
L’absorbance et fonction du temps (durant 4 minutes) est alors mesurée pour chaque solution. Cela nous
permettra d’obtenir la vitesse de notre réaction.
1.4 Résultats
Tableau n°1 : Calcul des masses théoriques et des concentrations expérimentales
Solutions
Concentration
[S]
théorique
[mol/L]
Masse
théorique [g]
Masse
expérimentale
[g] ±0.0001 g
Concentration
[S]
expérimentale
[mol/L]
Concentration
[S] dans la
cuvette [mol/L]
A
0.0030
0.0029
0.0005
B
0.0050
0.0050
0.0008
C
0.0080
0.0082
0.0014
D
0.0120
0.0117
0.0020
E
0.0160
0.0164
0.0027
F
0.0200
0.0435
0.0425
0.0195
0.0033
G
0.0400
0.0870
0.0889
0.0409
0.0068
H
0.0500
0.1087
0.1077
0.0495
0.0083
Calcul utilisé pour la masse théorique :
Molaire MasseVolumeionConcentratMasse théoriquethéorique ⋅⋅=
Calcul utilisé pour la concentration expérimentale :
Molaire MasseVolume
Masse
ionConcentrat aleexpériment
aleexpériment ⋅
=
Avec : Volume = 0.005 L et Masse molaire(BAPNA) = 434.89 g/mol
Tableau n°2 : Calcul de la vitesse de formation des produits
Pente [Absorbance/min]
V0 [M/min]
1/[S] [M-1]
1/V0 [min/M]
0.025922
2.59E-06
2046.5412
3.86E+05
0.033230
3.32E-06
1211.3928
3.01E+05
0.054104
5.41E-06
733.7852
1.85E+05
0.055370
5.54E-06
511.6353
1.81E+05
0.075154
7.52E-06
366.8926
1.33E+05
0.068026
6.80E-06
306.9812
1.47E+05
0.089729
8.97E-06
146.7570
1.11E+05
0.087651
8.77E-06
121.1393
1.14E+05

Travaux pratiques de chimie physique I
Fournier Coralie, Chappuis Emilie
Groupe E 08.10.2009
- 4 -
Lineweaver - Burk plot
y = 147.91x + 94042
-5.0E+04
0.0E+00
5.0E+04
1.0E+05
1.5E+05
2.0E+05
2.5E+05
3.0E+05
3.5E+05
4.0E+05
4.5E+05
-1.0E+03 -5.0E+02 0.0E+00 5.0E+02 1.0E+03 1.5E+03 2.0E+03 2.5E+03
1/ [S]
1/ V0
Calcul utilisé pour déterminer V0 :
M/min en vitesse notre obtenons nous Ainsi
: avons Nous
min temps=tavec
: par donnéeest pente la que donnéeEtant
M ionconcentrat =c
cm 1 = l
cmM 10= :Avec
:Lambert - Beer de loi la par donnéeest absorbancel' de équationL'
1-1-4-
lvl
dt
dc
dt
dA
dt
dA
clA
⋅⋅=⋅⋅=
⋅⋅=
εε
ε
ε
0
Graphique n°1 :
Tableau n°3 : Détermination des constantes de Michaelis-Menten KM et Vmax :
Ordonnée [min/M]
9.4042E+04
Pente
147.9116
Vmax [M/min]
1.06E-05
X lorsque y=0
-635.8010
KM
1.5728E-03

Travaux pratiques de chimie physique I
Fournier Coralie, Chappuis Emilie
Groupe E 08.10.2009
- 5 -
Cinétique de Michaelis - Menten
0.0E+00
2.0E-06
4.0E-06
6.0E-06
8.0E-06
1.0E-05
1.2E-05
0.00 0.02 0.04 0.06 0.08 0.10
[S] mol/L
V0 [M/min]
Données
1/2Vmax
Vmax
Logarithmique (Données)
Calcul pour Vmax :
€
Vmax =1
Ordonnée à l'origine
Calcul pour x :
€
x=− Ordonnée à l'origine
pente
Calcul pour KM :
€
KM=−1
x
Graphique n°2 :
1.5 Discussion des résultats
Calculs d’erreur :
Tableau n°4 : Erreurs sur le matériel
Matériel
Erreur
Pipette de 1mL
±0.01
Pipette de 2mL
±0.02
Pipette de 5mL
±0.1
Ballon de 5mL
±0.08
Seringue de 0.5 mL
±0.005
 6
6
 7
7
 8
8
1
/
8
100%