Les effets secondaires de la morphine : lesquels prévenir

DOULEUR
a fréquence des différents effets secondaires des morphiniques
varie considérablement en fonction des doses, des voies d’ad-
ministration (per os, intrathécale, épidurale), ainsi que du mode
d’administration (traitement au long cours ou ponctuel). Les effets secon-
daires de la morphine constatés au cours des traitements pour des patholo-
gies non malignes sont identiques à ceux observés au cours de la prise en
charge de la douleur du cancer. Les effets indésirables les plus fréquents
sont la constipation, les nausées, les vomissements et la somnolence. Ces
effets sont dose-dépendants, et cèdent habituellement au cours des traite-
ments prolongés, à l’exception de la constipation (1). Les dérivés de la mor-
phine glucuroconjugués en 6 (métabolites actifs responsables de l’activité
antalgique) seraient, pour certains auteurs, plus particulièrement impliqués
dans la survenue des effets indésirables (2), mais cette hypothèse est contro-
versée (3). La plupart de ces effets secondaires sont bénins mais entraînent
malgré tout l’arrêt du traitement par le patient, celui-ci estimant qu’ils sur-
passent le bénéfice antalgique. La parfaite connaissance du déterminisme
des effets secondaires et leur explication précise aux patients avant traite-
ment sont donc essentielles, dès lors que l’on envisage un traitement mor-
phinique pour une douleur chronique non cancéreuse.
L
es effets secondaires de la morphine :
lesquels prévenir systématiquement,
et comment les prévenir ?
La Lettre du Rhumatologue - n° 254 - septembre 1999
mandé d’utiliser d’emblée une association de
laxatifs, avec mise à disposition dans ces pays
de comprimés contenant conjointement un
stimulant du péristaltisme et un émollient.
Certains auteurs (14) proposent d’ailleurs des
recommandations pratiques permettant une
meilleure gestion de la constipation liée aux
opioïdes, comprenant notamment un bilan
des selles initial (fréquence habituelle des
exonérations, utilisation habituelle des laxa-
tifs...), une surveillance journalière des selles,
la recommandation de boissons en quantité
suffisante (au moins 1,5 litre par jour), la pres-
cription immédiate, à titre prophylactique,
d’une association de laxatifs. Si cette asso-
ciation de laxatifs est mal tolérée, elle est rem-
placée par un laxatif de type osmotique (lac-
tulose, mannitol, sorbitol). D’autres
approches sont actuellement à l’étude, utili-
sant de la naloxone per os ou des antagonistes
Constipation
La constipation liée aux morphiniques est la
conséquence d’une diminution de la motilité
intestinale associée à une augmentation du
tonus de repos et à des spasmes (4, 5) [la
constipation est définie par un maximum de
deux selles spontanées par semaine avec un
sentiment de gêne ressenti par le patient].
Cette constipation est constante au cours des
traitements morphiniques et ne cède pas avec
la poursuite du traitement. Sa fréquence est
variable, selon les études et la coprescription
systématique de laxatifs (de 8 à 84 %) (6-12).
Même si différents laxatifs sont utilisés de
façon pragmatique, il n’existe aucune étude
contrôlée permettant de définir quelle est la
meilleure stratégie d’utilisation de ces laxa-
tifs. Les experts de l’ANDEM (13) ont pro-
posé des recommandations pour la prise en
charge de la douleur du cancer chez l’adulte
en médecine ambulatoire. La prescription
systématique de laxatifs oraux a été préconi-
sée de façon conjointe à toute prescription de
morphinique, dès la première prise. Ce trai-
tement laxatif est associé en pratique à des
mesures hygiéno-diététiques (maintien d’une
activité physique, augmentation des apports
liquidiens, apports alimentaires équilibrés,
conditions confortables et respect de l’inti-
mité du malade pour aller à la selle). Le type
de laxatif (émollient ou stimulant du péri-
staltisme) est déterminé par la consistance des
selles au cours de la surveillance clinique,
permettant ainsi de s’adapter à chaque situa-
tion. Dans les pays anglo-saxons, il est recom-
L
44
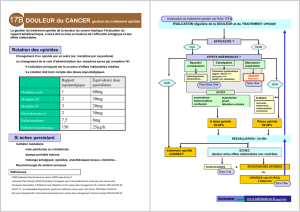
Prévention de la constipation
liée aux opioïdes (d’après 14).
!Bilan initial selles (fréquence exonéra-
tion ? usage préalable laxatifs ?)
!Surveiller selles et consistance (faire
noter)
!Encourager les apports hydriques
1,5 l/j (eau, soupes, jus de fruits) et les
fibres alimentaires
!Prescrire systématiquement un laxatif
par voie orale, voire une association de
deux laxatifs :
"Laxatifs de lest (ex. mucilages : Spagu-
lax®,Transilane®,Normacol®)
"Laxatifs osmotiques (ex. sucres et poly-
ols, lactulose ou lactitol : Importal®,Sor-
bitol®,Duphalac®)
"Laxatifs lubrifiants (huile de paraffine
ou Lansoÿl®,Transitol®)
"Laxatifs stimulants (anthracéniques :
Tamarine®,bisacodyl :Contalax®,docu-
sate sodique : Jamylène®)
!Adapter les posologies ou modifier le
type de laxatif après quelques jours

DOULEUR
opioïdes de quatrième génération sans pas-
sage hémato-encéphalique, avec des résultats
encourageants (15, 16).
Nausées, vomissements
La fréquence des nausées et vomissements
varie de 20 à 60 % selon les séries. Ils sont
liés principalement à la stimulation centrale
de la zone chémoréceptrice de l’area post-
rema avec réaction émétisante. Cette action
peut exister même à des doses faibles. La
stase gastrique induite par la fermeture du
pylore est un facteur associé accessoire. Ces
nausées et vomissements apparaissent habi-
tuellement en début de traitement, quelle
que soit la dose, et s’estompent en deux à
trois semaines. La prévention systématique
de cet effet indésirable n’est habituellement
pas recommandée, et il n’existe actuelle-
ment aucune étude contrôlée permettant
d’en définir le meilleur traitement curatif.
Deux stratégies curatives différentes ont été
proposées. Les experts de l’ANDEM ont
recommandé d’utiliser (selon le mécanisme
supposé être à l’origine des vomissements)
soit un neuroleptique d’action centrale
(halopéridol, chlorpromazine), soit un neu-
roleptique gastrokinétique (métoclopra-
mide, dompéridone) avec, en cas d’échec de
cette monothérapie, une association de deux
médicaments de mode d’action différent.
Les équipes anglo-saxonnes, quant à elles
(9), recommandent d’utiliser d’emblée de
l’halopéridol (neuroleptique d’action cen-
trale) 1 à 1,5 mg deux fois par jour avec, en
cas d’inefficacité, une substitution par un
neuroleptique gastrokinétique. Il faut
d’ailleurs noter que plusieurs études consa-
crées au traitement de cet effet secondaire
au cours de traitements morphiniques en
per- et postopératoire concluent à l’ineffi-
cacité du métoclopramide ou à une activité
inconstante (17-19).
Somnolence
Une asthénie et une somnolence sont surtout
observées en début de traitement. Ces signes
sont plus importants chez les patients insuf-
fisants hépatiques et/ou rénaux et chez les
patients âgés ou traités de façon conjointe par
des psychotropes. Cette somnolence régres-
serait habituellement après quelques jours si
la posologie est stable et adaptée à l’inten-
sité douloureuse. Malgré tout, un ralentisse-
ment cognitif pourrait persister, parfois non
perçu par le patient, si bien que certains
auteurs recommandent de signaler aux
patients le risque de troubles de la vigilance
au cours de la conduite automobile. Cepen-
dant, la prise au long cours de morphine n’af-
fecterait pas de façon statistiquement signi-
ficative les fonctions neuropsychologiques
utilisées au cours de la conduite automobile
(20).
Effets indésirables plus rares
!Les effets psychodysleptiques (dyspho-
rie, agitation, confusion, hallucinations)
seraient plus fréquents chez les sujets âgés,
même si cela reste controversé selon les
équipes. Ils seraient présents quelle que soit
la posologie, et il faut savoir interroger le
patient qui hésite à évoquer spontanément
ses cauchemars et hallucinations, cause d’ar-
rêt du traitement. Aucune étude curative
contrôlée n’est disponible dans cette indica-
tion, mais l’attitude pragmatique est de les
traiter par halopéridol avec diminution
momentanée des doses et recherche de fac-
teurs métaboliques favorisants. Il n’y a pas
de mesures préventives validées.
!Le prurit est un effet inexpliqué, souvent
bien toléré, plutôt remarqué par l’entourage,
qui serait plus fréquent chez l’enfant ou pour
la morphine épidurale. Les antihistaminiques
ne seraient pas efficaces dans cette indica-
tion. Différentes molécules (naloxone, dro-
péridol) seraient efficaces pour traiter le pru-
rit secondaire à la morphinothérapie
administrée par voie épidurale (21, 22).
!La dépression respiratoire serait excep-
tionnelle au cours des traitements morphi-
niques oraux prolongés, surtout si l’aug-
mentation des doses est progressive et que
les paliers sont respectés. En effet, la dépres-
sion respiratoire est habituellement dose-
dépendante et ne s’observe qu’en cas de sur-
dosage ou de toxicomanie associée.
!Les myoclonies sont rares et seraient trois
fois plus fréquentes en cas de traitement oral
par rapport au traitement par voie intravei-
neuse (3). La prescription de midazolam per-
mettrait la poursuite du traitement (23).
D’autres auteurs proposent la rotation des
opioïdes (c’est-à-dire la substitution d’un
opioïde fort à un autre) pour gérer cet effet
indésirable (24).
!La rétention urinaire serait plus fréquente
chez les sujets âgés ou en cas de fécalome
associé. Il convient de garder à l’esprit cet
effet indésirable, notamment en cas de confu-
sion chez un sujet âgé.
Au total
Les effets indésirables de la morphine utili-
sée dans les affections non cancéreuses méri-
tent d’être parfaitement connus par le rhu-
matologue et par le patient, qui devront en
avoir discuté ouvertement avant le début du
traitement. La prescription initiale de sulfate
de morphine devrait être de 30 mg/12 h, voire
de 10 mg/12 h si le sujet est âgé, insuffisant
rénal ou insuffisant hépatique. Certains
auteurs (6) préconisent cette dose initiale de
10 mg/12 h de façon systématique pour toute
morphinothérapie au long cours instaurée
chez un patient non cancéreux, et ce afin
d’éviter les effets secondaires dose-dépen-
dants et de permettre une meilleure adhésion
au traitement par le patient. Cette prescrip-
tion initiale doit être associée dès le premier
jour et pour toute la durée du traitement à des
mesures hygiéno-diététiques et à des laxatifs
per os. Les autres effets indésirables ne seront
pas prévenus de façon systématique et ils ne
seront traités qu’au moment de leur appari-
tion.
Par ailleurs, il faudra discuter l’arrêt du trai-
tement morphinique en présence d’effets
secondaires centraux au cours de ces patho-
logies non cancéreuses traitées au long cours.
1. Portenoy R.K. Opioid therapy for chronic non
malignant pain : a review of the critical issues.
J Pain Symp Manag 1996 ; 11 : 203-17.
2. Hagen N.A., Foley K.M., Cerbone D.J., Porte-
noy R.K., Inturisi C.E. Chronic nausea and mor-
phine-6-glucuronide. J Pain Symp Manag 1991 ;
6 : 125-8.
3. Tiseo P.J., Thaler H.T., Lapin J. et coll. Mor-
phine-6-glucuronide concentrations and opioid-
related side effects : a survey in cancer patients.
Pain 1995 ; 61 : 47-54.
4. Adler H.F., Atkinson A.J., Ivy A.C. Effect of
morphine and dilaudid on the ileum and of mor-
phine, dilaudid and atropine on the colon of man.
Arch Intern Med 1942 ; 69 : 974-85.
5.
Stewart J.J.,Weisbrodt N.W., Burks T.F. Central
and peripheral actions of morphine on intestinal
transit. J Pharmacol Exp Ther 1978 ; 205 : 547-
55.
6. Torres L.M. Management of non-oncological
pain with morphine. Clin Drug Invest 1997 ; 14
(suppl. 1) : 1-5.
La Lettre du Rhumatologue - n° 254 - septembre 1999
45
R.M. Javier
Service de rhumatologie,
hôpital de Hautepierre, Strasbourg.
Références bibliographiques

7. Portenoy R.K., Foley K.M. Chronic use of
opioid analgesics in non-malignant pain. Report
of 38 cases. Pain 1986 ; 25 : 171-86.
8. Portenoy R.K. Constipation in the cancer
patient : causes and management. Med Clin North
Am 1987 ; 71 : 303-11.
9. Twycross R.G. Opioids. In : Wall P.D., Mel-
zack R. Textbook of Pain, 3eed, pp 943-962, Edin-
burgh, Churchill Livingstone, 1994.
10. Ytterberg S.R., Mahowald M.L., Woods S.R.
Codeine and oxycodone use in patients with chro-
nic rheumatic disease pain. Arthritis Rheum
1998 ; 41 : 1603-12.
11. Pichard-Leandri E. Douleurs liées aux can-
cers. Prise en charge par les opioïdes. Presse Med
1997 ; 26 : 1746-55.
12. Jamison R.N., Raymond S.A., Slawsby E.A.,
Nedeljkovic S.S., Katz N.P. Opioid therapy for
chronic non cancer back pain. Spine 1998 ; 23 :
2591-600.
13. Recommandations pour la prise en charge de
la douleur du cancer chez l’adulte en médecine
ambulatoire. Publication de l’Agence Nationale
pour le Développement de l’Evaluation Médicale
- ANDEM, 1995, 153 p.
14. Twycross R.G., Harcourt J.M.V. The use of
laxatives at a palliative care centre. Palliative Med
1991 ; 5 : 27-33.
15.
Yuan C.S., Foss J.F., Osinski J. et coll. The
safety and efficacy of oral methylnaltrexone in pre-
venting morphine-induced delay in oral-cecal tran-
sit time. Clin Pharmacol Ther 1997 ; 61 : 467-75.
16. Sykes N.F. An investigation of the ability of
oral naloxone to correct opioid-related constipa-
tion in patients with advanced cancer. Palliative
Med 1996 ; 10 : 135-44.
17. Freedman G.M., Kreitzer J.M., Reuben S.S.,
Eisenkraft J.B. Improving patient-controlled anal-
gesia : adding droperidol to morphine sulfate to
reduce nausea and vomiting and potentiate anal-
gesia. Mount Sinai J Med 1995 ; 62 : 221-5.
18. Cohen S.E., Woods W.A., Wyner J. Antieme-
tic efficacy of droperidol and metoclopramide.
Anesthesiology 1984 ; 60 : 67-9.
19. Rowbotham D.J., Bamber P.A., Nimmo W.S.
Comparison of the effect of cisapride and meto-
clopramide on morphine-induced delay in gastric
emptying. Br J Chir Pharmacol 1988 ; 26 : 741-6.
20. Vainio A., Ollila J., Matikainen E., Rosen-
berg P., Kalso E. Driving ability in cancer patients
receiving long-term morphine analgesia. Lancet
1995 ; 34, 6 : 667-70.
21. Kendrick W., Woods A., Daly M., Birch R.,
Difazio C. Naloxone versus nalbuphine infusion
for prophylaxis of epidural morphine-induced
pruritus. Anesth Analg 1996 ; 82 : 641-7.
22. Horta M.L., Ramos L., Goncalves Z.R. et coll.
Inhibition of epidural morphine-induced pruritus
by intravenous droperidol. The effect of increa-
sing the doses of morphine and of droperidol.
Regional Anesthesia 1996 ; 21 : 312-7.
23. Holdsworth M.T., Adams V.R., Chavez C.M.,
Vaughan L.J., Duncan M.H. Continuous midazo-
lam infusion for the management of morphine-
induced myoclonus. Ann Pharmacother 1995 ;
29 : 25-9.
24. Paix A., Coleman A., Lees J. et coll. Subcu-
taneous fentanyl and sufentanil infusion substitu-
tion for morphine intolerance in cancer pain
management. Pain 1995 ; 63 : 263-9.
La Lettre du Rhumatologue - n° 254 - septembre 1999
46
DOULEUR
“M
ieux comprendre la douleur pour mieux agir
”.
1
/
3
100%