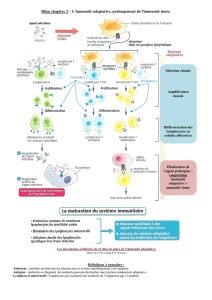
Les récepteurs de l`immunité innée

Immunité naturelle
versus
Immunité acquise ou adaptative
Définition (tentative) :réactions immunitaires qui fonctionnent
sans connaissance préalable et spécifique de l’Ag.
Autrefois considérée comme
•« non spécifique », (concept à préciser)
• première ligne de défense en attendant que l’immunité acquise
• s’installe
•faisant appel à des mécanismes « passifs », mécaniques et chimiques
Phylogénétiquement la plus ancienne (invertébrés et même plantes.

Aujourd’hui, l’immunité naturelle :
Est bien une première phase de défense, en attendant la mise en jeux
de l’immunité adaptative, immunité qu’elle induit et qu’elle pilote
pour la meilleure adaptation au type de l’agression
«L’immunité adaptative brûle au feux de l’immunité innée »

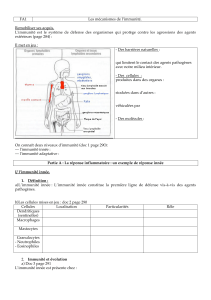
Evolution d’une maladie infectieuse bégnine
temps
Contamination
virale
incubation
Symptomes
Lésions tissulaires virales
Réaction inflammatoire
Immunité innée
Immunité acquise
05 -10
Restitutio
ad
integrum

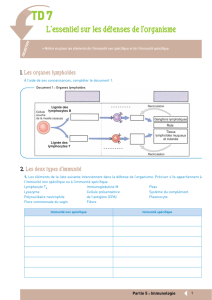
Un double système,cellulaire
et moléculaire
de reconnaissance
de l’antigène
CD3
TCR
MHC
T cell B cell
BcR
= immunoglobulines
Organe de différenciation thymus Bourse de Fabricius
Ou moelle osseuse
Récepteurs clonaux
Antigène (protéine bactérienne)
Antigène entier
Peptide issu de l’antigène
Cellule
souche

Tolérance
au soi
Délétion clonale
Spécificité
pré-établie
Mémoire
Persistance clonale
1°) clonalité de la réponse spécifique :
régulations Ag par Ag
I - Les grands principes classiques (1955 –1980)
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
 37
37
 38
38
 39
39
 40
40
 41
41
 42
42
 43
43
 44
44
 45
45
 46
46
 47
47
 48
48
 49
49
 50
50
 51
51
1
/
51
100%