Place des analyses toxicologiques

Place de l’analyse toxicologique
au cours des intoxications aiguës -
Relations pharmacocinétiques et pharmacodynamiques
Bruno Mégarbane
Réanimation Médicale et Toxicologique,
INSERM U705 - CNRS, UMR 7157 , Université Paris 7,
Hôpital Lariboisière, Paris

Épidémiologie des intoxications aiguës
Intoxication aiguë : une des premières causes d’hospitalisation et de
mortalité des sujets jeunes.
Une intoxication se définit comme grave :
• Des symptômes présentés (coma, convulsions, détresse respiratoire,
hypoventilation alvéolaire, instabilité hémodynamique ou troubles du rythme ou
de conduction cardiaque).
• Devant la nécessité d’une surveillance rapprochée, en raison de la quantité
importante de substance à laquelle le sujet a été exposé.
• Du terrain sous-jacent (co-morbidités lourdes, âge très avancé ou nourrisson).
Conférence d’Experts SRLF 2006

• La prise en charge d'une intoxication est essentiellement
symptomatique et repose avant tout sur l'approche clinique
(anamnèse et toxidromes).
• Le bilan biologique prime toujours sur l'analyse toxicologique.
[Accord fort]
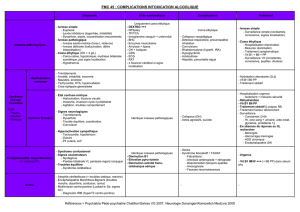
Place des analyses toxicologiques
Conférence d’Experts SRLF 2006

•Intoxication alcoolique
•Ethylène glycol
•Anti-rouille
(acide fluorhydrique)
•Cyanure
•Antivitamines K
•Organophosphorés
•Sels de fer
Intoxication Analyse biologique Analyse toxicologique
Glycémie
pH artériel
et trou anionique
Calcémie
Lactacidémie
Taux de prothrombine
Cholinestérases globulaires
Sidérémie
Ethanolémie
Ethylène glycol plasmatique
Fluorure sanguin
Cyanure sanguin
-
-
-
Place de la biochimie toxicologique
Erickson TB. Emerg Med Clin North Am 2007

Acquisition
d’un signal
Interprétation
- Diagnostic
- Pronostic
- Thérapeutique
Intérêt
de l’analyse
Prélèvements
Sang/plasma
Urine
Liquide Gastrique
Mais aussi :
Salive
Sueur
Cheveux
Détection
Séparation
+
Détection
Quantification
Qu’est-ce une analyse toxicologique ?
x
xxxx
Urines
Sang
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
 37
37
 38
38
 39
39
1
/
39
100%