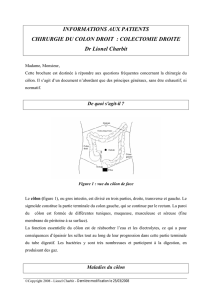
Répartition des malades selon le motif d`hospitalisation

0

1
Plan
INTRODUCTION ....................................................................................................... 6
HISTORIQUE ............................................................................................................ 8
OBJECTIFS DE L'ETUDE ........................................................................................... 11
1. Objectif général : ........................................................................................... 12
2. Objectifs spécifiques : .................................................................................... 12
METHODOLOGIE .................................................................................................... 13
1. Le type de l‘étude : ......................................................................................... 14
2. Le cadre de l‘étude : ....................................................................................... 14
3. La période de l‘étude : .................................................................................... 14
4. La population étudiée : ................................................................................... 14
4-1. Les critères d‘inclusion : .......................................................................... 14
4-2. Les critères de non inclusion : .................................................................. 14
5. Les supports des données : ............................................................................ 15
6. Analyse statistique : ....................................................................................... 15
7. Limites : ......................................................................................................... 16
RESULTATS ........................................................................................................... 17
1. Effectifs des malades par année : .................................................................... 18
2. Répartition des malades selon l‘âge : ............................................................. 18
3. Le sexe : ........................................................................................................ 19
II Les données cliniques : .................................................................................. 20
1. Les antécédents médicaux : ......................................................................... 20
1-1. Eléments de comorbidité ...................................................................... 20
1-2. Facteurs de risque : .............................................................................. 20
2. Les antécédents chirurgicaux : .................................................................... 21
3. Le motif d‘hospitalisation : .......................................................................... 22

2
4. Etat clinique à l‘admission : ......................................................................... 23
4-1. Poids /IMC : .......................................................................................... 23
4-2. Etat général à l‘admission et perte de poids : ........................................ 24
4-3. Le toucher rectal ................................................................................... 24
4-4. Adénopathies périphériques : ............................................................... 24
4-5. Hépatomégalie ou splénomégalie : ........................................................ 25
III. Les données paracliniques : ........................................................................... 25
1. L‘endoscopie : ............................................................................................. 25
1-1. Siège de la tumeur : .............................................................................. 25
1-2. La taille de la tumeur : .......................................................................... 26
1-3. Aspect macroscopique de la tumeur :.................................................... 27
1-4. Le nombre des tumeurs : ...................................................................... 27
1-5. L‘anatomie pathologique : .................................................................... 27
2. Autres : ....................................................................................................... 28
3. La TDM : ..................................................................................................... 28
3-1. Extension tumorale ............................................................................... 28
3-2. Statut ganglionnaire : .......................................................................... 28
3-3. Métastases à distance : ......................................................................... 29
4. Dosage des marqueurs tumoraux : .............................................................. 29
IV- Classification TNM : ...................................................................................... 30
V. Le traitement chirurgical : .............................................................................. 33
1. La voie d‘abord : ......................................................................................... 33
2. Type d‘intervention : ................................................................................... 34
3. Autres interventions : .................................................................................. 34
4. La durée de l‘intervention : .......................................................................... 35
5. Délais entre l‘acte opératoire et la reprise du transit : .................................. 36
6. Séjour en réanimation : ............................................................................... 38

3
7. La durée du séjour hospitalier : ................................................................... 38
7-1. La durée totale : ................................................................................... 38
8. La durée postopératoire : ............................................................................ 41
VI. L‘anatomie pathologique de la pièce opératoire : ........................................... 42
VII. Les complications per-opératoires : ............................................................. 43
1. Pour le premier groupe ayant bénéficié d‘une cœlioscopie : ......................... 43
2. Pour le deuxième groupe ayant bénéficié d‘une laparotomie : ..................... 44
VIII. Les complications post opératoires : ............................................................ 45
IX. Mortalité : .................................................................................................... 47
DISCUSSION .......................................................................................................... 49
I- Evaluation préopératoire et sélection des malades : ........................................ 50
1-Age : ........................................................................................................... 50
2-Etat cardio-pulmonaire : .............................................................................. 51
3-Obésité : ..................................................................................................... 52
4-Caractère de la tumeur : .............................................................................. 54
5-les adhérences : .......................................................................................... 55
6-localisation : ................................................................................................ 56
II-Préparation du patient : .................................................................................. 57
1-Le bilan préopératoire : ............................................................................... 57
2-Préparation colique : .................................................................................... 58
3-Immunonutrition préopératoire : .................................................................. 59
4-Prévention thromboembolique : ................................................................... 60
III- Anesthésie pour chirurgie colorectale sous laparoscopie : ............................. 60
1. Choix des agents anesthésiques : ................................................................ 61
2. Installation : ................................................................................................ 62
3. Monitorage : ................................................................................................ 63
VI-Techniques opératoires : ............................................................................... 63

4
1-Installation du patient et conditionnement : ................................................. 63
2-Temps opératoires ...................................................................................... 66
2-1 Création du pneumopéritoine : .............................................................. 66
2-2 Position des trocarts : ............................................................................ 67
2-3 Localisation de la tumeur: ...................................................................... 69
2-4 Dissection du mésocôlon et mobilisation du segment du côlon atteint :.. 70
2-5 Différents types de colectomies : .......................................................... 72
2-6 Anastomose colorectale : ....................................................................... 77
V-Résultats per-opératoires de la laparoscopie : ................................................ 80
1-Taux de conversion : ................................................................................... 80
2-Durée opératoire : ....................................................................................... 83
3-Qualité de résection : ................................................................................... 85
VI-Avantages de la cœlioscopie dans la chirurgie colique : .................................. 87
1-A court terme : ............................................................................................ 87
1-1 Douleurs postopératoires ....................................................................... 87
2-2 Iléus postopératoire ............................................................................... 88
2-3 Les pertes sanguines : ........................................................................... 89
2-4 Fonction respiratoire postopératoire ...................................................... 90
2-5 Fonction immunitaire : ........................................................................... 91
2-6 Durée d‘hospitalisation : ........................................................................ 92
2-7 Morbidité postopératoire : ..................................................................... 94
2-8. Mortalité ............................................................................................... 94
2 A long terme : .............................................................................................. 95
2-1 Survie : .................................................................................................. 95
2-2 Dissémination néoplasique aux orifices de trocarts : .............................. 95
VII. Complications opératoires : .......................................................................... 99
1. Complications peropératoire :...................................................................... 99
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
 37
37
 38
38
 39
39
 40
40
 41
41
 42
42
 43
43
 44
44
 45
45
 46
46
 47
47
 48
48
 49
49
 50
50
 51
51
 52
52
 53
53
 54
54
 55
55
 56
56
 57
57
 58
58
 59
59
 60
60
 61
61
 62
62
 63
63
 64
64
 65
65
 66
66
 67
67
 68
68
 69
69
 70
70
 71
71
 72
72
 73
73
 74
74
 75
75
 76
76
 77
77
 78
78
 79
79
 80
80
 81
81
 82
82
 83
83
 84
84
 85
85
 86
86
 87
87
 88
88
 89
89
 90
90
 91
91
 92
92
 93
93
 94
94
 95
95
 96
96
 97
97
 98
98
 99
99
 100
100
 101
101
 102
102
 103
103
 104
104
 105
105
 106
106
 107
107
 108
108
 109
109
 110
110
 111
111
 112
112
 113
113
 114
114
 115
115
 116
116
 117
117
 118
118
 119
119
 120
120
 121
121
 122
122
 123
123
 124
124
 125
125
 126
126
 127
127
 128
128
 129
129
 130
130
 131
131
 132
132
 133
133
 134
134
 135
135
 136
136
 137
137
 138
138
 139
139
 140
140
 141
141
 142
142
 143
143
 144
144
 145
145
 146
146
 147
147
 148
148
1
/
148
100%