Travaux Pratiques de Chimie Première S 1 ) Protocole expérimental

Travaux Pratiques de Chimie Première S
TP10_oxyalcool_tests Page 1 sur 1
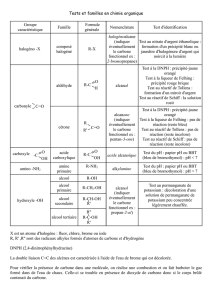
PASSAGE D’UN GROUPE CARACTERISTIQUE A UN AUTRE : ALCOOLS, ALDEHYDES, CETONES
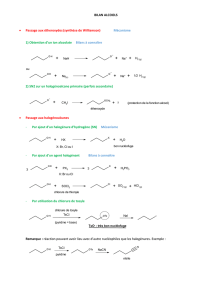
I ) Oxydation des différentes classes d’alcools : cas de l’oxydant en défaut
1 ) Protocole expérimental :
Principe : On mélange un alcool (primaire, secondaire ou tertiaire) avec une solution oxydante. L'objectif est de
comparer le pouvoir réducteur des différentes classes d'alcools et d'identifier les produits formés lorsqu'une
oxydoréduction a lieu.
La solution oxydante utilisée est une solution acidifiée de permanganate de potassium (K+ + MnO4-) à 0,05 mol.L-1.
Le couple oxydoréducteur concerné est le couple MnO4-/Mn2+.
Les ions MnO4- sont violets cependant que les ions Mn2+ sont incolores.
On dispose de butan-1-ol, de butan-2-ol et de 2-méthylpropan-2-ol.
Donner les formules semi-développée et topologiques de chacun de ces alcools et en déduire leur classe.
Pour chacun de ces alcools, préparer le mélange réactionnel suivant : 1 mL d’alcool + 2 mL d’eau + 1 mL
d’oxydant. Placer celui-ci dans des tubes à essais numérotés munis de tube réfrigérant.
Que conclure d’une première observation ?
Afin d’accélérer la réaction, laisser le mélange au bain-marie pendant environ 20 à 30 minutes. Pendant cette
attente, réaliser les tests de caractérisation des aldéhydes et des cétones (§II)
2 ) Extraction des produits de la réaction :
Sortir le mélange réactionnel du bain-marie à l’aide de la pince de bois et le refroidir sous le robinet d’eau froide.
Le cyclohexane est un bon solvant des produits organiques insolubles dans l'eau : il ne réagit pas avec les produits
utilisés dans les tests du II donc ne les fausse pas.
En verser environ 5 mL dans chaque tube à essai ; boucher à l’aide du tube réfrigérant, agiter puis laisser reposer.
On voit se séparer deux phases, l’une aqueuse contenant les substances colorées, et l’autre organique qui surnage.
3 ) Identification des produits formés :
Les tests de caractérisation seront réalisés sur la phase organique. Prélever à l’aide d’une pipette simple quelques
gouttes de cette phase organique et les verser dans chacun des deux réactifs. Compléter le tableau ci-dessous :
Test des produits formés à
partir du:
butan-1-ol butan-2-ol 2-méthylpropan-2-ol
2,4-DNPH Positif / Négatif Positif / Négatif Positif / Négatif
Liqueur de Fehling Positif / Négatif Positif / Négatif Positif / Négatif
famille chimique obtenue
4 ) Conclusions :
Conclure sur l’oxydation ménagée (oxydant en défaut par rapport à l’alcool) des trois classes d’alcools.
Donner les formules semi-développée et topologiques de chacun des produits formés.
Ecrire les équations bilans des réactions d’oxydoréductions en ayant pris soin d’écrire les deux demi-équations.
II ) Oxydation des différentes classes d’alcools : cas de l’oxydant en excés
On prépare au début de la séance trois erlenmeyers contenant respectivement 1 mL de chaque alcool. On ajoute
alors 20 mL de la solution oxydante à 0,5 mol.L-1 , donc dix fois plus concentrée qu’en II. On bouche et on agite.
Lorsque les I et III sont terminés, tirer les conclusions d’une première observation.
Suite à ces conclusions, on ajoute dans les erlenmeyers des alcools primaire et secondaire, 10 mL de cyclohexane.
On agite et on laisse décanter. On prélève la phase supérieure de nouveau et on pratique les mêmes tests qu’en I.
Répondre aux mêmes questions qu’en I. 4).

Travaux Pratiques de Chimie Première S
TP10_oxyalcool_tests Page 2 sur 2
III ) Tests d’identification des aldéhydes et des cétones :
1 ) Test à la DNPH : Ajouter quelques gouttes de composé à tester
Verser d’abord la DNPH ; sous hotte si possible
2 mL de DNPH
2 ) Test à la liqueur de Fehling :
Ajouter 1 mL de composé à tester
Mettre le tube dans un bain-marie.
2 mL de liqueur de Fehling
3 ) Test au réactif de Tollens :
Agiter. Placer le tube dans un bain-marie
2 mL de réactif de Tollens
4 ) Test au réactif de Schiff :
1 mL de réactif de Schiff placé dans la glace pilée.
5 ) Récapitulatif :
Les produits à testés sont indiqués dans le tableau.
Réactif Aldéhyde : éthanal Cétone : propanone
2,4-DNPH Positif / Négatif Positif / Négatif
Liqueur de Fehling Positif / Négatif Positif / Négatif
Réactif de Tollens Positif / Négatif Positif / Négatif
Réactif de Schiff Positif / Négatif Positif / Négatif
Ajouter 1 mL de composé à tester
1
/
2
100%