Mise au point clinique L`amylose cardiaque

16:00:20:04:12
Page 165
Page 165
Mise au point clinique
L’amylose cardiaque
Une affection curable au diagnostic trop souvent négligé
Rodney H. Falk, MD
Observation clinique : une femme de
55 ans, jusqu’alors physiquement
très active, a noté que sa tolérance à
l’effort avait progressivement diminué
au cours des trois ou quatre derniers
mois au point de devoir reprendre son
souffle chaque fois qu’elle gravit des
escaliers. Il y a six mois de cela, elle
a consulté un dermatologue pour
de petites ecchymoses palpébrales
récidivantes, sans qu’aucune cause
n’ait été identifiée. Un ECG montre
des signes en faveur d’un infarctus du
myocarde ancien ainsi qu’un axe
cardiaque orienté de manière peu
courante (Figure 1) et, lors d’une
consultation cardiologique, l’écho-
cardiographie met en évidence une
hypertrophie ventriculaire gauche
symétrique sans altération de la frac-
tion d’éjection ventriculaire gauche,
des valves cardiaques fonctionnant
normalement et une légère hyper-
trophie ventriculaire droite. La
patiente ne présente aucun antécédent
familial de trouble cardiovasculaire
ou neurologique. L’examen physique
objective une discrète élévation de la
pression veineuse jugulaire, des bruits
du cœur normaux, une absence de
souffle cardiaque, un discret œdème
périphérique, des champs pulmonaires
clairs et une légère congestion hépa-
tique. La pression artérielle est de
110/65 mmHg. Il existe une protéinurie
de grade 1+. L’électrophorèse des
protéines sériques ne montre pas
de bande anormale, mais l’immuno-
fixation sérique décèle la présence d’un
pic d’immunoglobine monoclonale qui
se révèle être une IgGλ. Une biopsie
médullaire est pratiquée, qui met
en évidence 5 à 10 % de plasmocytes
d’un même type prenant la coloration
caractéristique des chaînes légères λ.
Le dosage des chaînes légères libres
montre une augmentation du taux
d’éléments λ libres et un rapport
κ/λ anormal. Le taux de peptide
natriurétique de type B est de 1 019
pg/ml (la normale se situant en dessous
de 100 pg/ml) et celui de troponine I
de 0,07 ng/ml (taux normalement
inférieur à 0,01 ng/ml). La biopsie
endomyocardique (Figure 2) révèle
la présence de matériel extracellulaire
amorphe prenant la coloration au
rouge Congo et au bleu Alcian sulfaté
et qui, en immunohistochimie, réagit
aux anticorps anti-chaînes légères λ
mais non à ceux dirigés contre les
chaînes κ, AA et de la transthyrétine.
Le diagnostic d’amylose de type AL
(c’est-à-dire à chaînes légères) à IgGλ
est dès lors porté.
Les amyloses constituent un
groupe de maladies caractérisées par
l’accumulation extracellulaire d’un
matériel protéinique appelé substance
amyloïde. Ces dépôts résultent du
mauvais repliement d’un précurseur
protéique, dont les types les plus
fréquents sont les chaînes légères, la
transthyrétine et l’amyloïde A sérique.1
Bien que la microscopie optique
ou électronique ne permette pas de
déterminer quel est le précurseur
protéique à l’origine des dépôts
observés, un typage précis peut
être réalisé en ayant recours à des
colorations spécifiques, ce qui est
indispensable à l’instauration du
traitement approprié (en écartant ainsi
les approches inadaptées). L’amylose
est une affection systémique qui peut
affecter de multiples organes (dont le
cœur), la sévérité du trouble au niveau
d’un organe donné variant selon le
précurseur protéique en cause. Les
Tableaux 1 et 2 décrivent les formes
d’amylose les plus courantes. Nous
nous limiterons ici aux amyloses AL
et à transthyrétine, qui sont les deux
formes les plus fréquemment observées
en pratique clinique.
L’amylose AL
La patiente qui nous occupe est
atteinte d’amylose AL. Il s’agit d’une
dyscrasie plasmocytaire étroitement
apparentée au myélome multiple, mais
qui en est généralement distincte.
Environ 2 000 nouveaux cas d’amylose
AL sont annuellement enregistrés aux
Etats-Unis, dont environ la moitié
comporte une atteinte cardiaque
marquée. L’âge médian d’apparition
du trouble se situe vers 55 à 60 ans. Les
principaux organes communément
affectés par l’amylose AL sont les reins
(l’affection se manifestant générale-
ment par une importante protéinurie),
le cœur, les nerfs (neuropathie péri-
phérique et syndrome neurovégétatif),
le tractus digestif (amaigrissement,
troubles du transit) et le foie (élévation
des phosphatases alcalines sans modi-
fication des transaminases, les formes
ictériques étant rares). La fragilité
capillaire occasionnée par les dépôts de
substance amyloïde est cause de
l’apparition de lésions cutanées
purpuriques au moindre choc ainsi que
Programme d’étude de l’amylose cardiaque, Brigham and Women’s Hospital et Harvard Vanguard Medical Associates, Boston, Massachusetts,
Etats-Unis.
Le supplément de données uniquement disponible en ligne peut être consulté, tout comme la version anglaise de cet article, sur le site :
http://circ.ahajournals.org/lookup/suppl/doi:10.1161/CIRCULATIONAHA.110.010447/-/DC1.
Correspondance : Rodney H. Falk, MD, Department of Cardiology, Harvard Vanguard Medical Associates, 133 Brookline Ave, Boston MA 02215,
Etats-Unis.
E-mail : rfalk@partners.org
(Traduit de l’anglais : Cardiac Amyloidosis; A Treatable Disease, Often Overlooked. Circulation. 2011;124:1079–1085.)
© 2011 American Heart Association, Inc.
Circulation est disponible sur le site http://circ.ahajournals.org
165

16:00:20:04:12
Page 166
Page 166
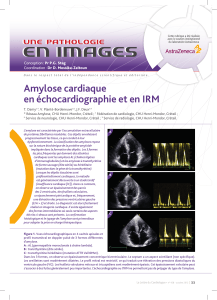
Figure 1. Tracé électrocardiographique du cas décrit. Celui-ci fait apparaître un faible voltage limite dans les dérivations périphériques et une
déviation axiale droite extrême. Il existe également des extrasystoles auriculaires et, bien que le voltage des dérivations précordiales soit
normalement conservé, celles-ci montrent une très médiocre progression des ondes R, ce qui est en faveur d’un infarctus du myocarde
ancien (les artères coronaires épicardiques étaient normales).
d’un purpura périorbitaire (comme
cela est le cas chez la patiente dont il
est ici question).
Le pronostic de l’amylose AL
dépend du nombre d’organes affectés
et de la sévérité de leur atteinte ; la
localisation cardiaque est celle dont le
pronostic est le plus sombre, la durée
médiane de survie chez un patient non
traité étant d’environ 6 mois à compter
de l’installation de l’insuffisance
cardiaque congestive.2 Dans l’amylose
cardiaque de type AL, le décès est
secondaire à l’aggravation progressive
de l’insuffisance cardiaque ou revêt
la forme d’une mort subite. Celle-ci est
le plus souvent la conséquence d’une
asystolie ventriculaire ou d’une dis-
sociation électromécanique, la pose
d’un défibrillateur dans un but pré-
ventif n’étant que rarement efficace.3
Les signes électrocardiographiques
peuvent orienter à tort vers une coro-
naropathie. Il arrive fréquemment
que le diagnostic d’amylose ne soit
porté qu’avec beaucoup de retard, car,
face à la normalité de la coronaro-
graphie, le médecin juge inutile de
poursuivre les investigations plus
avant. L’épaississement de la paroi
myocardique mis en évidence par
l’échocardiographie dans l’amylose
cardiaque symptomatique est souvent
faussement assimilé à une «hyper-
trophie » (comme dans le cas présent),
ce qui conduit à formuler un diagnostic
erroné de cardiopathie hypertensive ou
de cardiomyopathie hypertrophique.
En réalité, l’épaississement pariétal
décrit dans l’amylose résulte d’un
infiltrat et, contrairement à ce que l’on
observe dans l’hypertrophie ventricu-
laire gauche vraie, à savoir une aug-
mentation du voltage des complexes
électrocardiographiques, dans l’amy-
lose le voltage est diminué, ce qui est
fortement en faveur d’une affection
myocardique infiltrante.4 Les signes
échocardiographiques caractéristiques
sont décrits dans la Figure 3 et dans les
clips vidéo inclus dans le supplément
de données uniquement disponible
en ligne. Outre l’échocardiographie,
l’imagerie par résonance magnétique
cardiaque contribue utilement au
diagnostic de l’amylose cardiaque en
objectivant un aspect relativement spé-
cifique de rehaussement diffus tardif
myocardique sous-endocardique après
injection de gadolinium (Figure 4) et
un ralentissement de la disparition
des images contrastant avec une élim-
ination accélérée du gadolinium du
courant circulatoire et du myocarde.5
Le précurseur protéique en cause
dans l’amylose AL est un fragment
d’immunoglobuline monoclonale.
L’immunofixation des protéines
sériques et urinaires met en évidence
une bande monoclonale anormale
dans près de 90 % des cas. La protéine
monoclonale est généralement
présente à un taux nettement inférieur
à celui observé dans le myélome
multiple. C’est pourquoi l’on ne peut
s’en remettre à la seule électrophorèse
des protéines sériques et urinaires pour
confirmer une suspicion d’amylose
AL. Le dosage des chaînes légères
libres est un test quantitatif dont le
résultat est anormal dans plus de 95 %
des cas. Chez un patient présentant une
suspicion d’amylose cardiaque ou
reconnu atteint d’une telle affection
au vu des données de l’examen biop-
sique, un excès de chaînes λ (ou plus
rarement κ) oriente préférentiellement
vers une amylose AL.
L’amylose cardiaque à
transthyrétine
L’amylose cardiaque peut également
être causée par l’accumulation de
substance amyloïde secondaire à une
mutation de la transthyrétine, une
166 Circulation Mai 2012

16:00:20:04:12
Page 167
Page 167
Figure 2. Biopsie endomyocardique. A, la coloration à l’hématoxyline-éosine met en
évidence la présence d’un matériel extracellulaire amorphe rose-clair séparant les
myocytes, dont la coloration est plus intense. Bien que compatible avec le diagnostic de
dépôts amyloïdes, cet aspect demande à être approfondi par l’emploi de colorations plus
spécifiques. La coloration au rouge Congo (non présentée) était positive ; le bleu Alcian
sulfaté (B) colore les dépôts amyloïdes en bleu turquoise et les myocytes en jaune.
L’immunocoloration des dépôts amyloïdes aux anticorps anti-λ était fortement positive
(coloration verte en C), alors que les colorations faisant appel aux autres types d’anticorps
étaient négatives, confirmant par là même le diagnostic d’amylose AL. (Figure
gracieusement prêtée par le Dr Gayle Winters, du Service d’Anatomopathologie du Brigham
and Women’s Hospital.)
protéine synthétisée par le foie. La
transthyrétine est une petite protéine
composée de 127 acides aminés.
Plus d’une centaine de mutations
ponctuelles ont été décrites, dont la
plupart sont pourvoyeuses d’amylose.
La transthyrétine mutée tend à former
des monomères instables qui, du fait de
leur repliement incorrect, provoquent
des dépôts amyloïdes siégeant
préférentiellement au niveau du cœur
et du système nerveux. L’atteinte de ce
dernier se traduit par une neuropathie
sensorimotrice progressive, à laquelle
vient fréquemment s’ajouter un
syndrome neurovégétatif de degré
variable. Etonnamment, l’insuffisance
cardiaque congestive peut être minime,
voire absente, même en cas de
dépôts intracardiaques massifs. Cette
observation a conduit à considérer que
l’insuffisance cardiaque congestive
rapidement progressive observée dans
l’amylose AL a une composante
toxique liée à la circulation des chaînes
légères libres, alors que l’amylose à
la transthyrétine est essentiellement
une cardiomyopathie infiltrante.6 La
propension des chaînes légères à
induire une amylose a été par la
suite confirmée par des études
animales.7
Un variant de la transthyrétine est
particulièrement fréquent chez les
individus d’origine africaine. Environ
4 % des Afro-américains sont hétéro-
zygotes pour une substitution de la
valine par l’isoleucine en position 122.
Cette mutation est à l’origine d’une
amylose cardiaque qui débute vers
la fin de la soixantaine et se carac-
térise par une insuffisance cardiaque
congestive progressive s’accompagnant
assez fréquemment d’une insuffisance
tricuspidienne cliniquement significa-
tive.8 La neuropathie est rare mais peut
survenir à un stade tardif de la maladie ;
de plus, contrairement à ce que l’on
observe dans l’amylose systémique
sénile, elle touche communément la
femme. La constatation troublante de
ce que le pourcentage d’individus
présentant une isoleucine en position
122 est plus élevé dans les essais
cliniques sur l’insuffisance cardiaque
que dans la population générale9
conduit à se demander si cette muta-
tion ne contribuerait pas au dévelop-
pement d’autres formes d’insuffisance
Falk L’amylose cardiaque 167

16:00:20:04:12
Page 168
Page 168
Tableau 1. Principaux types d’amyloses
Type
Précurseur
protéique Organes cibles
Principaux moyens
diagnostiques Traitement
AL Chaînes
légères
Rein
Cœur
Système nerveux
Tractus digestif
et foie
Téguments
Immunofixation des
protéines sériques
et urinaires
Chaînes légères libres
Biopsie médullaire
Chimiothérapie
dirigée contre
les plasmocytes
ATTR Transthyrétine
mutée
Système nerveux
Cœur
Absence d’anomalie
de type AL
Dépistage génétique
positif de la
transthyrétine mutée
Transplantation
hépatique
Traitements
expérimentaux
visant à stabiliser
la transthyrétine
SSA Transthyrétine
de type
sauvage
Cœur Absence d’anomalie
de type AL
Dépistage génétique
négatif
Traitements
expérimentaux
visant à stabiliser
la transthyrétine
AA Amyloïde A
sérique
Rein
Foie
Néant Traitement de
l’inflammation
sous-jacente
AANF Facteur
natriurétique
atrial
Oreillette Néant Néant
cardiaque, peut-être en induisant la
formation de petits dépôts amyloïdes.
De faibles quantités de substance
amyloïde peuvent être décelées dans les
ventricules de 50 à 80 % des individus
âgés de plus de 80 ans. Ces dépôts ont
généralement pour origine une trans-
thyrétine de type sauvage et n’ont pas
ou que peu de conséquences cliniques.
En revanche, l’accumulation myo-
cardique massive de substance amy-
loïde issue de ce même type sauvage,
qui est toutefois relativement rare,
provoque une insuffisance cardiaque
congestive progressive et constitue
le syndrome désigné sous le nom
d’amylose cardiaque sénile (ou
amylose systémique sénile). Pour des
raisons inexpliquées, ce trouble frappe
principalement les hommes, générale-
ment au-delà de 70 ans, le rapport
hommes/femmes étant de l’ordre de
20/1.10 Alors que l’autopsie des patients
atteints d’amylose systémique sénile
met en évidence l’existence de dépôts
pulmonaires, l’accumulation rénale de
substance amyloïde est très rare dans
cette forme de la maladie et l’amylose
à la transthyrétine de type sauvage
Tableau 2. Eléments différenciant l’amylose cardiaque de la cardiopathie hypertensive et de la cardiomyopathie hypertrophique
Amylose Cardiopathie hypertensive Cardiomyopathie hypertrophique
Répartition de
l’épaississement VG
Globale Globale Habituellement
segmentaire
Taille de la cavité VG Normale à faible Normale, mais dilatation
possible au stade terminal
Normale, mais dilatation
possible au stade terminal
Fraction d’éjection Faible mais normale, ou
légèrement diminuée
Varie d’hyperdynamique à
faible
Souvent hyperdynamique
Epaisseur du VD Fréquemment augmentée Normale Rarement augmentée
Echogénicité myocardique Fréquemment augmentée Normale Normale
Contrainte
longitudinale/vélocité
en Doppler tissulaire
Fortement réduite Diminution discrète à modérée Diminution segmentaire
Anomalies valvulaires Possible épaississement
généralisé
Insuffisance mitrale le plus
souvent minime
Aucune anomalie
particulière
Insuffisance mitrale en cas de
déplacement systolique
vers l’avant
Fonction diastolique Souvent restrictive
(grade 3 ou 4)
Le plus souvent de
grade 1 ou 2
Absence d’anomalie
pathognomonique
Voltage de l’ECG Fréquemment bas dans les
dérivations périphériques
HVG HVG
Pression artérielle Normale à faible ; rarement élevée Augmentée Normale
IRM cardiaque Fréquent rehaussement tardif
généralisé après injection de
gadolinium, intéressant notamment
le VD et les oreillettes
Rehaussement tardif
absent ou minime
Variable ; un léger
rehaussement tardif est
fréquent, généralement
limité au VG
VG : ventriculaire gauche ; VD : ventriculaire droit ; IRM : imagerie par résonance magnétique ; HVG : hypertrophie ventriculaire gauche.
168 Circulation Mai 2012

16:00:20:04:12
Page 169
Page 169
n’induit quasiment jamais de neuro-
pathie cliniquement manifeste. La
réticence à pratiquer des biopsies
endomyocardiques chez les patients
âgés et l’erreur diagnostique consistant
à qualifier de cardiopathie hypertensive
Figure 3. Aspect caractéristique d’une cardiomyopathie amyloïde. A, image en incidence
parasternale selon le grand axe montrant l’épaississement concentrique du ventricule
gauche, dont la cavité demeure néanmoins de taille normale, ainsi que l’augmentation de
l’échogénicité myocardique. L’oreillette gauche est dilatée et il existe un petit épanchement
péricardique. B, image en incidence sous-costale chez un autre patient. On note une
dilatation des deux oreillettes, alors que les cavités ventriculaires droite et gauche sont de
taille normale, ainsi qu’un épaississement des parois ventriculaires droite et gauche avec
augmentation de l’échogénicité. C, Doppler tissulaire enregistré à hauteur de la portion
basale du septum objectivant une diminution de la vélocité systolique, un raccourcissement
de la durée de contraction longitudinale systolique et d’importants ralentissements des
vélocités diastoliques précoce et tardive. AVO : ouverture de la valve aortique ; AVC :
fermeture de la valve aortique.
ce qui est en réalité une amylose
cardiaque contribuent très certaine-
ment à une sous-estimation diagnos-
tique de l’amylose à la transthyrétine
mutée par substitution d’une isoleucine
en position 122 et de l’amylose sénile
cardiaque. Il a été publié que l’acide
3,3-diphosphono-1,2-propanodicarb-
oxylique marqué au 99mTc, qui est un
traceur utilisé en scintigraphie osseuse,
est très fortement capté par le myo-
carde dans l’amylose à la trans-
thyrétine. Certains ont proposé
d’utiliser la scintigraphie au dicarboxy-
propane diphosphonate comme
méthode simple de diagnostic non
invasif de l’amylose cardiaque à la
transthyrétine, car elle permet de la
distinguer de l’amylose AL, dans
laquelle la captation myocardique est
généralement plus faible.11
Traitement
Quelle que soit la forme d’amylose
cardiaque en cause, la prise en charge
comporte deux volets : le traitement
de l’insuffisance cardiaque congestive
et la prévention de l’accumulation
des dépôts amyloïdes. L’élimination
pharmacologique des dépôts pré-
existants n’est pas encore possible, bien
que de récentes données préliminaires
dans un modèle de souris transgénique
aient montré l’intérêt potentiel d’une
approche combinant médicaments
et anticorps.12 Si le traitement de
l’insuffisance cardiaque ne diffère que
peu suivant que l’amylose qui en est
responsable est à chaînes légères ou à
transthyrétine, celui de l’affection
sous-jacente, en revanche, diffère
totalement selon la forme en cause.
Dans l’amylose AL, peut-être en raison
de la présence conjointe d’un syn-
drome neurovégétatif, les inhibiteurs
de l’enzyme de conversion de l’angio-
tensine et les inhibiteurs des récepteurs
à l’angiotensine II sont rarement
tolérés et peuvent provoquer une
hypotension majeure, même lorsqu’ils
sont prescrits à faibles doses. Les
bêtabloquants n’ont pas d’efficacité
démontrée et peuvent aggraver l’hypo-
tension ; de leur côté, les inhibiteurs
calciques tendent à aggraver l’insuf-
fisance cardiaque congestive. C’est
pourquoi les diurétiques sont pra-
tiquement les seuls médicaments
disponibles pour traiter l’insuffisance
cardiaque secondaire à cette forme
d’amylose, bien que la spironolactone
et l’éplérénone soient généralement
bien tolérées et doivent probablement
être prescrites. Les bêtabloquants et les
inhibiteurs de l’enzyme de conversion
Falk L’amylose cardiaque 169
 6
6
 7
7
 8
8
1
/
8
100%