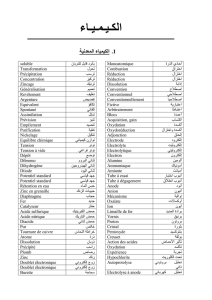
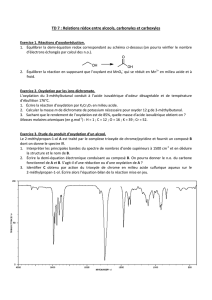
Chimie organique Chapitre 4 : Conversion par oxydoréduction


!
→ l'oxydation dépend de la classe de l'alcool
"#
OH
CrO
3
pyridine
CH
2
Cl
2
O
r = 90%

$%
#
●Utilisation du permanganate de potassium dilué
et à froid:
●Utilisation du tétraoxyde d'osmium et d'un co-
oxydant:
KMnO
4
dilué, à froid
HO OH
+
HO OH
OsO
4
(cat.)
H
2
O
2
(stoech.)
OH
OH
+
OH
OH

%
&'()
*deux réactions: oxydation de l'alcène en diol
puis clivage oxydant.
OsO
4(cat)
NaIO
4(stoechio)
O
O
solvant eau/éther

+,-
,./0)
1): cf tableau
#2): Un équivalent de NaBH4 pour
quatre équivalents de carbonyle.
#: Addition nucléophile
.
O
NaBH
4
éthanol
OH
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
1
/
13
100%