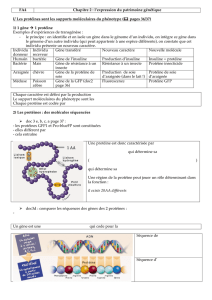
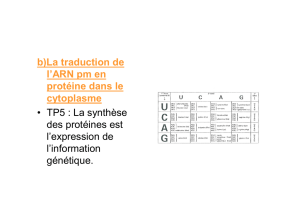
Web 5 Fiche 2

1
Web 5 Fiche 5.1
MUTANTS DES GÈNES DE DIVISION :
LEUR UTILISATION DANS LA CONSTRUCTION DU
SEPTOSOME
L. Paolozzi
Les premiers mutants de division ont été isolés chez E. coli dans différents laboratoires dans les
années 1964 à 1973. Il s’agissait de mutants conditionnels de type thermosensible, c’est-à-dire
poussant à la température permissive de 30 °C et létaux à 40-42 °C. Ces mutants (encore
précieux) ont été au centre des premières dissections du processus de division. En effet,
l’observation au microscope de ces bactéries mutantes exposées à la température non permissive
a fourni les toutes premières indications sur l’identification et le rôle des gènes de division :
gènes à activité précoce (intervenant dans la formation du septum), gènes impliqués dans la
croissance de cette structure ; et gènes « tardifs ». D’autres mutants ont permis d’identifier les
gènes contrôlant la localisation et la chronologie de la formation du septum, d’autres encore
ceux responsables de la ségrégation des nucléoïdes, et encore d'autres activités liées à la
division. Beaucoup de ces mutants sont caractérisés par la formation de longs filaments à
température non permissive, d’où le nom de fts donné aux gènes correspondant (fig. F5.1-1).
Avec le développement des technologies du génie génétique, il est devenu possible
d’effectuer des constructions génétiques qui permettent de bloquer transitoirement dans une
cellule l’activité d’un gène donné. De telles constructions ont été réalisées aussi pour les gènes
de division chez E. coli et quelques autres Bactéries modèles. Le principe de ces constructions
est le suivant. Le gène étudié, ici un gène essentiel puisqu’intervenant dans la division, est
mutagénisé (sous forme de mutants thermosensibles, ts, ou de mutants insertionnels, avec un
transposon). La fonction du gène muté est suppléée dans la cellule grâce à un allèle sauvage du
gène positionné sous le contrôle d’un promoteur (plac ou para) inductible par ajout,

2
respectivement, de lactose ou d’arabinose. Cette bactérie croît normalement, par
complémentation, tant que le gène sauvage est induit, mais cesse de croître et meurt en absence
d’induction. Ce genre de constructions permet d'étudier l’effet d'un blocage transitoire de
l’expression d’un gène donné. Formellement, des observations analogues peuvent être faites
avec des mutants thermosensibles au cours des transitions thermiques 30 °C 42 °C 30 °C.
L’avantage des systèmes agissant sur l’expression d’un gène par rapport à ceux basés sur
l’inactivation par dénaturation protéique, est d’effectuer des transitions plus rapides et plus
nettes entre les deux états (expression vers non-expression d’un gène, et éventuellement retour à
la condition normale par ré-induction du gène). De telles souches mutantes, associées à
l’utilisation du marquage de protéines avec un fluorochrome, en général la GFP (Web 5 Fiche
5.2), ont permis d’aborder la question complexe de la chronologie des événements associés à la
formation du septum. Ainsi, il a été possible d'analyser, par mutation de la douzaine de gènes
essentiels impliqués dans la formation du septum, la séquence temporelle de migration au site
de division de chacune des protéines Fts.
Figure F5.1-1 - Phénotype d’un mutant thermosensible du gène ftsI d’E. coli à températures
permissive (30 °C) et non permissive (42 °C).
Différentes études réalisées avec des mutants du gène ftsZ ont conduit à la conclusion que le
produit de ce gène est le premier à agir dans la formation du septum. En effet, en son absence
aucune autre protéine de division ne se localise au site de division. Il y a donc dépendance de la
localisation de toute autre protéine vis-à-vis de la localisation de FtsZ. À partir de cette base, la
question de la séquence temporelle de localisation des autres protéines, après celle de FtsZ, a pu
être abordée. La méthodologie consiste à observer, chez une série de souches isogéniques, c’est-
à-dire ayant toutes le même génotype sauf pour le marqueur étudié, les effets du blocage de

3
l’expression de ce marqueur sur la localisation des autres protéines de division : par exemple, le
blocage de l’expression du gène ftsA sur la localisation des protéines FtsK, FtsI, FtsN, etc.,
visualisées par leur marquage fluorescent. Puis le même protocole est appliqué à une autre série
de souches bloquées pour l’expression d’un autre gène de division. Ces expériences sont à la
base de nos connaissances sur la temporalité de la localisation des protéines de division décrite
dans le Chapitre 5.

4
Web 5 Fiche 5.2
MÉTHODES D’ÉTUDE POUR LA LOCALISATION
DES PROTÉINES DE DIVISION
L. Paolozzi
La détection et la localisation des protéines sont de grande importance pour comprendre leur
rôle et leur mode de fonctionnement, particulièrement quand elles agissent au sein de complexes
multiprotéiques. Deux techniques précieuses, développées dans ce but pour l’étude des cellules
eucaryotes et appliquées ensuite aux procaryotes, sont l’immuno-microscopie électronique et
l’examen en microscopie à fluorescence de protéines marquées avec un fluorochrome. Chez les
procaryotes, ces technologies trouvent de nombreux domaines d'emplois, depuis la détection et
le dénombrement de cellules dans l’environnement (aliments compris) jusqu’à l’étude des
fonctions des protéines, pour laquelle elles permettent d’analyser et de disséquer des processus
complexes tels que la réplication, la division, la différenciation.
L'immuno-microscopie électronique a été appliquée pour la première fois chez E. coli pour
étudier la localisation de la protéine FtsZ (Chap. 5). La technique consistait en un immuno-
marquage utilisant des billes d’or couplées à des anticorps. Il fut ainsi possible d’observer la
formation de la structure annulaire de l’anneau Z dans la région centrale de la cellule. Quelques
années plus tard (1996), X. Ma et W. Margolin mirent au point chez E. coli une technique
permettant de détecter la localisation de protéines de division en microscopie à fluorescence.
Cette technique consistait à faire exprimer aux cellules des protéines recombinantes dont
l’extrémité C-terminale était fusionnée à un fluorochrome (par exemple la protéine GFP,
Encart F5.2-1). Les résultats observés avec cette technique ont confirmé ceux obtenus par
immuno-microscopie électronique quant à la localisation de FtsZ, ouvrant le chemin à l’étude de
la localisation des autres protéines de division, ceci sans recourir à la production d’anticorps
spécifiques. Par exemple la localisation de la protéine de division FtsN, sous forme de fusion
FtsN-GFP, a été suivie chez E. coli (fig. F5.2-1).

5
Figure F5.2-1. Localisation de la protéine FtsN au site de division chez E. coli.
Visualisation en microscopie à fluorescence par fusion à GFP (Grenga et al., 2013).
Encart F5.2-1 - La microscopie à fluorescence et les sondes fluorescentes
La microscopie à fluorescence permet d’observer un échantillon marqué de façon spécifique
avec une sonde fluorescente, ou fluorochrome. Cette technique utilise une source de lumière
plus puissante que celle du microscope optique, et des filtres qui permettent de choisir une
gamme de longueur d’onde permettant d'exciter spécifiquement le fluorochrome. La lumière
alors émise par l’échantillon excité est filtrée à la longueur d’onde d’émission du fluorochrome.
Le signal détecté renseigne donc de façon spécifique sur la molécule ou le complexe
fluorescent, et permet d’en observer la localisation dans la cellule.
Les fluorochromes, ou fluorophores, sont des substances composées de plusieurs noyaux
aromatiques conjugués ou de molécules planes et cycliques. Ces substances ont la propriété
d’émettre de la lumière à une longueur d’onde définie lorsqu'elles sont excitées à leur longueur
d'onde d'absorption (lumière d’excitation). Puis elles retournent à leur état fondamental très
rapidement en émettant de la lumière à une longueur d’onde supérieure à celle d’excitation
(lumière d’émission). Parmi les fluorochromes les plus utilisés dans les études de biologie
cellulaire, citons la protéine fluorescente « verte » GFP (Green Fluorescent Protein) extraite de
la méduse Aequorea victoria (le mot « verte » désigne la lumière verte intense émise). Il existe
un certain nombre de mutants du gène exprimant la GFP, conduisant à la synthèse de
fluorochromes ayant de nouvelles caractéristiques d’absorption et d’émission de lumière. Ce
sont YFP (Yellow Fluorecent Protein) qui émet une lumière jaune, CFP (Cyan Fluorescent
Protein), qui émet dans le bleu-gris, et BFP (Blue Fluorescent Protein), qui émet dans le bleu.
De nombreux mutants ont aussi été produits pour modifier la sensibilité au pH de ces protéines
et l’intensité d’émission de la lumière.
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
1
/
12
100%