La protonthérapie - Paul Scherrer Institut

La protonthérapie
à l‘Institut Paul Scherrer

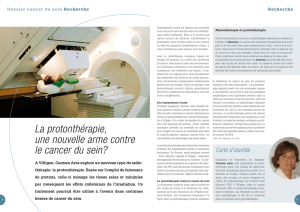
Protonthérapie au PSI pour les tumeurs de l’œil (OPTIS). La tête des patients est immobilisée avec un masque et un porte-empreinte dentaire. L’irradiation
proprement dite de la tumeur de l’œil dure moins d’une minute. Il est nécessaire de pratiquer quatre irradiations durant quatre jours consécutifs.

3
L’objectif de la radiothérapie à l’Institut Paul
Scherrer (PSI) est la destruction du tissu tumoral
au moyen de particules chargées appelées pro-
tons. Les protons se prêtent particulièrement bien
à la radiothérapie car ils exercent l’essentiel de
leurs effets dans les profondeurs de l’organisme,
au niveau de la tumeur. Grâce à une technique
d’irradiation unique au monde, la nouvelle ins-
tallation de protonthérapie du PSI permet d’adap-
ter très précisément la dose de radiation à la
forme de la tumeur, la plupart du temps irrégu-
lière, et de préserver encore mieux le tissu sain
qu’avec les techniques modernes usuelles de
radiothérapie.
En 1984, pour la première fois, des tumeurs de
l’œil ont été irradiées avec des protons au PSI.
L’installation utilisée pour ce faire était la première
de ce genre en Europe. Fin 1996 a été mis en service
au PSI le premier bras isocentrique (Gantry)pour
l’irradiation des tumeurs profondes. Grâce au
développement en cours de la technique d’irradi-
tion, à l’avenir également des tumeurs mobiles
pendant la durée du processus d’irradiation (p.ex.
les cancers du sein ou des poumons) devront
pouvoir être traitées avec une très haute précision.
En matière d’avancées technologiques de la pro-
tonthérapie, le PSI est numéro un mondial et c’est
donc lui qui donne les tendances pour le traitement
des tumeurs cancéreuses par radiothérapie.
La protonthérapie
à l’Institut Paul Scherrer
Installation OPTIS pour l’irradiation des tumeurs de l’œil avec des protons. Une fois les faisceaux de protons ajustés
avec précision sur la tumeur de l’œil, l’irradiation est réalisée. Jusqu’à présent, plus de 5000 patientes et patients ont
bénéfi cié de cette thérapie au PSI.

4LA PROTONTHÉRAPIE À PSI
Une meilleure radiothéra
p
ie
signifi
e
• ada
p
tation
p
lus
p
récise de la
dose de radiation à la forme
de
l
a
tu
m
eu
r
• dose de radiation
p
lus élevée
dans le volume cible (tumeur
plus marge de sécurité)
• diminution de l’ex
p
osition
des structures organiques
saines aux rayons
• chances de
g
uérison durable
p
lus im
p
ortantes
•
e
ff
ets
seco
n
da
ir
es
m
o
in
s
im
p
ortants
• meilleure
q
ualité de vie
•
coûts
du
t
r
a
i
te
m
e
n
t
r
a
i
so
nn
ab
l
es
permet de réduire considérablement ou d’éviter
les effets secondaires à court et à long terme.
La thérapie par rayonnement, aussi appelée
radiothérapie, est, comme la chirurgie, une
méthode de traitement locale qui lutte donc contre
des tumeurs «géographiquement limitées». Elle
ne peut pas être remplacée par des thérapies
devant agir sur l’ensemble de l’organisme (notam-
ment pour le traitement des métastases), comme,
par exemple, la chimiothérapie et l’immunothéra-
pie (thérapies systémiques).
La radiothérapie est une forme de traitement
dans laquelle les cellules tumorales sont détruites
soit par des rayons X ou gamma (thérapie par
photons), soit par des faisceaux de particules
(protonthérapie par exemple). Toutes les amélio-
rations de la radiothérapie visent à détruire la
totalité de la tumeur tout en préservant de mieux
en mieux les tissus sains.
Au cours des 20 dernières années, de grands
progrès ont été faits dans le domaine de la radio-
thérapie conventionnelle. Cependant, avec la pro-
tonthérapie, il est possible de parvenir à des
résultats encore nettement meilleurs pour certai-
nes indications et localisations de tumeurs. De
plus, les progrès faits au PSI montrent que les
possibilités d’amélioration sont encore loin d’être
épuisées.
Comment agit la radiothérapie?
Si une particule chargée, par exemple un proton,
traverse une cellule ou s’immobilise dans celle-ci,
l’énergie qu’elle y dépose (dose) endommage le
noyau de la cellule. Cependant, la cellule peut,
dans certains cas, réparer ces dommages. Tout
l’art de la radiothérapie consiste à administrer une
dose telle que les cellules tumorales n’aient aucune
chance de se réparer et meurent toutes, sans
exception, et que les cellules saines subissent, par
contre, le moins possible de dommages et puissent
se remettre sans problème.
La dose de radiation mesure l’énergie absorbée
dans un matériau, par exemple dans les tissus.
Cependant, les effets biologiques des rayons ne
dépendent pas uniquement de la quantité d’éner-
gie, mais aussi de la façon dont l’énergie est
La radiothérapie et son importance
En Europe, une personne sur trois souffrira proba-
blement d’un cancer au cours de son existence.
Chaque année, rien qu’en Suisse, environ 30 000
personnes apprennent qu’elles ont un cancer.
Parmi elles, environ 70 % auront besoin pendant
leur maladie de radiothérapie. Aujourd’hui, un peu
plus de 45 % de l’ensemble des tumeurs diagnos-
tiquées sont curables, ce qui signifi e qu’à l’issue
du traitement, les personnes concernées vivent
plus de cinq ans sans récidive cancéreuse. Environ
22 % doivent leur guérison à la chirurgie, environ
12 % à la radiothérapie, environ 6 % à une combi-
naison de ces deux méthodes et environ 5 %
(tumeurs métastasées et non localisées) à d’autres
techniques et combinaisons de traitements,
chimiothérapie comprise.
La radiothérapie constitue donc une forme de
traitement importante, qui est souvent la seule
possible pour les tumeurs non opérables. Le trai-
tement des tumeurs primaires augmente les chan-
ces de guérison et donc l’espérance de vie. Il est
d’autant plus important de procéder à la radiothé-
rapie en ciblant les tissus malades avec la plus
grande précision possible et en irradiant le moins
possible les cellules saines de l’organisme. Cela
Au PSI, protonthérapie des tumeurs de l’œil avec un
faisceau de protons spécial de faible profondeur de
pénétration (OPTIS). Ces photographies de l’intérieur de
l’œil, réalisées à travers la pupille, montrent un exemple
de guérison: en haut avant le traitement protonique, en
bas, un an après: la tumeur s’est résorbée.

5
LA PROTONTHÉRAPIE À PSI
déposée dans les cellules. La dose d’énergie est
toujours mesurée en grays (Gy). Une dose théra-
peutique typique pour la destruction d’une tumeur
est de 60 à 70 Gy environ. En radiothérapie, elle
est administrée en plusieurs fractions (environ 30
à 40 fractions au total) sur plusieurs journées
successives.
La protonthérapie dans le monde
et au PSI
La protonthérapie repose sur plus de 50 ans d’ex-
périence des effets biologiques des faisceaux de
protons sur les cellules malades et saines du corps.
En 1954, un patient a été traité pour la première
fois au Lawrence Berkeley Laboratory, en Californie
(Etats-Unis), et le premier programme européen
de protonthérapie s’est déroulé de 1957 à 1976 à
Uppsala (Suède). En 1961, l’Harvard Cyclotron
Laboratory et le Massachusetts General Hospital
de Boston, aux Etats-Unis, ont lancé un projet de
protonthérapie. En 1984, des traitements de méla-
nomes oculaires ont eu lieu pour la première fois
en Europe, au PSI, dans l’installation OPTIS spé-
cialement conçue à cet effet.
La première installation de protonthérapie
mise en service dans une clinique l’a été au Loma
Linda City University Medical Center, en Californie,
en 1990. Depuis 1999, après une phase de mise
au point et d’essais de presque 10 ans, quelque
1500 patientes et patients y bénéfi cient chaque
année régulièrement de la protonthérapie.
Aujourd’hui, dans le monde entier, plus de 35
centres sont en service et plus de 80 000 patients
ont déjà été traités par protonentherapie, presque
10 % d’entre eux au PSI.
Au début des années 90 a été développée au
PSI la technique dite Spot Scan pour le traitement
des tumeurs profondes par protonthérapie. La
technique du PSI est supérieure aux méthodes
d’irradiation par protons utilisées dans les autres
centres. Elle permet une meilleure préservation
des tissus sains. Depuis 1996, sont traités au PSI
grâce à cette méthode extrêmement précise des
patientes et patients souffrant de tumeurs parti-
culièrement diffi ciles à irradier. En Europe, outre
le PSI, six autres installations de protonthérapie
sont en service, trois d’entre elles peuvent unique-
ment traiter les tumeurs de l’œil. A l’heure actuelle,
dans le monde entier, plus de 30 projets de pro-
tonthérapie, dont une dizaine environ en Europe,
sont en cours d’élaboration ou à un stade avancé
de planifi cation. Aujourd’hui, plus de 10 000
patientes et patients par an, essentiellement celles
et ceux souffrant de tumeurs de l’œil, de tumeurs
au cerveau et dans la région de la tête, du bassin
et de la colonne vertébrale, sont traités avec des
protons dans environ 35 centres situés dans le
monde entier.
L’expérience clinique acquise avec les protons
a montré que la précision spatiale de l’irradiation
contribuait souvent de manière décisive au succès
de la thérapie. Comme la technique développée
au PSI permet une irradiation d’une précision très
élevée, c’est elle qui, dans le monde entier, a donné
l’exemple pour l’amélioration de la protonthérapie.
La quasi-totalité des installations en phase de
planifi cation ou en cours de construction misent
aujourd’hui sur la technique Scanning, utilisée
pour la première fois au PSI. Ce succès ne reposait
pas seulement sur des accélérateurs appropriés
et des spécialistes expérimentés, mais aussi, pour
beaucoup, sur l’environnement interdisciplinaire
du PSI et sur le contexte expérimental particulier
que constitue la recherche physique fondamentale.
L’équipe du PSI dispose aujourd’hui de plus
de 25 ans d’expérience dans le domaine de la
protonthérapie. Jusqu’à la mi-2011, presque 6000
tumeurs de l’œil et plus de 750 tumeurs profondes
Protonthérapie des tumeurs
profondes sur la Gantry 1.
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
1
/
16
100%



![b Hadron [Mode de compatibilité]](http://s1.studylibfr.com/store/data/002417202_1-6b36b4f76839b80a7f6a44fc60111ea2-300x300.png)






