Lire l`article complet

141
repères repères
Neuro-Sciences
Répartition
anatomique
du médiateur
Au sein du SNC, les grandes
voies cholinergiques ont été
réparties en trois grandes
catégories :
– les motoneurones de la moelle épinière,
dont les collatérales stimulent les neurones de
Renshaw ;
– le groupe des neurones à projections locales
ou interneurones : striatum +++, en faible pro-
portion, dans l’hippocampe et le cortex ;
– les neurones cholinergiques à projections
diffuses (figure 1).
Selon la classification de Mesulam, il existe
huit sous-groupes distincts par leurs localisa-
tions et leurs projections. Les groupes Ch1 et
Ch2 innervent l’hippocampe ; le groupe Ch3
innerve le cortex cingulaire et le bulbe olfac-
tif ; le groupe Ch4 comprend le nucleus basa-
lis de Meynert, le noyau préoptique magno-
cellulaire et la substance innominée. Les
noyaux Ch5 à Ch8 concernent des territoires
du tronc cérébral, les groupes Ch5 et Ch6 pro-
jetant pour partie vers le thalamus et l’hypo-
thalamus.
Synthèse, libération
et dégradation (figure 2)
Ces deux étapes se font grâce à des enzymes,
respectivement l’acétylcholine transférase
(ChAT) et l’acétylcholine estérase (AChE).
La ChAT est synthétisée dans le péricaryon
des neurones cholinergiques, puis véhiculée
par le transport axonal lent vers les terminai-
sons synaptiques. Sa concentration n’est pas
un facteur limitant de la synthèse de l’ACh.
Celle-ci a lieu dans le cytosol où, en présence
d’ATP, la ChAT utilise un acétyl-CoA (issu
du cycle de Krebs), qu’elle couple à une cho-
line dont l’origine est variable (recaptage
d'un catabolite de l’ACh, dégradation de
phospholipides, pool plasmatique) ; la captu-
re de la choline dépend d’un transporteur uti-
lisant le Na+. Après relargage de la coenzy-
me A, l’ACh est stockée dans des vésicules
grâce à une ATPase. On distingue deux pools
synaptiques, le nouvellement synthétisé
étant plus facilement libéré.
Quant à l’exocytose de
l’ACh, elle se fait de façon
classique, calcium-dépen-
dante. L’inactivation de
l’ACh, au contraire des
catécholamines et des autres
médiateurs dérivés des
acides aminés, ne dépend
pas d’un système de recap-
ture mais uniquement d’une hydrolyse enzy-
matique, par l’AChE (1). Celle-ci est
concentrée dans les membranes synaptiques,
où elle agit très vite (une molécule d’enzyme
peut dégrader 5 000 molécules d’ACh par
seconde !).
Les différents types
de récepteurs et leurs voies
de transduction (figure 3)
Deux types de récepteurs : les récepteurs
nicotiniques et les muscariniques.
À l’inverse de la répartition observée dans le
système nerveux végétatif, la densité des
L’acétylcholine (ACh) a été le premier neuromédiateur
identifié et reste au centre des préoccupations
des neuropharmacologues du fait de la multiplicité
de ses effets et des voies nerveuses qui interagissent
avec le système cholinergique central.
* Service de pharmacologie,
CHU Côte de Nacre, Caen.
La neurotransmission
cholinergique centrale
A. Coquerel*
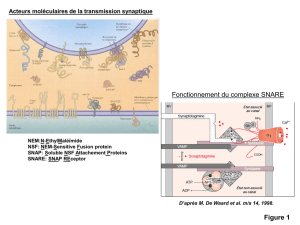
Figure 1. Représentation
schématique sur une
coupe sagittale centren-
céphalique des localisa-
tions anatomiques des
voies longues choliner-
giques centrales
(d’après Mesulam) :
Ch1 et Ch2 : innervation
de l’hippocampe ;
CH3 : cortex
cingulaire ; Ch4 :
nucleus basalis de
Meynert ; Ch 5 et 6 :
voies projetant vers l’hy-
pothalamus et le thala-
mus ; Ch 7 et 8 : voies
longues du tronc
cérébral.
Ch5 et 6
Ch4
Ch1 et 2
Ch7 et 8
Ch3
FORMER

repères repères
Act. Méd. Int. - Neurologie (1) n° 4, septembre 2000 142
récepteurs muscariniques est plus importan-
te dans le SNC que celle des nicotiniques.
Ces derniers sont présents dans le cortex et
l’hippocampe, le noyau caudé, le thalamus et
l’hypothalamus.
Sur le plan structural, comme pour les autres
récepteurs-canaux, les récepteurs nicoti-
niques sont constitués par l’assemblage de
5 sous-unités. Chacune possède 4 domaines
transmembranaires.
Au niveau du SNC, cet assemblage consiste
en une stoechiométrie simple : 3 sous-
unités α(et 2 sous-unités ß). Mais il en exis-
te 8 variants ! Les récepteurs nicotiniques
centraux peuvent donc correspondre à une
grande palette d’associations de sous-unités
(et ß). Le site d’action des agents nicoti-
niques est extra-cellulaire, au niveau des
extrémités N-terminales des sous-unités du
récepteur canal. La liaison ligand-récepteur
aboutit à une brutale perméabilité du canal cen-
tré entre les 5 sous-unités (1, 2). La régulation
de ces récepteurs-canaux dépend de la phos-
phorylation des différentes boucles intracellu-
laires (forte phosphorylation = canal ouvert,
déphosphorylation = canal fermé).
Les récepteurs muscariniques :
ils sont caractérisés par
autoradiographie, puis
par hybridation in situ
Les récepteurs M1 et M2, les plus répandus,
peuvent être caractérisés par des ligands spéci-
fiques 5 gènes qui codent pour 5 types de
séquences voisines (notées de M1 à M5). Ces
différents récepteurs appartiennent à la super-
famille des récepteurs à 7 domaines transmem-
branaires couplés à des protéines G (RCPG).
Forte expression des récepteurs M1 au niveau
du cortex et de la région hippocampique, ainsi
que dans le noyau accumbens et le néostriatum.
Récepteurs M2 = distribution plus diffuse,
prépondérants dans le système habenulo-
pédonculaire et les noyaux du tronc cérébral.
Les mécanismes de transduction
(1, 2)
●Pour les récepteurs M1 = couplage à l’adé-
nylate-cyclase.
Neuro-Sciences
Figure 2. La synapse cholinergique.
ChAT
ChAT ChAT
flux axonal acétyl-CoA
choline
Acétylcholine
cycle
de Krebs
Glucose
ChAT : acétylcholine tranférase
AChE : acétylcholine estérase
Choline
plasmatique
Dégradation des
phospholipides
membranaires
choline captage Na+
dépendant
Acétyl
AChE
récepteurs
muscariniques
récepteurs
nicotiniques
ACh
ACh
Figure 3. Représentation schématique des récepteurs nicotiniques (partie gauche) et muscariniques
(partie droite). Les récepteurs nicotiniques sont constitués de 5 sous-unités (3 formes αet 2 formes
ß) qui traversent la membrane et créent un pore ionique au centre de leur assemblage ; les deux
types de récepteurs muscariniques ont en commun leur structure classique à 7 domaines trans-
membranaires, donc un couplage à des protéines G. En revanche, on peut distinguer deux sous-
groupes par leur type de transduction : le sous-groupe M1 est couplé négativement à l’adénylate-
cyclase ; la diminution de l’AMP cyclique entraîne une inhibition de la protéine-kinase de type A
(PKA). Pour les récepteurs de type 2 (M2) la transduction se fait par la stimulation de la phos-
pholipase C, qui catalyse un lipide membranaire (PIP2) en inositol tri-phosphate (IP3), qui mobi-
lise le calcium intracellulaire, et le di-acyl-glycérol qui va stimuler la protéine-kinase C (PKC).
R nicotinique
unités 3α 2ß
R muscarinique
7 dom. trans Mb R muscarinique
7 dom. trans Mb
Phospholipase C
stimulée ++
PKC stimulée
Adénylate-
cyclase
PKA inhibée
…/…

143
La stimulation des protéines G inhibe l’adé-
nylate-cyclase et diminue donc la concen-
tration d’AMP cyclique.
Cette baisse de l’AMPc cytosolique induit
à son tour une inhibition de la protéine-kina-
se A (PKA).
●Pour les récepteurs de type M2 : voie de la
phospholipase C (PLC), qui va cliver des
phospholipides membranaires et ainsi don-
ner naissance à deux types de signaux : les
inositols triphosphates (IP3) et le di-acyl-
glycérol (DAG). L’IP3 augmente le calcium
cytosolique et va donner naissance à de nom-
breuses réactions, telle l’activation de la cal-
cium-calmoduline-kinase, enzyme clé qui
peut tantôt moduler l’activation des canaux
ioniques par phosphorylation et tantôt indui-
re la mobilisation ou la synthèse de nom-
breux neurotransmetteurs. Quant au DAG,
il peut soit être catabolisé en acide arachi-
donique (précurseur de nombreux messa-
gers dont les prostaglandines), soit activer
la protéine-kinase C (PKC) qui peut phos-
phoryler de nombreuses protéines intracel-
lulaires. Des cascades de phosphorylations
pourront aboutir à l’activation de facteurs
de transcription au niveau nucléaire.
Effets cellulaires de la stimulation
des récepteurs cholinergiques
La stimulation des récepteurs nicotiniques
aboutit à une excitation rapide et intense
liée à l’ouverture d’un canal cationique,
donc perméable au Na+.
L’ A Ch a un effet excitateur direct sur les
récepteurs muscariniques, en particulier au
niveau du cortex et de l’hippocampe.
L’ A Ch induit une dépolarisation de longue
durée par blocage des conductances potas-
sique et calcique et augmentation de la
résistance membranaire, d’où une augmen-
tation de la fréquence des décharges neuro-
nales et des modifications durables de l’ex-
citabilité des champs récepteurs
périphériques. On décrit également des
effets présynaptiques de l’ACh sur des
récepteurs muscariniques et une inhibition
de ces neurones par la stimulation d’auto-
récepteurs.
Effets physiologiques globaux
Rythme veille/sommeil.
Certains contrôles moteurs (noyaux gris cen-
traux).
Mémorisation et tâches d’apprentissage
(voies septo-hippocampique ou basalo-corti-
cale) :
–l’injection d’agonistes cholinergiques amé-
liore la mémorisation ;
–les anticholinergiques centraux diminuent
l’efficience mnésique et les capacités d’ap-
prentissage.
La pathologie et ses espoirs
d’exploration
Maladie d’Alzheimer (MA) ++++.
Maladie des corps de Lewy disséminés.
Maladie de Parkinson (MP).
Intérêt +++ de l’imagerie par émission de
positons (PET), avec des ligands nicotiniques,
➞diagnostic précoce de la démence de type
Alzheimer (DTA).
Traitements par des
médicaments cholinergiques
Anticholinergiques centraux (trihéxyphéni-
dyle [Artane®, Parkinane LP®], tropatépine
[Lepticur®], bipéridène [Akinéton LP®]) et
syndromes parkinsoniens.
Emploi actuellement limité aux syndromes
parkinsoniens liés à la prise de neuroleptiques.
Risques +++ effets parasympathicolytiques
périphériques ( mydriase, rétention d’urine,
etc.).
Effets atropiniques centraux = confusion men-
tale chez les sujets âgés.
Cholinomimétiques et maladie
d’Alzheimer
●apport de choline = pas de résultats signi-
ficatifs ;
●inhibiteurs centraux de l’AChE : efficaci-
té modérée mais documentée.
La tacrine (Cognex®) a été le premier à
recevoir une AMM, la rivastigmine
(Exelon®) et le donépézil (Aricept®) ont une
meilleure tolérance hépatique, on doit
reconnaître que l’efficacité de ces inhibi-
teurs de l’AChE reste modérée.
Traitements “antidégénératifs”
Deux facteurs de croissance, dont les rôles
physiologiques sont bien établis lors de
l’organogenèse : le LIF (Leukemia
Inhibitory Factor) et le CNTF (Ciliary
Neurotrophic Factor)=facteurs de crois-
sance peptidiques qui appartiennent au
groupe des cytokines.
Deux de leurs actions reconnues pendant la
vie fœtale sont d’orienter la différenciation
neuronale vers le phénotype cholinergique
et d’entraîner un accroissement de résis-
tance à l’apoptose.
Des tentatives de thérapie génique sont à
l’étude, soit par intégration au sein des
neurones des séquences codantes pour ces
facteurs de croissance, soit par sécrétion de
ces polypeptides à partir de lignées cellu-
laires animales modifiées qui sont implan-
tées dans le SNC sous forme encapsulée
(3). Des essais thérapeutiques commencent
à se développer avec ces cellules encapsu-
lées.
Références
1. Lamour Y, Dutar P, Bassant MH.
Physiologie et pharmacologie des systèmes
cholinergiques centraux. Circ Métab Cerveau
1989 ; 6 : 21-46.
2. Neurosciences. Purves, Augustine,
Fitzpatrick, Katz, LaMantia, McNamara.
(Édition française). De Boeck Université,
1999 : 109-43.
3. Lysaght MJ, Aebischer P. Encapsulated
cells as therapy. Sci Am 1999 ; 280 : 76-82.
repères repères
Neuro-Sciences
1
/
3
100%