i. obstacles sur la voie d`ejection du ventricule gauche

Chapitre IIC, page 1
I. OBSTACLES SUR LA VOIE D'EJECTION DU VENTRICULE
GAUCHE (JP BOURDARIAS)
A. ANATOMIE
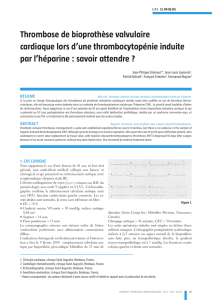
L'obstacle peut siéger en un point quelconque de la voie d'éjection (Figure 1):
a - Valvulaire : fixe, acquis (RAA, calcifications) ou congénital
b - Sus- ou sous-valvulaire : fixe, toujours congénital
c - Sous-valvulaire, dynamique (cardiomyopathie obstructive (héréditaire)
d - Coarctation de l'isthme de l'aorte (congénitale)
Sus-Valvulaire
Sous-Valvulaire
Valvulaire
Aorte
Figure 1-
Siège possible de la sténose sur la voie d'éjection du VG. Les valves mitrales antérieure et postérieure délimitent
la partie supérieure de la chambre de remplissage. Noter que la valve antérieure est bien fixée sur l'anneau
aortique tandis que la postérieure s'insère sur l'arc postérieur de l'anneau mitral
B. CONSEQUENCES PHYSIOPATHOLOGIQUES
En amont de la sténose : hypertension VG
En aval de la sténose : hypotension aortique
Mécanisme compensateur : HVG de type concentrique (sauf dans la cardiomyopathie (HVG asymétrique)
C. RETRECISSEMENT VALVULAIRE AORTIQUE
Surface normale de la valve : 2,5 à 3,5 cm2
- Apparition d'un souffle si la surface diminue de 20 à 25 %
- Apparition d'un gradient de pression si la surface = 1 cm2
- Apparition de signes fonctionnels si 1.0 < S < 0.75 cm2
1. LES 10 POINTS IMPORTANTS DU RETRECISSEMENT VALVULAIRE AORTIQUE (RA)
1- Dans les pays développés, la cause est : maladie de Monckeberg ou rétrécissement dégénératif. La dialyse
rénale peut induire une sténose et si elle préexiste, l’aggrave toujours.
2- Le RA entraîne une HVG de type concentrique (cavité VG non dilatée, parois épaisses) correspondant à la
phase dite "compensée".

Chapitre IIC, page 2
3- Pendant la phase compensée, les signes fonctionnels surviennent à l’effort (DE, AE, syncopes). Un AE peut
exister alors que les coronaires sont normales.
4- La phase "décompensée" est caractérisée par l’apparition d’une insuffisance cardiaque avec dilatation du
VG.
5- Le souffle de RA est maximum au foyer aortique, irradie dans les vaisseaux du cou mais aussi à la pointe où
il simule une insuffisance mitrale. Cependant, le fait qu’il augmente d’intensité lors de la contraction qui suit
une diastole longue prouve que cette irradiation apicale est un souffle d’éjection.
6- La radiographie thoracique ne montre pas de dilatation du VG sauf si le patient est en insuffisance cardiaque
ou que le RA est associé à une insuffisance aortique notable.
7- Pour détecter l’HVG, l’échocardiogramme est beaucoup plus sensible que l’ECG.
8- L’échocardiogramme permet d’évaluer le degré de sévérité du RA en mesurant la surface de l’orifice. En
moyenne, la surface aortique diminue de 0,1 cm2 par an.
9- L’indication opératoire (remplacement valvulaire) est basée sur l’existence de symptômes et la surface de
l’orifice (valeur critique < 0,7 cm2 ou mieux : 0,45 cm2/m2 ou si la surface n’a pas été calculée : vitesse du
jet > 4 m/s).
10- Patient symptomatique + surface valvulaire aortique < 0,7 cm2 : indication opératoire
Patient asymptomatique + surface < 0,7 cm2 : surveillance clinique (apparition de symptômes) et
échocardiographique trimestrielle.
2. ETIOLOGIE
1. RA Congénital : La valve est sténosée dès la naissance (aspect en dôme par fusion des
commissures).
2. RAA : Fusion de 2 ou 3 commissures, très souvent associée à une autre atteinte valvulaire
(RM, IA)
3. RA dégénératif calcifié de Monckeberg -
- Soit calcification d'une valve bicuspide ; la valve bicuspide est un précurseur fréquent de RA.
- Soit calcification d'une valve aortique normale (tricuspide), mais il n'y a pas en principe de
fusion des commissures. C'est de très loin la cause actuelle la plus fréquente .
4. Le RA dégénératif est plus fréquent dans l'hypercalcémie (dialysés chroniques±
hyperparathyroïdie), la sarcoïdose et la maladie de Paget. On a constaté chez les sujets âgés
que le taux de parathormone est plus élevé dans le RA qu'un groupe contrôle et que la perte
osseuse (mesurée par la densité osseuse) est associée à la fréquence des calcifications
aortiques. A titre exceptionnel: sténose athéromateuse des hypercholestérolémies majeures
homozygotes.
3. PHYSIOPATHOLOGIE
a) La résistance à l'éjection du VG :
Deux mécanismes possiblement associés :
- Degré de sténose de l'orifice, dont les dimensions sont fixes (fusion commissurale); c'est le cas
du RA congénital ou rhumatismal.
- Degré de mobilité des sigmoïdes en raison des calcifications, (sans fusion commissurale). Dans
ce cas, la sévérité du RA varie avec la "force d'ouverture" de la valve, c'est à dire avec la force
contractile du VG. La survenue de l'IVG aggrave donc la sévérité de la sténose. Cette
immobilisation des valves par les calcifications peut aggraver le RA congénital ou rhumatismal.
b) La surcharge de pression entraîne une HVG concentrique,
Elle permet le maintien pendant longtemps d'une fonction VG normale. La survenue d'une dysfonction
VG permet de diviser l'évolution en 2 périodes :
- Une phase compensée (Selon la loi de Laplace; T = (P x R)/e, l'augmentation de tension (T) due à
l'élévation de la pression VG (P) est compensée par une diminution du rayon (R) et une augmentation de
l'épaisseur de la paroi VG (e) par l'HVG concentrique) où les SF sont la conséquence directe de
l'obstruction : angor, syncopes. L'angor peut être fonctionnel ou dû à des sténoses coronaires.
Les syncopes résultent de la stimulation des mécanorécepteurs VG par l'hyperpression VG qui
provoque bradycardie et vasodilatation.
- Une phase décompensée marquée par l'apparition de la dyspnée. L'IVG accroît la sévérité de
la sténose.

Chapitre IIC, page 3
4. SIGNES FONCTIONNELS
Surviennent à l'effort
- Syncopes : 1er signe dans 15 % des cas
- Angor d'effort : 1/3 des cas fonctionnel,
1/2 secondaire à des sténoses coronaires
- Dyspnée: 1er signe d'IVG, tardif
5. SIGNES PHYSIQUES
6. SIGNES RADIOLOGIQUES
HVG concentrique donc n'augmentant pas le volume du coeur
Dilatation post-sténotique de l'aorte ascendante
Calcifications valvulaires
7. SIGNES ELECTROCARDIOGRAPHIQUES
HVG de type systolique (R en V5 > 30 mm, en V6 > 25 mm
et ondes T négatives et asymétriques (voir figure 4)
Troubles de la conduction intra-ventriculaire(bloc de branche G)
8. PHONO-MECANOGRAMME
N'est plus utilisé actuellement et montrerait les mêmes anomalies que les courbes de pression
VG et Ao.
1 - Allongement de la durée de l'éjection
2 - Diminution de la vitesse d'ascension du carotidogramme
3 - Allongement de l'intervalle R-pic du souffle (le maximum du souffle est comme le pic de
pression VG d'autant plus tardif que le RA est serré)
9. ECHO-DOPPLER
a) Écho
- En TM: Diminution de l'amplitude d'ouverture des valves sigmoïdes (mais souvent difficile à
affirmer en raison de la présence de calcifications)
- En Bi-D: HVG concentrique; l'échographie est plus sensible que l'ECG pour déceler l'HVG -
Éventuel fluttering de la valve mitrale antérieure du à une insuffisance aortique associée
b) Doppler
Continu : permet de mesurer le gradient transvalvulaire. En couplant cette donnée à la mesure
du diamètre de la chambre de chasse du VG à l'écho, il devient possible d'évaluer la surface de
l'orifice aortique. Il y a une bonne corrélation avec la surface valvulaire mesurée au KT par la
formule de Gorlin (Figure 2).
En cas d'insuffisance cardiaque sévère, les méthodes de calcul sous-estiment la surface
valvulaire (la surface réelle est un peu plus grande) car ces méthodes dépendent du débit
cardiaque qui est très diminué. La meilleure détermination de la surface valvulaire est fournie par
sa
planimétrie en ETO.
10. CATHETERISME
Gradient de pression entre le VG (hyperpression) et l'aorte (Fig 3)
Calcul de la surface de l'orifice valvulaire (formule de Gorlin)
11. COMPLICATIONS
Insuffisance cardiaque, mort subite, endocardite,
Embolies calcaires (œil : visibles au FO),
Angor sévère (possible maladie coronaire associée)
12. DIAGNOSTIC DIFFERENTIEL
Essentiellement topographique :
a) Données cliniques
- RA sous-valvulaire: souffle parasternal gauche, A2 présent, calcifications valvulaires
absentes.
- RA sus-valvulaire : exceptionnel ; dysmorphie associée.
b) 2 - Données échocardiographiques:
visualisation de la collerette sous-valvulaire ou sus-valvulaire.
c) 3 - Identification par le siège du gradient au KT
selon que la différence de pression s'établit entre
- 2 courbes de pression de morphologie ventriculaire: sous-valvulaire ;
- 2 courbes de morphologie aortique : sus-valvulaire ;
- 1 courbe ventriculaire et 1 courbe aortique: valvulaire

Chapitre IIC, page 4
A1
A 2
V1V2
VALVE
STÉNOSÉE
CHAMBRE DE
CHASSE VG AORTE
Figure 2 - Équation de continuité
A = surface de l'orifice; V = vitesse du flux; D = diamètre de l'orifice
L'équation de continuité établit que le débit cardiaque Q = A1 x V1 = A2 x V2,
Soit: A2 = (A1 x V1) / V2. A1 = 3,14 x (D12) / 4,
En pratique, pour un sujet moyen, D1 est de l'ordre de 2 cm et V1 de 1 m/s.
A2 est donc égal à (3,14 cm2 x 1m/ sec) /V2.
Si V2 a été mesurée à 6 m/sec, la surface de l'orifice est de : 0,52 cm2.
FIGURE 3 - Enregistrement de la pression dans le ventricule gauche, l'aorte et le capillaire pulmonaire dans un
rétrécissement valvulaire aortique. Noter la présence d'un gradient VG-Ao (70 mm Hg) et la survenue tardive du
pic systolique aortique.
13. CRITERES DE SEVERITE

Chapitre IIC, page 5
1. La présence des SF
2. Le frémissement systolique et la disparition de B2
3. Le B4 et la présence d'une HVG concentrique sont en général présents si le gradient est au moins
égal à 70 mmHg
4. L'écho-Doppler et le cathétérisme : Surface valvulaire :
< 0,7 cm2 : RA très serré
0,71 à 1,0 cm2 : RA moyennement serré
1,0 cm2 : RA non serré
En cas d'IVG sévère, la formule de Gorlin fournit une valeur de surface plus petite qu'elle n'est en réalité car la
formule n'est pas indépendante du flux. Il peut être difficile de déterminer si l'insuffisance cardiaque résulte
d'une autre étiologie ou d'une sténose aortique réellement serrée.
Si la surface valvulaire aortique n'a pu être calculée, le RA est serré si
le gradient est > 50 mmHg
à une IA significative est associé un gradient > 70 mmHg
à une IVG est associé un gradient > 30 mmHg
5 - Coronarographie systématique après 50 ans: présence de sténoses
14. EVOLUTION
En moyenne, la surface valvulaire diminue de 0,1 cm2 par an. Mais il y a de très grandes variations
individuelles.
Le RA congénital : En principe, la surface de l'orifice est déterminée à la naissance, mais une
progression de la sténose est possible en raison des calcifications surajoutées.
Le RA rhumatismal : Progresse très lentement ; l'accrétion calcaire diminue encore la mobilité des
valves.
Le RA calcifié sénile : Progression plus rapide que dans les 2 autres étiologies du fait des
calcifications massives et de la dépression de la fonction VG. Chez les dialysés, l'évolution est très
rapide (0,23 cm2/an)
15. TRAITEMENT
Remplacement valvulaire: lorsque le RA est serré et symptomatique, le plus souvent actuellement par
une valve à disque basculant (voir Fig 6 et 7)
Valvuloplastie à ballonnet: technique proposée par A Cribier chez les patients âgés, récusés par les
chirurgiens mais :
risque vital (> 10 %)
récidive à 6 mois: 70-80%; à 1 an: 80-90%
mortalité à 1 an: 40% du fait de la récidive
Patient âgé, ayant un RA serré, avec insuffisance cardiaque sévère ou choc cardiogénique:
valvuloplastie suivie de remplacement valvulaire.
 6
6
 7
7
1
/
7
100%