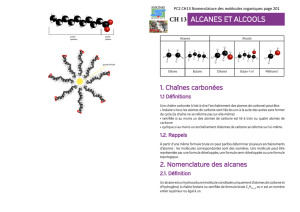
Alcanes et alcools

Alcanes et alcools
Notions et contenus
Compétences attendues
Nomenclature des alcanes et des alcools ; formule semi-développée.
Lien entre les températures de changement d’état et la structure
moléculaire dans le cas de l’eau, des alcools et des alcanes.
Miscibilité des alcools avec l’eau.
Reconnaître une chaîne carbonée linéaire, ramifiée ou cyclique.
Nommer un alcane et un alcool.
Donner les formules semi-développées correspondant à une formule
brute donnée dans le cas de molécules simples.
Interpréter :
- l’évolution des températures de changement d’état au sein d’une
famille de composés ;
- les différences de température de changement d’état entre les alcanes
et les alcools ;
- la plus ou moins grande miscibilité des alcools avec l’eau.
Reconnaître la classe d'un alcool.
Savoir que les molécules de la chimie organique sont constituées
principalement des éléments C et H.
I) Nomenclature des alcanes et alcools
1) Les alcanes
a) Rappels:
H: Z = 1 (K)1. Pour satisfaire à la règle du duet, H doit engendrer une liaison covalente H est monovalent.
C: Z = 6 (K)2(L)4. Pour satisfaire à la règle de l'octet, C doit engendrer 4 liaisons covalentes. C est tétravalent.
Nous allons rentrer ici dans le domaine de la chimie organique. Cette branche de la chimie qui étudiait autrefois
la chimie des composés issus des organismes a due être redéfinie depuis que le chimiste allemand Friedrich
Wöhler synthétisa en 1828 l'urée à partir de matière minérale et in vitro, remettant en cause le concept de force
vitale alors admis.
La chimie organique est donc aujourd'hui la chimie des composés du carbone (avec une forte proportion
d'hydrogène).
b) Les alcanes
Un alcane est un hydrocarbure (ne contient que des atomes C et H) saturé c'est-à-dire dont tous les atomes de
carbone engendrent 4 liaisons covalentes simples (C tétraédrique).
Le premier des alcanes est le méthane:
Formule brute: CH4 Formule développée: Représentation de Cram:
Vient ensuite l'éthane:
Formule brute: C2H6 Formule développée: Représentation de Cram:
On utilise aussi la formule semi-développée où on ne représente que les liaisons C – C: CH3 – CH3
Ainsi que la formule topologique où on représente le liaisons C – C par des traits: –
Représenter les formules semi développées, topologiques et les représentations de Cram des alcanes de
formules brutes C3H8 et C4H10. Pour ce dernier, n'y a-t-il qu'une seule possibilité?
Des isomères sont des molécules ayant même formule brute et des formules développées différentes.
Ce sont deux molécules aux propriétés physiques et chimiques différentes.
Il y a une molécule qu'on qualifie d'alcane linéaire et l'autre d'alcane ramifié.
La formule générale d'un alcane est CnH(2n+2).
Il existe aussi des alcanes cycliques dont la formule générale sera CnH2n. Exemple: le cyclohexane:
c) Nomenclature des alcanes
- Alcanes linéaires
Un préfixe correspondant au nombre d'atomes de carbone est suivi de la terminaison "ane":
nbre d'atomes de C
1
2
3
4
5
6
7
8
9
10
11
12
20
Préfixe
méth
éth
prop
but
pent
hex
hept
oct
non
dec
undec
dodec
eicos
- Alcanes ramifiés
Identifier la chaîne carbonée la plus longue.
Repérer le ou les radicaux substitués et numéroter la chaîne de manière à ce que les radicaux soient affectés
des numéros les plus petits possibles.

On donne le nom en écrivant dans l'ordre alphabétique les noms des radicaux avec leurs positions puis le nom
de la chaîne carbonée la plus longue.
Exemple: donner le nom des molécules suivantes:
A l'inverse, représenter le 3-méthyl,4-éthylhexane.
2) Les alcools
Les alcools sont des molécules organiques possédant le groupe caractéristique hydroxyle: – OH et dont le
carbone porteur de ce groupe caractéristique n'est lié à aucun autre groupe caractéristique ni engagé dans une
liaison multiple.
On distingue trois classes d'alcools:
Alcools primaires
Alcools secondaires
Alcools tertiaires
Le C porteur du groupe hydroxyle
est lié à un seul autre atome de
carbone
Le C porteur du groupe hydroxyle
est lié à deux autres atomes de
carbone
Le C porteur du groupe hydroxyle
est lié à trois autres atomes de
carbone
R – CH2 – OH
Nomenclature: on retrouve les mêmes règles que pour les alcanes avec la terminaison "ol" au lieu de "ane".
Concernant la numérotation, le groupe hydroxyle est prioritaire sur les radicaux alkyle. Il sera affecté du plus
petit numéro possible.
Exemples:
Représenter les molécules de: propan-2-ol, de 2-méthylpropan-2-ol et de 2-méthylbutan-1-ol.
Nommer les molécules suivantes:
II) Changements d'états
1) Molécules linéaires
Les alcanes et les alcools à chaîne carbonée linéaire ont des températures de changement d'état d'autant plus
grandes que leur chaîne carbonée est longue. En effet, il y aura davantage d'interactions (forces de Van Der
Waals) entre les molécules si le nombre d'atomes de carbone est élevé.
Pour un nombre d'atomes de carbone identiques, les alcools sont bien moins volatils que les alcanes. En effet, la
présence d'un atome d'oxygène crée davantage de liaisons hydrogène entre les molécules.
Alcanes
eb (°C)
Alcane ou alcool
eb (°C)
Méthane (CH4)
-161
Ethane (CH3-CH3)
-89
Butane (CH3-(CH2)2-CH3)
0
Ethanol (CH3-CH2OH)
78
Hexane (CH3-(CH2)4-CH3)
69
Pentane (CH3-(CH2)3-CH3)
36
Octane (CH3-(CH2)6-CH3)
126
Pentan-1-ol (CH3-(CH2)3-CH2OH)
138
2) Molecules ramifiées
La ramification des chaînes conduit à un abaissement des températures de changement d'état. Ceci est encore dû
aux forces de Van Der Waals.
Molécule
eb (°C)
Octane
(CH3-(CH2)6-CH3)
126

Isooctane
99
Pentan-1-ol
(CH3-(CH2)3-CH2OH)
138
Alcool isoamylique
132
Donner les noms en nomenclature officielle de l'isooctane et de l'alcool isoamylique.
3) Miscibilité des alcools avec l'eau
Rappel: deux liquides sont miscibles si ils ne présentent qu'une seule phase lorsqu'on les mélange (mélange
homogène).
L'eau et l'éthanol sont miscibles alors que l'eau et le cyclohexane ne le sont pas (revoir cours de seconde sur
l'extraction).
La présence d'un atome d'oxygène dans la molécule d'alcool permet d'engendrer des liaisons hydrogène avec
l'eau ce qui va permettre la solvatation.
Cependant, le caractère hydrophobe de la chaîne carbonée va finir par l'emporter et limiter cette miscibilité.
Au delà de trois atomes de carbone, la miscibilité n'est plus infinie:
Alcool
Solubilité massique
dans l'eau (g.L-1)
Ethanol
CH3-CH2OH
Propan-1-ol
CH3-CH2-CH2OH
Butan-1-ol
CH3-(CH2)2-CH2OH
80
Pentan-1-ol
CH3-(CH2)3-CH2OH
22
Hexan-1-ol
CH3-(CH2)4-CH2OH
6
1
/
3
100%