cours - profdephysique

!" #$%&'(" &) &*#'# '" !%#%!) #' *%# "#
%"'%**
✔&!+%,&)-') '!+%("%)-!%#.&-%
!+%,&&/)' ("/0-"1%)-!%#.&%"%1'"2
✔& !+%,& ) -') ' "& " *"'"# %) -
!%#.&&)' 0*"--"1%)-!%#.&2
✔&!+%,&)-') '% !"!&3&)%"'&
"&!4!
&)-!* #$%&'("%!4!'("%&!4!-5#".#")
$ & #% &6&768& ) "&&.#&3#"* #'"#" $% 0 %&"&%!%&
)")'%'&9&)-'%'&'*
&) - !* #$%&'(" ("' *# &)&) "&
("'):1 "#"&%)-!%#.&) )#%$&%
"#5#"$ & #%) 89)"&!+%,&!%#.& '& %'#"#%':
#;$-&&!%)"#*#<&)-&#%!%&)%!!5
=):!+ )+->
?/
!!"
"'&-/"&@5%'-!* )* #%)"#-!+%&$&)-/ )%)
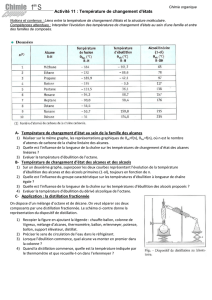
•!%A!%&$""#-%!+%,&!%#.& 2
•!("%&-&.#-#%':!%3&%"$&)
"#"& @!+%,&!%#.& %!&)- )* #%)"#-!+%&$&)
-/ )%)"* #'"# 0 ! - %!%& &)-&! '& (" %!%&
!##*&-%&)
#!$
%& %!%& ' &/4 % (" - '&)#%!3& - % & /'&)&') -
'&)#%!3&-B%&-#C%% !%A!%&$""#-%!+%,&!%#.& 2*%#
!&)#*"%!+%,&)#%': *""#'&)&') ! !"&)*"
-%0#%**#!+#
%&%!'4%&*"- '-"0%*# &!-"$#"*
+4-#149'&''5%")*"-/ &#$'*"##*#!'%'&) '$&#
!"-/%!("*"#"&%!%&')"&)* #%)"#-!+%&$&)-/ )%)
"* #'"#
( )
&-'3%3&5#%!3&& )"&)!+&'("
("' *#) - *%## !&3)"%&) -/"&
%&$ - '("'- '!'. %4%&) -
)* #%)"# -/ ."'3& &<&)
-'D #&) !%#)-/%"'&6E
-'D #&) *%#3 -" &)%$ -
-'3%3&)"##F&)
!
!
G%&)
!+%"DH
.%&
&&
-B'$#"1
@)-!&&
"&'-/"&
)+#;)#
5#'$ #%&) %!&
#!A"#
* !+%"D%$ *%#%3& "#-%
)* #%)"# '(" 5%!3& !)-"
-'3%)
G/
"1'("'-&)'!'./'5#&)"& %&$!'
%!%&&)- !" '&&)*%'!'.%A!/%"("')
"&A%&)*%'#*%-/'&)#%!3&&)#%!%&)/%"
%'!'.'') -%!%A!/%"# ")-/1')&!- '&)#
!" -/%" ) $#"* +4-#14 9 - /%! !/) !%#%!);#
IJ-/%!
% ".'') - %! -%& /%" "# !%*%!') 0 %&$# %A! /%"
!%A!%&$""#-%!+%,&!%#.& %!+%,&!%#.& -/%!&/%
*%-/%K&') %A!/%"!/)!%#%!);#IJ-/%!
+!,-
•%A'##!&&%,)#"&!+%,&!%#.& '& %'##%': "!4!'("
•%A'#'-&3:#)&#"&%!%&)"&%!
•%A'# -&&# 5#" 'H- A** !##*&-%&) 0 "& 5#"
.#")-&& -%&!%- !"'*
•&)#*# )# / A"3& - )* #%)"# - !+%&$&) -/ )%) %" '& -/"&
5%'-!* %!3A')
•&)#*# )# -'D #&! - )* #%)"# - !+%&$&) -/ )%) &)#
%!%&)%!%!3A')
•&)#*# )#%*""'&$#%&-'!'.'') -%!%A!/%"
•
-./0/102/3103
'& %'#
#%':
!4!'("
1
/
1
100%