imagerie

Harmand Jonathan
Gadzo Edin
Physique, Imagerie scintigraphique par gamma-caméras
Pr Garin
Imagerie scintigraphique par
gamma-caméras
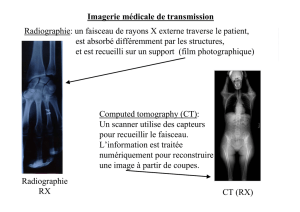
I- Introduction
L’intérêt de la Médecine Nucléaire pour la radioactivité a suivi de peu sa découverte. Dès 1913,
Georges de Hevesy, chimiste suédois, eut l’idée d’employer des radionucléides comme indicateurs
pour suivre la circulation du sang dans l’organisme. Cependant, il a fallu attendre la fin des années
quarante pour que l’Iode 131 provenant des réacteurs nucléaires soit disponible et qu’en conséquence
l’étude de sa fixation dans la glande thyroïde soit aisément réalisable. Mais ce n’est que dix ans plus
tard, après l’invention d’Anger d’une gamma-caméra capable de produire des images corrélables au
fonctionnement des organes que l’on peut parler des applications de l’imagerie scintigraphique au
diagnostic médical. En effet, il devint possible d’enregistrer simultanément tous les points de la région
explorée et ensuite de suivre l’évolution de la radioactivité dans les différentes parties de l’organisme.
a) Principe de la scintigraphie
La scintigraphie repose sur la détection externe d’un traceur radioactif administré au patient, on en
distingue 2 types :
– Emetteurs g : scintigraphie par gamma caméra
– Emetteurs de positions : scintigraphie par caméra TEP (Tomographie d’Emission
Photonique)
NB: La Médecine Nucléaire regroupe l’ensemble des méthodes diagnostiques (scintigraphies) et
thérapeutiques (radiothérapie métabolique) qui nécessitent l’utilisation d’isotopes radioactifs en
sources non scellées.
Le principe physique de détection est la scintillation solide, c.a.d une détection faisant appel a des
photons lumineux.
Chaque traceur possède des propriétés biologiques qui lui sont propres
La scintigraphie est une technique d’imagerie fonctionnelle qui permettra l’analyse du
fonctionnement biologique d’une structure.

b) Notion de traceur
Un traceur est constitué soit de l’atome radioactif pur appelé marqueur (ex iode 131), ou fixé par
liaison chimique à une molécule d’intérêt biologique appelé vecteur.
Mode d’administration :
– Injection intraveineuse +++
– Aérosol (scintigraphie de ventilation pulmonaire)
– Voie orale (scintigraphie gastrique)
Chaque traceur aura une captation préférentielle par un organe, par exemple :
99mTc-HMDP = activité osseuse ostéoblastique utile pour la scintigraphie osseuse
99mTc-MAA = embolisation vasculaire utile pour la scintigraphie pulmonaire de perfusion)
111In-pentétréotide (analogue de la somatostatine) = fixation sur les récepteurs de la somatostatine pour
détecter les tumeurs endocrines
c) Choix du radioélément
Le choix du radioélément se fera fonction de plusieurs facteurs :
Type d’imagerie :
Pour les émetteur de photons g , on parle alors de scintigraphie gamma, on en retrouve 2 types :
– imagerie 2D : Scintigraphie planaire:
– imagerie 3D : Tomographie d’Emission MonoPhotonique, TEMP,
Pour les émetteurs de positon on parle de TEP:
– imagerie 3D exclusive : Tomographie par Emission de Positon TEP
La demie-vie ou période T: elle est de qlq secondes à tout au plus qlq mois.
La plus courte possible pour diminuer l’irradiation, mais adaptée au phénomène que l’on veut étudier
(ex: étude fonctionnelle sur plusieurs jour => demi-vie prolongée)
Période effective, Te:
Prise en compte de :
- la décroissance radioactive T du radionucléide
- et de l'élimination biologique propre à l'organe cible. Tb
En première approximation, on considère que l'élimination biologique obéit à une loi exponentielle de
période biologique Tb, qui est le temps nécessaire pour que la moitié de la quantité d'une substance
introduite dans un organe en soit éliminée.
1 1 1
____ =___ +___
Te T Tb
Radiotoxicité : c’est la propriété des radionucléides à générer des dommages aux tissus, ceci est
fonction :

– du type de rayonnement émis (X, g, e < neutron < a )
– nature du tissu irradié (localisation dans l’organisme)
Coût de production
– Générateur (99mTc), réacteur (iode 131) : faible coût
– Cyclotron (Thallium 201, iode 123, fluor 18): coût élevé
d) Délais administration du traceur/ imagerie
Immédiatement après injection :
- scintigraphie osseuse dynamique
- étude de la perfusion rénale
- étude du premier passage cardiaque
Quelques heures après administration
- scintigraphie osseuse: 2h
- scintigraphie rénale DMSA: 6h
Sur plusieurs jours:
- scintigraphie à l’111In-pentétréotide
- durée de vie des plaquettes
II- La gamma caméra
Rappel :

Effet Compton

a) Cristal
Le cristal arrête les photons g et restitue l’énergie déposée par ces derniers sous forme de photons
lumineux, d’énergie différente de l’énergie absorbée.
Pour augmenter la probabilité d’interaction, on introduit des impuretés dans le cristal (ex Tl).
La fluorescence est le seul processus de désexcitation suffisamment rapide pour être exploité en
spectroscopie.
Pour obtenir cette fluorescence on distingue 2 types d’interaction :
-effet Campton
-effet Photo-electrique
Le scintillateur idéal :
-Fort pouvoir d’absorption pour l’énergie du rayonnement détecté - numéro atomique et densité élevés
(t/r # k. Z3/E3, loi de Bragg et Pierce)
---> Bonne efficacité de détection dans le cristal
-Efficacité de conversion importante, c.a.d forte aptitude à transformer l’énergie du rayonnement
incident en énergie lumineuse
---> Permet une bonne résolution en énergie
-Faible constante de décroissance (la constante de temps représente le temps moyen qui sépare le
moment où la radiation est absorbée de celui où la scintillation est émise)
-Un indice de réfraction proche de celui du verre (1.5) afin de faciliter le couplage avec le
photomultiplicateur
-Matériau facile à usiner en grandes dimensions
On utilise aujourd’hui le cristal NaI(Tl)
Plus le cristal est épais, plus l’efficacité de détection augmente, MAIS plus la diffusion, entraînant une
mauvaise localisation des événements, augmente aussi.
Les gamma caméras sont optimisées (nature et épaisseur du cristal) pour la détection du 99mTc.
b) Guide de lumière
L’efficacité de collection de la lumière par les PM (PhotoMultiplicateurs ) dépend de la façon dont ils
sont couplés au cristal.
1ier rôle: Réduire la perte de lumière:
Les premières caméras possédaient un PM circulaires, il y avait donc un espace libre relativement
important entre eux. Pour réduire cette perte, une plaque de verre est placée entre le cristal et les PM,
avec des joints optiques (graisse de silicone)
2iéme rôle: Adaptation de l'indice de réfraction entre le cristal NaI (indice très élevé) et le vide des
photomultiplicateurs (indice = 1).
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
1
/
18
100%