poly de cours

1S Chapitre …. : Introduction à la chimie organique
I. Généralités
Les substances organiques sont formées d’un nombre limité d’éléments chimiques : on y trouve
toujours le ………………………………………….., généralement accompagné de l’hydrogène …...
On peut aussi y trouver de l’oxygène …, de l’azote ….., du chlore …., etc.
La chimie organique regroupe l’ensemble des techniques d’extraction, d’analyse et de synthèse des
molécules à base de carbone.
Les ressources de molécules organiques sont principalement :
Non renouvelables : …………………………………………………………………………..……………….
Renouvelables : …………………………………………………………………………………………………….
II. Les liaisons chimiques :
Dans les molécules organiques, les éléments chimiques sont reliés par des ……………………..….………………
Chaque élément chimique fait toujours le même nombre de liaisons covalentes (règle du duet et de
l’octet)
Elément chimique
Nombre de
liaisons
covalentes
Valence
Représentations possibles
Carbone …………….
Hydrogène …………….
Oxygène ……………..
Azote …………………
« les halogènes » :
…………………………………….
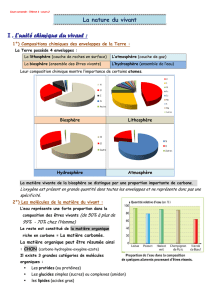
III. Composition massique
Un composé organique peut être défini par sa composition massique : c’est le pourcentage de la
masse de chaque élément chimique par rapport à la masse totale du composé :
Exemple : pour le méthane CH4 : %C =
% H=

1S Chapitre …. : Introduction à la chimie organique
I. Généralités
Les substances organiques sont formées d’un nombre limité d’éléments chimiques : on y trouve
toujours le ………………………………………….., généralement accompagné de l’hydrogène …...
On peut aussi y trouver de l’oxygène …, de l’azote ….., du chlore …., etc.
La chimie organique regroupe l’ensemble des techniques d’extraction, d’analyse et de synthèse des
molécules à base de carbone.
Les ressources de molécules organiques sont principalement :
Non renouvelables : …………………………………………………………………………..……………….
Renouvelables : …………………………………………………………………………………………………….
II. Les liaisons chimiques :
Dans les molécules organiques, les éléments chimiques sont reliés par des ……………………..….………………
Chaque élément chimique fait toujours le même nombre de liaisons covalentes (règle du duet et de
l’octet)
Elément chimique
Nombre de
liaisons
covalentes
Valence
Représentations possibles
Carbone …………….
Hydrogène …………….
Oxygène ……………..
Azote …………………
« les halogènes » :
…………………………………….
III. Composition massique
Un composé organique peut être défini par sa composition massique : c’est le pourcentage de la
masse de chaque élément chimique par rapport à la masse totale du composé :
Exemple : pour le méthane CH4 : %C =
% H=
1
/
2
100%