Synthèse du Paracétamol : Fiche d'Activité Expérimentale

Auteur : Brigitte VRAY Académie de LYON
FICHE 1 PRÉSENTATION
Titre
SYNTHESE DU PARACETAMOL
Type d'activité
Activité expérimentale
Objectifs de
l’activité
Mettre en évidence le caractère sélectif ou non d’une réaction.
Pratiquer une démarche expérimentale pour synthétiser une molécule organique d’intérêt
biologique à partir d’un protocole.
Références par
rapport au
programme
Cette activité illustre le thème : AGIR / Défis du XXIème siècle
et le sous thème : Synthétiser des molécules, fabriquer de nouveaux matériaux
en classe de terminale S
Notions et contenus
Sélectivité en chimie organique
Composé polyfonctionnel : réactif
chimiosélectif, protection de fonctions.
Compétences exigibles
Extraire et exploiter des informations :
- sur l'utilisation de réactifs
chimiosélectifs,
- sur la protection d’une fonction dans le
cas de la synthèse peptidique,
pour mettre en évidence le caractère sélectif ou
non d’une réaction.
Pratiquer une démarche expérimentale pour
synthétiser une molécule organique d’intérêt
biologique à partir d’un protocole.
Conditions de mise
en œuvre
Prérequis :
Savoir reconnaître les groupes caractéristiques dans les acide carboxylique, amine, amide.
Savoir déterminer la catégorie d’une réaction (substitution, addition, élimination) à partir de
l’examen de la nature des réactifs et des produits.
Protocole de synthèse organique :
- identification des réactifs, du solvant, du catalyseur, des produits ;
- détermination des quantités des espèces mises en jeu, du réactif limitant ;
- choix des paramètres expérimentaux : température, solvant, durée de la réaction, pH ;
- choix du montage, de la technique de purification, de l’analyse du produit ;
- calcul d’un rendement ;
- aspects liés à la sécurité
Durée : 2h
Contraintes matérielles : salle de chimie équipée
Remarques
Cette synthèse se faisait déjà en enseignement de spécialité.
Elle est tout à fait réalisable en 2h dans une salle de chimie équipée.
Les questions portant sur la transformation elle-même peuvent être traitées avant, soit en
travail à la maison, soit en classe.
Auteur
Brigitte VRAY
Académie de LYON

Auteur : Brigitte VRAY Académie de LYON
FICHE 2 LISTE DU MATÉRIEL
TITRE DE L’ACTIVITÉ
SYNTHESE DU PARACETAMOL
Le matériel nécessaire aux manipulations disposé sur la paillasse du professeur.
Le matériel nécessaire aux manipulations disposé sur la paillasse des élèves.
gants et lunettes
une éprouvette de 5 mL
une éprouvette de 10 mL
une éprouvette de 50 mL
un cristallisoir
un dispositif pour filtration sous pression réduite avec rondelles de papier filtre
2 erlenmeyers de 100 mL
une spatule
un agitateur magnétique chauffant + barreau aimanté
une coupelle
une baguette de verrre
pissette d’eau distillée
glace
1 thermomètre de 0°C à 110°C
eau distillée glacée
pince en bois, en métal ou gants isolants

Auteur : Brigitte VRAY Académie de LYON
FICHE 3 FICHE POUR LE PROFESSEUR
TITRE DE L’ACTIVITÉ
SYNTHESE DU PARACETAMOL
La transformation chimique :
Le paracétamol est synthétisé au laboratoire à partir d’anhydride éthanoïque et de 4-aminophénol.
L’équation associée à la réaction s’écrit :
NH2
OH
O
O
O
C
C
H3C
H3C
O
CH3COH
O
CH3C
NH OH
++
4-aminophénol anhydride éthanoïque paracétamol acide éthanoïque
Réflexions préalables :
Les amines réagissent avec les anhydrides d’acide pour conduire à des amides. La transformation associée à cette
réaction est rapide et totale.
L’acylation directe d’une amine par un acide carboxylique est difficile à réaliser. En effet, la réaction acide-base
entre l’acide et l’amine conduit à la formation du carboxylate d’ammonium. Ainsi disparaissent à la fois le
caractère nucléophile de l’amine et le caractère déjà faiblement électrophile de l’acide.
Données :
Rechercher les fiches de toxicité des composés suivants et compléter le tableau de données :
4-aminophénol
anhydride éthanoïque
acide éthanoïque.
Composé
Aspect à 25°C
et sous 105 Pa
(1 bar)
Risques
Solubilité dans
l’eau
Température
de fusion
Température
d'ébullition
Masse
molaire
en g.mol-1
4-aminophénol
solide blanc
Nocif par
contact,
inhalation et
ingestion
8 g.L-1 à 20°C
33 g.L-1 à 60°C
85 g.L-1 à 100°C
186 °C
109
Anhydride
éthanoïque
Liquide
incolore
Densité: 1,08
Corrosif,
inflammable,
irritant
réagit avec l’eau en
donnant l’acide
dont il est issu
-73°C
136 °C
102
Paracétamol
solide blanc
10 g.L-1 à 20°C
250 g.L-1 à 100°C
168 °C
151
Acide
éthanoïque
liquide
incolore
Corrosif,
inflammable,
irritant
Très grande
solubilité de 0° C à
100°C
17 °C
60
Justifier les états physiques de l'anhydride éthanoïque et du 4-aminophénol à température ambiante (20 °C).
L'anhydride éthanoïque est liquide car sa température de fusion est inférieure à 20 °C et sa température
d’ébullition supérieure à 20 °C. Le 4-aminophénol est solide car sa température de fusion est supérieure à 20 °C.

Auteur : Brigitte VRAY Académie de LYON
Sécurité :
Quelles précautions faut-il prendre lors de cette synthèse ?
Il faut se protéger avec des gants, des lunettes, une blouse et manipuler sous une hotte aspirante.
Protocole expérimental :
1. Dissolution du 4-aminophénol
Dans un erlenmeyer, on introduit 5,45 g de 4-aminophénol, 50 mL d’eau et 3,5 mL d’acide éthanoïque.
Après avoir adapté sur l’erlenmeyer un réfrigérant à air, le mélange est placé sous agitation dans un bain-marie à
80°C pendant 10 minutes.
2. Obtention du paracétamol brut
Sous la hotte et tout en agitant, enlever le réfrigérant à air et ajouter lentement environ 7 mL d’anhydride
éthanoïque au mélange précédent. Le mélange s’échauffe un peu.
L’addition terminée, adapter le réfrigérant à air et porter le mélange au bain-marie à 80°C pendant 10 minutes.
3. Cristallisation du paracétamol
Refroidir le mélange réactionnel dans un bain d’eau glacée et attendre la cristallisation complète (on amorcera
éventuellement celle-ci en grattant les parois de l’erlenmeyer avec un agitateur en verre).
Filtrer sur filtre Büchner (sous pression réduite).
Rincer le solide avec un minimum d’eau glacée, puis le récupérer dans un erlenmeyer.
4. Purification du paracétamol
Dans l’erlenmeyer contenant le solide à purifier, introduire au maximum 20 mL d’eau distillée préalablement
chauffée et continuer à chauffer le mélange placé sur un agitateur magnétique chauffant.
Si la dissolution du solide n’est pas totale, ajouter encore 5 mL d’eau très chaude.
Procéder à la cristallisation lente du paracétamol purifié.
Filtrer sous pression réduite les cristaux obtenus et les récupérer dans une coupelle préalablement pesée.
Sécher les cristaux dans une étuve à 80 °C. Peser les cristaux secs.
5. Caractérisation du produit par CCM
Eluant : mélange CHCl3 (chloroforme) et CH3OH (méthanol) : 60/40 en volume.
Echantillons : 1 mL d’éluant + une pointe de spatule de 4-aminophénol
1 mL d’éluant + une pointe de spatule de paracétamol synthétisé et purifié
1 mL d’éluant + une pointe de spatule de paracétamol du commerce.
Révélation sous UV ( = 254 nm)
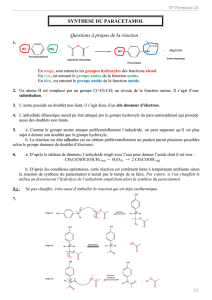
Questions à propos de la réaction :
1. Entourer et nommer les groupes fonctionnels caractéristiques présents dans la molécule de 4-aminophénol et
dans celle du paracétamol.
2. Justifier l’emploi de l’anhydride éthanoïque pour effectuer l’acylation du 4-aminophénol.
Le 4-aminophénol possède un groupe amine, l’acylation avec l’anhydride éthanoïque est alors rapide et totale.
3. A partir de la nature des réactifs et des produits, déterminer si cette réaction correspond à une :
x substitution ? □ addition ? □ élimination ?
4. Le caractère de l’azote est-il nucléophile ou électrophile dans cette réaction ?
L’azote dans le groupe amine a un caractère nucléophile.
5. L’anhydride éthanoïque aurait-il pu réagir de façon différente ?
L’anhydride pourrait agir sur le groupe –OH du 4-aminophénol .
6. En déduire si le groupe –OH est plus ou moins nucléophile que le groupe –NH2 ?
Le groupe –OH est moins nucléophile que le groupe –NH2 .

Auteur : Brigitte VRAY Académie de LYON
7. La synthèse s’effectue en milieux aqueux.
a) En utilisant le tableau de données, écrire l’équation de la réaction entre l’anhydride éthanoïque et l’eau.
CH3-CO-O-CO-CH3 + H2O = 2 CH3COOH
b) D’après les conditions opératoires, quelle conclusion peut-on donner quant à la cinétique de cette
réaction ?
L’anhydride éthanoïque s’hydrolyse lentement en milieu aqueux à température ambiante.
Questions à propos du protocole :
1.1. Quel est le rôle de l’acide éthanoïque ?
L’acide éthanoïque joue le rôle de solvant.
1. 2. Pourquoi chauffe-t-on le mélange après l’ajout d’acide éthanoïque ?
La solubilité du 4-aminophénol augmente avec la température.
2.1. Calculer les quantités initiales des réactifs. Déterminer le réactif limitant.
ni (4-aminophénol) = m / M = 5,4 / 109 = 5,0.10-2 mol
ni (anhydride éthanoïque) = (eau × d × V) / M = (1,0 × 1,08 × 7) / 102 = 7,4.10-2 mol
On remarque que ni (anhydride éthanoïque) > ni (4-aminophénol), or 1 mol d’anhydride éthanoïque réagit avec 1
mol de 4-aminophénol ; le 4-aminophénol est le réactif limitant.
2.2. Quelle masse de paracétamol pourrait-on alors obtenir ?
m (paracétamol) = 5,0.10-2 × 151 = 7,5 g
2.3. Indiquer la verrerie utilisée pour mesurer : 50 mL d’eau,
3,5 mL d’acide éthanoïque,
7 mL d’anhydride éthanoïque.
Ces 3 volumes ne demandent pas une grande précision, car ces composés sont utilisés soit comme solvant, soit en
excès, donc on utilisera une éprouvette graduée de 50 mL pour mesurer 50 mL d’eau, une éprouvette graduée de
10 mL pour mesurer 3,5 mL d’acide éthanoïque et 7 mL d’anhydride éthanoïque.
2.4. Comment élimine-t-on l’excès d’anhydride éthanoïque en fin de réaction ?
Le mélange réactionnel est chauffé, ce qui permet d’accélérer l’hydrolyse de l’anhydride éthanoïque.
3.1. Pourquoi utilise-t-on de l’eau glacée pour faire apparaître les cristaux ?
La cristallisation d'un solide dans un mélange est sa formation par diminution de sa solubilité dans le mélange.
La diminution de la solubilité du solide peut-être due à une variation de température, une variation de pH ...
L'existence d'impuretés dans la solution (particules de verre …) favorise aussi la cristallisation.
Le paracétamol est peu soluble dans l’eau froide.
 6
6
 7
7
 8
8
 9
9
1
/
9
100%