Aucun titre de diapositive

Pr D. BORDESSOULE 2005-2006
l ’ERYTHROPOIESE

Pr D. BORDESSOULE 2005-2006
Hématologie
A. Erythrocytes; C/E. Neutrophile; D. Eosinophile; J. Basophile; F. Monocyte;
B. H. Lymphocyte; B. Lymphocyte à grains; I. Band Neutrophil;
C. G. Platelets;

Pr D. BORDESSOULE 2005-2006
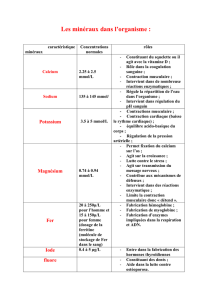
Eléments nécessaires à l ’érythropoïèse
Le fer
nécessaire à la synthèse de l' Hémoglobine.
2 - La vitamine B12 + folates
nécessaires dans les synthèses de DNA.
3 - Les autres vitamines
Vitamine B6 nécessaire à:
Îla synthèse de Hémoglobine.
Îincorporation du fer dans la protoporphyrine III.
Vitamine C
Îrôle dans le métabolisme du Fer
Riboflavine
l ’ERYTHROPOIESE

Pr D. BORDESSOULE 2005-2006
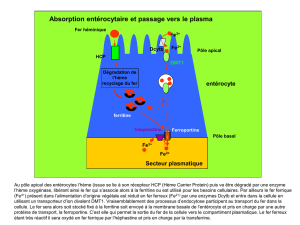
Le métabolisme du fer joue un rôle important dans
l'organisme par sa participation à la synthèse
d'hémoglobine.
Sa fonction essentielle est le transport de l’Oxygène
I - Répartition du fer dans l'organisme
II - Etude dynamique du fer
III – Régulation du métabolisme du fer
IV- Exploration du métabolisme du fer
)Compréhension du mécanisme
-des anémies microcytaires
-des hémochromatoses
)Actualités en recherche fondamentale:
le fer est vital+++
mais toxique+++
FER

Pr D. BORDESSOULE 2005-2006
:
Quantité totale de fer dans l'organisme
=
3 à 4 g chez l'adulte
.
Fer libre très toxique +++
complexé avec des protéines dans les milieux
extra et intra-cellulaires.
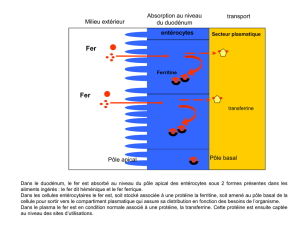
Fer réparti en plusieurs compartiments :
ªcompartiment fonctionnel : 70 %
érythroblastes et hémoglobine
ªcompartiment de stockage : 30 %
ferritine ou hémosidérine
ªcompartiment de transport : 0,1 %
transferrine ou sidérophilline
I- Répartition du fer dans l'organisme
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
1
/
33
100%