Anticorps anti-nucléaires et diagnostic des maladies auto

INTRODUCTION
Les auto-anticorps anti-nucléaires (AAN) apparaissent au cours d’un grand
nombre de pathologies auto-immunes. Ils sont dirigés contre des structures très
variées présentes dans le noyau : ADN, ribonucléoprotéines, protéines...
L’apparition de ces auto-anticorps signe un dérèglement du système
immunitaire, supposant une rupture de la tolérance aux antigènes du "soi".
Exceptionnellement pathogènes par eux-mêmes (certains anticorps anti-ADN
sont impliqués dans la genèse de la glomérulonéphrite lupique), ils constituent
des stigmates d’auto-immunisation et sont de bons marqueurs biologiques,
utiles pour le diagnostic et le suivi des patients.
Parmi les maladies de système, on reconnaît divers cadres nosologiques : lupus
érythémateux aigu disséminé (LED), polyarthrite rhumatoïde (PR), syndrome de
Gougerot-Sjögren (SGS), syndrome des anticorps antiphospholipides,
sclérodermie systémique, connectivite mixte (CM), dermato-polymyosite… La
définition de ces entités est fondée à la fois sur des critères cliniques et
biologiques. Parmi ces derniers, certaines catégories d’AAN tiennent une part
importante, permettant d’orienter le diagnostic et parfois de l’affirmer.
I - QUELLES SONT LES INDICATIONS DE LA RECHERCHE DES
ANTICORPS ANTI-NUCLEAIRES ?
Les AAN peuvent être mis en évidence dans 3 types de situations :
-les grandes maladies auto-immunes déjà citées : la découverte d’AAN
constitue alors un argument diagnostique.
-les pathologies autres que les maladies systémiques : cancers, leucémies
aiguës, hépatopathies, insuffisances rénales, infections diverses (notamment à
parvovirus B19 ou à EBV).
-les sujets apparemment sains, quel que soit leur âge (la proportion de sérums
positifs n’augmente pas notablement jusqu’à 60 ans). Chez la femme enceinte,
un résultat positif de la recherche d’AAN peut aussi être observé en l’absence
de maladie auto-immune.
Le diagnostic
Dès que le clinicien soupçonne l'existence d'une maladie auto-immune, cet
examen devient légitime. C'est néanmoins l'identification des antigènes
reconnus par l’AAN qui lui apportera le plus d'informations. Celles-ci ne seront
interprétables qu'une fois réinsérées dans le contexte clinique et radiologique
qui aura justifié l'examen : lupus, syndrome de Gougerot-Sjögren, polyarthrite
rhumatoïde, dermato-polymyosite, connectivite mixte…
La recherche des AAN peut avoir, au contraire, pour objet d'éliminer une
maladie auto-immune (et non plus d'en confirmer la réalité). En l'occurrence, le
praticien relève des symptômes susceptibles d'apparaître à l'occasion d'une
maladie auto-immune, mais également d'accompagner le cours d'une affection
inflammatoire mais non auto-immune (le dilemme entre polyarthrite rhumatoïde
débutante et pelvispondylite rhumatismale avec atteintes périphériques illustre
ce type de situation). S'il n'y a pas d'AAN, il semble déraisonnable de retenir le
diagnostic de maladie auto-immune, bien que cette situation s'observe dans
environ 5 % des cas de lupus.
Le pronostic et l’évolution sous traitement
Il est parfois utile de répéter les dosages d'AAN, que ceux-ci aient été dépistés ou
non dès le premier examen. Le meilleur exemple est celui du lupus induit par un
médicament, où l'amélioration parallèle des symptômes cliniques et des anomalies
biologiques à l’arrêt du traitement permet d'imputer la maladie au médicament.
Dans le cas du suivi d’un syndrome de Raynaud, la mise en évidence d’AAN pourra
permettre la détection de la forme CREST d’une sclérodermie systémique (qui
associe Calcinose sous-cutanée, syndrome de Raynaud, dysfonctionnement de
l’oEsophage, Sclérodactylie et Télangiectasies).
Remarque : Certaines catégories d’AAN ont aussi un intérêt particulier dans ce
cadre.
-La présence d’Ac anti-histones évoque fortement un lupus induit, de moindre gravité
qu’un LED.
-La présence d’Ac anti-Jo1 au cours d’une polymyosite suggère une atteinte
pulmonaire interstitielle et fait redouter une corticorésistance (50% des cas).
-L’existence d’Ac anti-Ro (ou SSa) chez une femme enceinte doit faire rechercher un
BAV congénital chez le fœtus entre 16 et 20 semaines de grossesse.
-La présence d’Ac anti-centromères est en faveur d’un CREST syndrome, de meilleur
pronostic que la sclérodermie systémique (où les atteintes rénales sont plus
fréquentes).
-Dans le LED, un titre initial élevé d’Ac anti-ADN natif traduit l’évolutivité du lupus (et
non sa gravité). Au cours du traitement, la chute puis la négativité des Ac anti-ADN
natif traduisent l’efficacité du traitement et la rémission de la maladie. Au contraire,
une réascension des Ac incitera à une surveillance clinique rapprochée car elle peut
précéder une rechute.
Le classement d'un état pathologique
La présence des AAN et leur type figurent parmi les critères utilisés pour classer
lupus et syndrome de Gougerot-Sjögren. A l'inverse, leur absence constitue l'un des
critères exigés pour poser le diagnostic de la maladie de Still de l'adulte. Aussi, la
recherche d'AAN est-elle indispensable à qui veut s'assurer que son patient répond
bien aux critères de classification de la maladie qu'il se propose d'étudier, par
exemple dans le cadre d'un protocole de recherche clinique.
Les indications de l'examen
Sur le plan pratique, ce sont la recherche de la cause d'un symptôme isolé et l'étude
étiologique d'un syndrome constitué qui justifient les demandes de dépistage d'AAN.
L'extrême variété des situations auxquelles le clinicien est confronté nous amène à
passer en revue différents organes. Chacun d'entre eux peut présenter des
manifestations particulières. Toute situation orientant vers une maladie auto-immune
invite de ce fait à vérifier s'il existe des AAN.
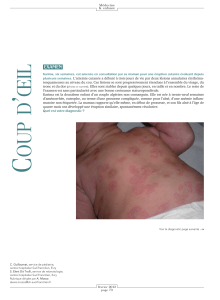
-La peau : Les manifestations dermatologiques font partie des signaux principaux de
nombreuses maladies auto-immunes : l’éruption malaire en aile de papillon du lupus,
les lésions cutanées de lupus discoïde et la photosensibilité sont des signes
classiques, au point qu'ils constituent 3 des 11 critères de classification du lupus. Une
alopécie peut aussi apparaître sur ce terrain. Une sclérodactylie, des télangiectasies,
et une sclérodermie proximale peuvent inaugurer l'évolution d'une sclérodermie
systémique. Les doigts boudinés évoquent une connectivite mixte.

-Les muqueuses : Des ulcérations buccales sont possibles au cours du lupus.
Une hypertrophie des parotides et un syndrome sec subjectif ou objectif peuvent
dénoncer un syndrome de Gougerot-Sjögren, qu'il soit primitif ou secondaire.
-Les articulations : Polyarthralgies ou arthrites alertent le patient dans la
grande majorité des maladies systémiques et plus particulièrement le lupus, le
syndrome de Gougerot-Sjögren et la polyarthrite rhumatoïde.
-Les reins : Protéinurie et présence de cylindres urinaires peuvent également
permettre la découverte d'un lupus.
-Le système cardio-vasculaire : La péricardite est classique au cours du
lupus. Le syndrome de Raynaud fait partie des manifestations habituelles du
lupus, du SGS
,
de la dermato-polymyosite, de la PR et de la sclérodermie.
Phlébites et thromboses font partie du tableau du syndrome des
antiphospholipides. La présence d’Ac anti-phospholipides impose la recherche
d'un lupus auquel ils peuvent être associés.
-Le système respiratoire : Pleurésie ou fibrose pulmonaire peuvent être
observées dans de nombreuses maladies systémiques et tout particulièrement
dans le lupus et la sclérodermie systémique.
-Les nerfs et les muscles : Des convulsions, voire une psychose, peuvent
traduire l'existence d'un lupus. Une faiblesse ou des douleurs musculaires font
partie du tableau caricatural de la dermato-polymyosite.
-Le système digestif : Une hépatopathie ou une splénomégalie peuvent
augurer d'une maladie auto-immune, quelle qu'elle soit.
-Les signes obstétricaux : La présence d’Ac antiphospholipides, associée ou
non à un lupus, peut induire des fausses couches à répétition.
-Le sang: De nombreuses manifestations hématologiques (leucopénie,
lymphopénie, thrombopénie, anémie inflammatoire ou hémolytique,
augmentation du temps de céphaline activée (TCA), cryoglobulinémie) doivent
faire évoquer le diagnostic de lupus et faire rechercher la présence d'AAN.
II - COMMENT METTRE EN EVIDENCE LES ANTICORPS ANTI-
NUCLEAIRES ?
Le plus fréquemment, les AAN se recherchent par technique
d’immunofluorescence indirecte sur cellules diploïdes humaines (Hep-2). Cet
examen de « screening » permet de connaître le titre et le type de fluorescence
observés. L’interprétation du titre doit tenir compte de l’âge et du sexe du
patient (valeurs de référence du laboratoire pour l’adulte < 1/20). La présence
d’AAN à taux faibles est physiologique et ce taux physiologique s’accroît avec
l’âge. Si le titre est nettement supérieur à la normale de l’âge, un terrain auto-
immun est probable.
L’analyse de l’image de fluorescence nucléaire oriente la démarche
diagnostique et permet de poursuivre de façon ciblée les examens
immunologiques afin d’identifier la spécificité de l’anticorps.
Plusieurs aspects de fluorescence nucléaire peuvent être observés : global
(homogène, périphérique ou translucide), moucheté, nucléolaire... Certains
aspects peuvent orienter d’emblée vers une sous-population particulière d’AAN
(anticorps anti-centromères…) mais, le plus souvent, d’autres techniques
devront être mises en œuvre selon une démarche schématisée dans le tableau
ci-dessous.
Remarque : la Nomenclature des Actes de Biologie Médicale prévoit dans le cas
d’une recherche d’AAN positive, la possibilité de rechercher des anticorps anti-
ADN natif à l’initiative du biologiste.
III - DEMARCHE DIAGNOSTIQUE DEVANT LE PRESENCE D'AC ANTI-
NUCLEAIRES
Voit tableau
CONCLUSION
La détection et la caractérisation des Ac anti-nucléaires constituent donc une étape
déterminante devant toute manifestation évoquant une maladie systémique. Les tests
disponibles pour la recherche des auto-Ac sont aujourd’hui assez standardisés ; mais
le nombre d’Ac anti-nucléaires et la diversité de leur mise en évidence font qu’il n’est
pas techniquement et économiquement envisageable de les dépister et de les
identifier systématiquement en routine. Il faut donc concevoir une stratégie et une
hiérarchie des examens à pratiquer.
Jean-Pierre BOUILLOUX et Sylvie HAMON
Prochain sujet : PSA et pathologies prostatiques
Remarque : ce « QDND ? », c’est inspiré en partie de l’article de P. YOUINOU, A.
SARRAUX et P. LEGOFF, « Les anticorps anti-nucléaires » , paru dans « LE
CAHIER DE FORMATION DE BIOLOGIE MEDICALE » N°13, février 1999.
Pas de parution du « QDND ? » en Juillet et en Août
1
/
2
100%