Le diagnostic de la rage

LES MALADIES TROPICALES (1)
REVUE FRANCOPHONE DES LABORATOIRES - MARS 2011 - N°430 // 33
SUMMARY
Rabies laboratory diagnosis
Rabies is an encephalitis due to a lyssavirus, a zoono-
tic agent. It is not yet controled and is even re-emer-
ging in many African and Asian countries. In France,
most of the animal and human cases are imported.
The clinical diagnosis of rabies is often difcult and
therefore the laboratory diagnosis remains the only
diagnosis of certainty. In post-mortem diagnosis in
animals or humans, brain biopsy or brain specimens
will be analysed by direct immunouorescence, cell
culture isolation and rabies antigen capture by ELISA.
In intra-vitam diagnosis in humans, nested RT-PCR
will be performed on 3 saliva specimens collected
at intervals and/or on a skin biospsy collected at
the tap of the neck. The contribution of laboratory
diagnosis methods is major for the control of rabies,
its prevention and for the optimal delivery of the post-
exposition prophylaxis in rabies-exposed patients.
Encephalitis – zoonosis – rabies – lyssavirus –
immunofluorescence – isolation – RT-PCR.
1. Introduction
La rage est une zoonose virale due à un lyssavirus auquel
sont sensibles tous les mammifères. Elle est transmissible
accidentellement à l’homme, généralement à la suite d’une
morsure, d’une griffure ou d’un léchage sur plaie par un
animal enragé. La contamination des muqueuses (par
exemple oculaire) est aussi une voie efcace d’infection.
Enn quelques rares cas de transmission par allogreffe sont
notés. La rage est caractérisée cliniquement par l’apparition
d’un tableau d’encéphalite dont les symptômes sont très
variables selon les individus et les espèces considérés.
Elle est toujours fatale dans un délai bref. Le diagnostic
différentiel avec d’autres encéphalites virales d’étiologie
différente est souvent difcile voire impossible. Dans ces
conditions, seul l’examen de laboratoire permet de porter
un diagnostic de certitude. Au début des années 1980,
un diagnostic demandait entre 15 jours et 3 semaines.
Ilétait effectué par immunouorescence et par l’inoculation
de souris avant de pouvoir mettre en évidence le virus.
Aujourd’hui le diagnostic de la rage peut s’effectuer en
24 heures. Les gains de temps et de sensibilité obtenus
permettent aujourd’hui de mieux répondre aux impératifs
de la prophylaxie de la rage chez l’homme. Nous pro-
posons ici de rappeler succinctement les principes, les
propriétés et les indications de ces techniques de labo-
ratoire. Elles sont maintenant utilisées par de nombreux
centres de diagnostic de la rage dans le monde entier et
en particulier en France. Elles ont aussi été adaptées aux
conditions des pays tropicaux où l’incidence de la rage
est la plus importante.
2. Les lyssavirus
2.1. Taxinomie
Les lyssavirus appartiennent à la famille des Rhabdoviri-
dae et à l’ordre des Mononegavirales. Sur la base de la
comparaison des séquences des nucléoprotéines et des
génomes complets, onze espèces (anciennement dénom-
mées génotypes) ont pu être dénies (tableau I) [1]. On
distingue pour chaque espèce un virus prototype : le virus
de la rage (espèce RABV), le virus Lagos bat (espèce LBV),
RÉSUMÉ
La rage est une zoonose virale due à un lyssavirus et caractérisée par un
tableau d’encéphalite. Elle est mal contrôlée voire en recrudescence dans
de nombreuses régions d’Afrique et d’Asie. En France, c’est aujourd’hui
essentiellement une maladie d’importation. Le diagnostic clinique étant
souvent difcile, le diagnostic de laboratoire est le seul diagnostic de cer-
titude. En post-mortem chez l’homme et l’animal, le diagnostic s’effectue
à partir d’une biopsie ou d’un prélèvement cérébral analysés par immuno-
uorescence directe, par isolement en culture cellulaire ou par immuno-
capture d’antigène par ELISA. En intra-vitam chez l’homme, le diagnostic
se pratique principalement par RT-PCR nichée sur 3 prélèvements sériés
de salive et/ou sur une biopsie de peau prélevée au niveau de la nuque.
La contribution des techniques de diagnostic au contrôle de la rage, à
sa prévention et à la prise en charge des patients exposés par la mise
en œuvre à bon escient de la prophylaxie post-exposition, est majeure.
Encéphalite – zoonose – rage – lyssavirus
immunofluorescence – isolement – RT-PCR.
article reçu le 20 février, accepté le 30 juin 2010
© 2010 – Elsevier Masson SAS – Tous droits réservés.
art
t
il
icl
e reçu
l
le
20
20
fé
fé
i
vri
er accep
té
té
l
le
30
30
ji
jui
2
n2
010
010
a
Centre national de référence pour la rage
Centre collaborateur de l’OMS de référence et de recherche pour la rage
Unité dynamique des lyssavirus et adaptation à l’hôte
Institut Pasteur
25, rue du Docteur-Roux
75724 Paris cedex 15
* Correspondance
laurent.dacheux@pasteur.fr
herve.bourhy@pasteur.fr
Laurent Dacheuxa, Hervé Bourhya,*
Le diagnostic de la rage

34 // REVUE FRANCOPHONE DES LABORATOIRES - MARS 2011 - N°430
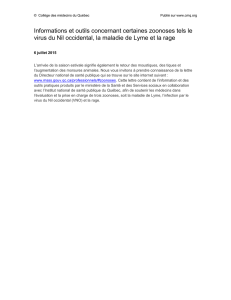
Figure 1 – Représentation schématique
de la structure du virion.
Tableau I – Classification des lyssavirus et caractéristiques épidémiologiques.
Dénomination Espèce Distribution géographique
Espèces réservoirs
et/ou
vectrices
Autres espèces
concernées (cul-de-sac
épidémiologique)
Cas humains identifiés
Virus de la rage RABV
Monde entier, à l’exception
de l’Antarctique, l’Australie,
certains pays d’Europe de
l’Ouest, une partie de la
Scandinavie et certaines îles
Chien, carnivores sauvages,
chauves-souris (uniquement
pour le continent américain)
Homme, carnivores
domestiques et
sauvages, herbivores,
autres chauves-souris (?)
55 000/an (99 % liés au
chien, et quelques dizaines
de cas liés aux chauves-
souris)
Lagos bat virus LBV
Afrique : Nigéria, République
centrafricaine, Afrique du
Sud, Sénégal, Ethiopie,
Guinée, Zimbabwe
Chauves-souris frugivores
(genres Eidolon,
Epomophorus, Rousettus,
Micropteropus)
Chauves-souris
insectivores (genre
Nycteris), chats, chiens,
mangouste aquatique
Aucun à ce jour
Mokola virus MOKV
Afrique : Nigéria, République
centrafricaine, Zimbabwe,
Cameroun, Ethiopie, Afrique
du Sud
Non identiées Homme, musaraignes,
chats, chiens, rongeur
1 conrmé (Nigéria, 1971),
1 suspecté (Nigéria, 1969)
Duvenhage virus DUVV Afrique : Afrique du Sud,
Zimbabwe
Chauves-souris insectivores
(genre Miniopterus,
Nycteris)
Homme
3 (Afrique du Sud, 1971,
2006, Pays-Bas via Kenya,
2007)
European bat lyssavirus type1
(sous-type a ou b) EBLV-1 Europe
Chauves-souris insectivores
(principalement genre
Eptesicus)
Homme, autres chauves-
souris insectivores (?),
chats, moutons, fouine
1 conrmé et 2 suspectés
(Russie, 1985)
European bat lyssavirus type 2 EBLV-2 Europe
Chauves-souris insectivores
(principalement genre
Myotis)
Homme 2 (Finlande, 1985, Ecosse,
2002)
Australian bat lyssavirus ABLV Australie
Chauves-souris frugivores
(genre Pteropus) et
insectivores (principalement
genre Saccolaimus)
Homme 2 (Australie, 1996, 1998)
Aravan virus ARAV Asie centrale (Kirghizistan)
Chauve-souris insectivore
(genre Myotis) (isolée une
seule fois en 1991)
? Non rapporté
Khujand virus KHUV Asie centrale (Tadjikistan)
Chauve-souris insectivoire
(genre Myotis) (isolée une
seule fois en 2001)
? Non rapporté
Irkut virus IRKV Sibérie orientale
Chauve-souris insectivore
(genre Murina) (isolée une
seule fois en 2002)
? Non rapporté
West caucasian bat virus WCBV Région du Caucase
Chauve-souris insectivore
(genre Miniopterus) (isolée
une seule fois en 2003)
? Non rapporté
M. La G, en position transmembranaire, s’associe sous
forme de trimères pour constituer des spicules. En micros-
copie électronique, les spicules distants d’environ 5nm
apparaissent disposés régulièrement autour du virion et
le virus Mokola (espèce MOKV) et le virus Duvenhage
(espèce DUVV), le virus European bat lyssavirus type1
(espèce EBLV-1), le virus European bat lyssavirus type2
(espèce EBVL-2) et le virus Australian bat lyssavirus (espèce
ABLV). De nouveaux isolats ont été obtenus chez des
chauves-souris et constituent les prototypes de nouvelles
espèces.
2.2. Morphologie - structure
Le virus rabique est un virus enveloppé présentant en
microscopie électronique une forme d’obus. La taille des
virions est d’environ 100-300 nm de long sur 75 nm de
diamètre. Ces virions sont constitués d’une nucléocapside
centrale de symétrie hélicoïdale entourée d’une enveloppe
lipidique empruntée à la cellule lors du bourgeonnement
(figure 1).
L’enveloppe composée d’un double feuillet phospholipi-
dique entoure tout le virion. Elle comporte deux protéines
d’origine virale, la glycoprotéine G et la protéine de matrice

LES MALADIES TROPICALES (1)
REVUE FRANCOPHONE DES LABORATOIRES - MARS 2011 - N°430 // 35
Figure 2 – Cycle épidémiologique de la rage.
donnent au virus son aspect hérissé. La M forme un man-
chon entre l’enveloppe et la nucléocapside virale.
La nucléocapside est constituée de l’ARN génomique (envi-
ron 12 000 nucléotides) associé à trois protéines virales :
la nucléoprotéine N, l’ARN polymérase ARN dépendante
L et la phosphoprotéine P. L’ARN génomique est linéaire,
monocaténaire, non segmenté, non polyadénylé et de
polarité négative. La transcription de 3’en 5’aboutit à la
production séquentielle de 5 ARN messagers (ARNm) en
quantité décroissante, monocistroniques coiffés et poly-
adénylés, codant pour les protéines N, M, P, G et L [1]. La
protéine N est étroitement liée à l’ARN sur la totalité de
sa longueur. Les protéines P et L ont un rôle fonctionnel
important dans les phénomènes de transcription et de
réplication du génome viral.
3. Epidémiologie
3.1. Dans le monde
Le contrôle de la rage reste encore une des priorités de
l’Organisation mondiale de la Santé (OMS). En effet, il ne faut
pas sous-estimer la gravité de cette infection dans certaines
parties du monde. Plus d’un siècle après la découverte de
la vaccination antirabique, on estime que la rage dans le
monde est encore à l’origine d’environ 55 000 décès par
an [2]. Ce chiffre ne semble pas évoluer favorablement. Au
contraire, la rage semble même ré-émerger dans certaines
parties du monde (c’est le cas en Chine, au Vietnam et
dans certaines parties d’Afrique). La raison est due à une
absence de prise en charge efcace par les autorités de
santé publique humaine et vétérinaire [3, 4]. Selon l’OMS, ce
chiffre place la rage au 10e rang des maladies infectieuses
mortelles. Deux continents sont particulièrement touchés :
l’Afrique et l’Asie. Le chien représente la principale espèce
animale réservoir dans le monde (il est à l’origine d’environ
99 % des décès humains) (figure 2). Cependant de très
nombreuses autres espèces de mammifères jouent le rôle
de réservoirs. Elles appartiennent à 2 ordres: celui des
chiroptères (chauves-souris hématophages, insectivores
et frugivores) et celui des carnivores (renard, mouffette,
mangouste par exemple). A chacun de ces réservoirs
correspond un variant particulier de lyssavirus. En dehors
de ces réservoirs, la plupart des espèces de mammifères
sont sensibles aux lyssavirus et peuvent donc constituer
des vecteurs de l’infection chez l’homme.
3.2. En Europe et en France
Durant ce dernier siècle, des modications importantes
des cycles épidémiologiques de la rage en Europe ont été
observées. De plus, la mise en place de nouvelles investi-
gations épidémiologiques et biologiques a permis la mise
en évidence de nouveaux cycles épidémiologiques. La
rage est aujourd’hui toujours présente. Son incidence chez
l’homme reste limitée (moins de 5 cas par an en Europe)
par l’application stricte de mesures de prophylaxie post
exposition (PPE) et par des mesures de contrôle vétéri-
naire de la rage dans les populations animales sauvages
et domestiques [5]. Les principaux réservoirs animaux
autochtones sont : le chien dans les pays d’Europe de
l’Est et aux frontières avec le Moyen-Orient ; le renard en
Europe centrale et de l’Est ; le chien viverrin dans le nord-
est de l’Europe et les chauves-souris insectivores sur
l’ensemble du continent [6, 7]. Enn, tous les ans des cas
d’importation d’animaux enragés en provenance de zones
d’enzootie sont recensés, montrant la perméabilité de nos
frontières et l’absence de prise de conscience du risque
rabique par les voyageurs. Ces importations menacent en
permanence le statut indemne de rage des animaux non
volants des pays de l’ouest européen et compliquent la
décision thérapeutique des médecins en l’absence d’in-
formation sur l’animal mordeur.
La rage des chauves-souris est de caractérisation ancienne
en Europe. Les premiers isolats datent de 1954. A par-
tir de 1985, des campagnes importantes de capture de
chiroptères sont réalisées au Danemark et dans les Pays-
Bas et révèlent l’importance de l’enzootie [8]. Depuis la n
de ces campagnes exploratoires, environ 50 cas par an
sont diagnostiqués dans de nombreux pays européens.
Trois cas humains dus à des lyssavirus de chauves-souris
européennes ont été conrmés en Europe de 1977 à 2010.
Les lyssavirus sont aussi présents dans les populations
françaises de chiroptères. Les conséquences en santé
publique restent réduites. Aucun cas humain n’a été rap-
porté. Cependant 50 à 100 patients par an reçoivent une
PPE suite à un contact avec une chauve-souris. Enn, un
cas d’infection par ces virus a été rapporté chez un chat
en Vendée en 2007 [9]. Ceci montre que le passage de
l’infection des chauves-souris aux animaux domestiques
est réduit mais possible.
Les lyssavirus du chien et du renard ont été éliminés du
territoire français depuis respectivement 1924 et 1998
[10]. Cependant l’importation d’animaux au statut sanitaire
incertain en provenance de zones d’enzootie met réguliè-
rement en péril la situation de la France. A la suite d’une de
ces importations passée malheureusement inaperçue, une
chaîne de transmission s’est temporairement développée
en France n 2007-début 2008. Cet épisode aujourd’hui
contrôlé a fait perdre temporairement à la France son sta-
tut de pays indemne de rage des carnivores non-volants.
La rage humaine en France métropolitaine est de nos
jours une maladie d’importation. Sur les 21 cas humains
recensés en France de 1970 à 2008, 20 ont été acquis
chez des voyageurs (18 en provenance d’Afrique dont 10
en provenance du Maghreb). Un cas humain rapporté à la
Réunion en 1996 est un cas importé de Madagascar. Un
autre cas rapporté en Guyane en 2008 est dû à un virus
de rage des chauves-souris hématophages.

36 // REVUE FRANCOPHONE DES LABORATOIRES - MARS 2011 - N°430
nerveux autonome (hypersalivation, énurésie, priapisme,
hypersudation). L’hydrophobie est un signe spécique de la
rage mais inconstamment retrouvé. Elle peut s’accompa-
gner d’aérophobie : le soufe d’air sur la peau ou le visage
du patient déclenche également ces spasmes phobiques.
Les signes de dysphagie sont plus fréquents. Les périodes
d’agitation ou d’obnubilation alternent avec des périodes
de normalité. Ces signes durent classiquement entre 1 à
4 jours puis le coma survient. Le patient décède ensuite
par paralysie du système cardiorespiratoire, en moyenne
dans les 5 jours après le début des signes cliniques en
l’absence de prise en charge médicale.
La forme paralytique ou « rage muette » (30 % des cas)
se manifeste par des paresthésies au niveau du point
d’entrée puis par une paralysie asque avec aréexie.
L’hydrophobie/aérophobie est peu présente. La maladie
évolue vers une para/quadriplégie qui peut faire évoquer
une myélite transverse ou un syndrome de Guillain Barré
et le décès survient par paralysie respiratoire, en moyenne
2 semaines après le début des symptômes (en l’absence
de prise en charge médicale).
6. Le diagnostic de laboratoire
6.1. Introduction
L’établissement d’un diagnostic clinique de la rage est
délicat et d’une abilité limitée. En effet, les signes cli-
niques de la maladie, bien que dominés par des symp-
tômes nerveux, restent pléiomorphes et non spéciques
chez l’animal et l’homme. Seule l’hydrophobie (associée
ou non à de l’aérophobie) peut être considérée comme
pathognomonique de la rage humaine, mais elle n’est pas
toujours retrouvée [14]. Ainsi, la conrmation du statut
enragé d’un animal ou d’un individu repose uniquement
sur la réalisation du diagnostic biologique, qui doit donc
être le plus able possible en termes de sensibilité et de
spécicité [15]. En effet, le résultat de ce diagnostic est
lourd de conséquence puisqu’il a un impact direct sur
la prévention de la mortalité humaine liée à la rage. La
conrmation d’un cas de rage animale conduit ainsi à la
mise en place le plus rapidement possible de la PPE chez
les personnes en contact. De même, l’établissement d’un
diagnostic de rage chez un patient conduit à des mesures
préventives chez les personnes de son environnement, et
à la mise en place d’un traitement palliatif pour ce patient
amené inéluctablement à décéder. Egalement, la sur-
venue de cas de rage chez des patients transplantés à
partir d’organes prélevés sur un donneur enragé souligne
l’intérêt de la mise en place d’un diagnostic intra-vitam
réalisé précocement [16]. A l’inverse, l’établissement d’un
diagnostic négatif chez l’animal aboutit à l’arrêt de la PPE.
Enn, le diagnostic biologique est l’outil indispensable de
tout programme de surveillance et de contrôle de la rage
humaine et animale, car il permet l’obtention de données
épidémiologiques ables [4].
Ce diagnostic biologique de la rage animale ou humaine
est réalisé exclusivement dans des centres de référence
habilités, en laboratoire de connement L2, voire L3. En
France, cette activité est répartie entre le Centre national
de référence pour la rage (CNRR) de l’Institut Pasteur à
4. Rappels sur la prise en charge
des patients exposés
A long terme, la prophylaxie de la rage repose sur le contrôle
et la disparition de la rage animale. La protection immé-
diate des populations repose sur la prévention au travers
de la vaccination antirabique des professions exposées et
sur la PPE des individus éventuellement contaminés. Le
nombre de PPE dans le monde est de l’ordre de 15 mil-
lions par an. En France, la PPE est administrée au travers
de consultations spécialisées effectuées par les centres
antirabiques répartis sur tout le territoire français [11]. Deux
protocoles recommandés par l’OMS sont utilisés [12]. Il
s’agit de protocoles associant 4 ou 5 injections de vaccins
par voie intramusculaire à une sérothérapie antirabique
effectuée si possible par instillation locale au niveau des
zones de morsure, dans les cas les plus graves.
5. Rappels cliniques
5.1. La rage chez l’animal
Le signe clinique le plus marquant reste la modication
du comportement habituel (ex : perte de méance pour
l’homme). Un comportement agressif et une hyperactivité
sont fréquemment retrouvés chez les carnivores infectés
(domestiques ou sauvages), mais des formes paralytiques
sont également observées, sans signe d’agressivité asso-
cié. Au cours de la maladie, un animal infecté peut aussi
présenter alternativement ces deux formes cliniques. La
mort survient en général en moins de deux semaines.
5.2. La rage chez l’homme
Le virus chemine de la zone de contamination vers le sys-
tème nerveux central par voie nerveuse. L’incubation a une
durée médiane de l’ordre de 30 jours avec des extrêmes
de 7 jours à plus de 1 an voire 6 ans. C’est pendant cette
période que les mesures prophylactiques doivent être
entreprises.
La période prodromique dure entre 2 et 10 jours. Le début
est brutal avec des douleurs et des paresthésies (sensation
de brûlure, froid, fourmillement) au niveau du point d’en-
trée. La èvre est inconstante. Le malade peut présenter
des signes digestifs (anorexie, nausées, vomissements,
diarrhée), des signes neurologiques (céphalées, vertiges)
ainsi que des signes divers (anxiété, tristesse, irritabilité,
insomnie, cauchemars).
La période d’état est ensuite très courte. Elle est carac-
térisée par une encéphalomyélite présentant principale-
ment deux types distincts de forme clinique : une forme
spastique et une forme paralytique [13]. Rapidement, cette
période d’état est suivie d’une phase de coma qui peut
être articiellement prolongée par l’administration de soins
intensifs. Toute rage déclarée est mortelle. Les évolutions
favorables sont exceptionnelles.
La forme spastique ou « rage furieuse » (70 % des cas) se
manifeste par des troubles du comportement, une hyperac-
tivité, des spasmes phobiques (hydrophobie, aérophobie)
ou inspiratoires et des dysfonctionnements du système

LES MALADIES TROPICALES (1)
REVUE FRANCOPHONE DES LABORATOIRES - MARS 2011 - N°430 // 37
Paris et le Laboratoire d’études sur la rage et la pathologie
des animaux sauvages de l’ANSES à Malzéville (ANSES
Nancy). Le CNRR est en charge de l’analyse de toutes les
suspicions de rage humaine (www.pasteur.fr/recherche/
unites/Dylah/fr-diagno.html) (figure 3) ainsi que de tous
les animaux domestiques ou sauvages suspects d’avoir
transmis la rage à l’homme (au travers de morsure, grif-
fure, léchage voire simple manipulation), l’ANSES Nancy
réalisant le diagnostic de la rage sur les autres animaux
pour lesquels le risque de contamination à l’homme a été
écarté. En France, la rage humaine et animale fait partie
des maladies à déclaration obligatoire.
Le diagnostic biologique de la rage est réalisé par la mise en
évidence directe du virus dans les prélèvements analysés,
que ce soit au travers de la détection des antigènes viraux,
de l’isolement viral ou de la détection des ARN viraux. Des
techniques de dosage des anticorps antirabiques peuvent
également être utilisées dans le cadre d’un diagnostic de
rage humaine, mais elles sont généralement utilisées pour
le suivi et le contrôle vaccinal chez l’homme et l’animal.
6.2. Prélèvements
Les prélèvements potentiellement infectieux doivent être
expédiés selon la réglementation en vigueur en matière
de risque infectieux, en l’occurrence dans la classe 6.2
et affectés au N° ONU 3373 en tant que « Matière biolo-
gique de catégorie B » (dans un triple emballage et par
un transporteur habilité). Ils doivent être accompagnés de
renseignements cliniques et biologiques (www.pasteur.
fr/recherche/unites/Dylah/fr-diagno.html) (figure 3).
r Chez l’homme
Le prélèvement de choix pour le diagnostic intra-vitam de
la rage humaine est la biopsie cutanée obtenue au niveau
d’une zone richement innervée (préférentiellement à la
base de la nuque dans une zone riche en follicules pileux)
[14]. En effet, le virus est régulièrement retrouvé dans les
cellules nerveuses entourant la base des follicules. Cette
biopsie peut être réalisée par un dermatologue à l’aide
d’un instrument de type Biopsy Punch (diamètre de 4 mm).
La salive est le second prélèvement à analyser. Elle doit
être collectée par écouvillonnage ou par recueil direct et
de façon séquentielle (au minimum 3 heures d’intervalle
entre deux prélèvements). L’excrétion intermittente du virus
dans la salive nécessite en effet de multiplier le nombre
d’échantillons. Les prélèvements d’urine, de LCR et de
sérum peuvent être également réalisés, bien que la sen-
sibilité diagnostique soit plus faible. Les empreintes de
cornées réalisées du vivant du patient sont à proscrire,
de par leur faible sensibilité diagnostique mais surtout
par le risque d’atteinte oculaire qu’elles induisent chez
les patients, surtout si la suspicion de rage est écartée.
En cas de décès du patient, des prélèvements cérébraux
(biopsies de cortex cérébral, d’hippocampe ou de cervelet)
peuvent être réalisés [17, 18]. L’ensemble de ces différents
prélèvements doit être conservé et expédié congelé, ceci
an de garantir au maximum l’intégrité de ces échantillons
biologiques, et donc du virus potentiellement présent.
r Chez l’animal
Le diagnostic est exclusivement réalisé sur l’animal mort
à partir de prélèvements cérébraux au niveau du bulbe
rachidien et de l’hippocampe, voire du cortex cérébral
Figure 3 – Prélèvements et conditions d’expédition
au CNR de la rage.
Figure 4 – Méthodes de diagnostic de laboratoire de la rage.
 6
6
 7
7
 8
8
1
/
8
100%