Quatrième Résumé de cours de chimie

Quatrième
Résumé de cours de chimie
1 Les molécules
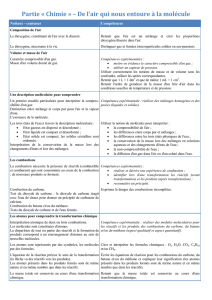
1.1 L’air qui nous entoure
L’atmosphère terrestre
L’air est un mélange de plusieurs gaz. Les deux principaux gaz qui composent l’air sont le
dioxygène (environ 20 %) et le diazote (environ 80 %).
Le dioxygène est nécessaire à la vie de nombreux organismes, et de l’être humain en
particulier.
L’air est constitué de molécules.
En chimie, on appelle « corps pur » une substance qui n’est constituée que d’une seule
sorte de molécules.
Il y a plusieurs sortes de molécules dans l’air : l’air n’est donc pas un corps pur, c’est un
mélange.
La molécule de dioxygène est faite de deux atomes d’oxygène.
Le symbole d’un atome d’oxygène est O et la formule d’une molécule de dioxygène est .
L’air est pesant
1 litre d’air pèse un peu plus de 1 gramme.
Cette valeur est à comparer à celle de 1 litre d’eau liquide, qui vaut environ 1 000
grammes (tu l’as appris en classe de 5e).
1.2 La pression des gaz
Comprimer de l’air
Il est possible de comprimer un gaz, c’est-à-dire de réduire son volume en appuyant
dessus. On dit qu’un gaz est compressible.
Lors de la compression d’un gaz, les molécules se rapprochent les unes des autres.
Mesurer la pression d’un gaz
La pression d’un gaz se mesure avec un manomètre. On trouve des manomètres, par
exemple sur les pompes destinées à gonfler les ballons, les pneus de voiture et de
Résumé de cours de chimie 1/4

bicyclette, etc.
L’unité légale de pression est le pascal (en abrégé Pa).
Dans la vie quotidienne, les manomètres sont souvent gradués en bars : .
Peut-on comprimer de l’eau ?
L’état solide de l’eau est un état compact, ce qui signifie que les molécules sont au contact
les unes des autres. C’est aussi un état ordonné, ce qui veut dire que les molécules sont
disposées selon un motif géométrique régulier.
L’état liquide de l’eau est un état compact, mais désordonné (les molécules n’ont aucune
disposition régulière).
L’état gazeux de l’eau est un état dispersé, ce qui signifie que les molécules ne sont pas
en contact les unes avec les autres. C’est aussi un état désordonné.
L’eau liquide est incompressible car c’est un état compact : on ne peut pas rapprocher
davantage les molécules.
La vapeur d’eau est compressible car c’est un état dispersé : on peut rapprocher les
molécules.
Lors d’un changement d’état, la masse se conserve car ce sont les mêmes molécules ;
c’est seulement leur disposition qui change.
2 Transformations chimiques
2.1 La combustion du carbone
La combustion du charbon de bois
Comme toutes les combustions, la combustion du charbon de bois :
nécessite du dioxygène en quantité suffisante :
libère de l’énergie sous forme de chaleur.
Lors d’une combustion, des matières disparaissent et d’autres, nouvelles, se forment : une
combustion est donc une réaction chimique.
Dans la combustion du charbon de bois, les deux réactifs sont le charbon de bois et le
dioxygène. Les produits de la combustion sont les cendres et le dioxyde de carbone.
Le dioxyde de carbone est identifié par le test à l’eau de chaux.
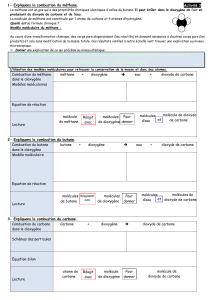
L’équation de la combustion du charbon de bois est :
dioxygène + charbon de bois → cendres + dioxyde de carbone
La combustion du carbone pur
L’équation de la combustion du carbone pur est :
dioxygène + carbone → dioxyde de carbone
Les atomes et les molécules pour interpréter la combustion du carbone pur
L’équation de la combustion du carbone se représente, avec les schémas d’atomes et de
molécules :
Résumé de cours de chimie 2/4

L’équation de la combustion du carbone s’écrit, avec les formules moléculaires :
On peut l’écrire tout aussi bien :
Lors d’une réaction chimique, il y a « conservation des atomes ». Cela veut dire que l’on
retrouve exactement les mêmes atomes à la fin d’une réaction chimique (dans les produits
de la réaction) qu’au début (dans les réactifs).
2.2 La combustion du méthane
La combustion du méthane
Le méthane est le principal constituant du gaz naturel. Ce dernier est extrait de gisements
souterrains (la Russie et le Moyen-Orient, notamment, sont de grands producteurs de gaz
naturel).
Quand la combustion du méthane donne une flamme bleue, on dit que cette combustion
est « complète ». Pour que la combustion soit complète, il faut que le dioxygène soit en
quantité abondante.
Si le dioxygène est en quantité insuffisante, la flamme est jaune : la combustion est
« incomplète ».
L’équation chimique de la combustion complète du méthane est :
méthane + dioxygène → dioxyde de carbone + eau
Les atomes pour comprendre la combustion du méthane
La formule chimique du méthane est
Pour qu’une équation chimique soit ajustée, il faut que les atomes présents dans les
réactifs se retrouvent intégralement dans les produits de réaction. On dit qu’il y a
« conservation des atomes » lors d’une réaction chimique.
C’est parce qu’il y a conservation des atomes lors d’une transformation chimique qu’il y a
conservation de la masse.
L’équation chimique ajustée de la combustion complète du méthane est :
Dans une équation chimique, les chiffres écrits en grand désignent des nombres de
molécules. Ceux écrits en petit et en bas désignent les nombres d’atomes dans les
molécules.
Résumé de cours de chimie 3/4

La combustion du butane
Le butane a pour formule chimique
Lors de la combustion complète du butane, les produits de réaction sont les mêmes que
lors de la combustion complète du méthane : de l’eau et du dioxyde de carbone.
Il faut être capable d’ajuster une équation chimique, telle que celle de la combustion
complète du butane :
équation non ajustée :
équation ajustée :
2.3 Les dangers des combustions
Les combustions incomplètes
Une combustion incomplète se produit quand l’apport de dioxygène à la flamme est
insuffisant. La flamme est jaune.
Une combustion incomplète produit notamment du monoxyde de carbone, gaz toxique.
Tout appareil destiné à réaliser des combustions doit être utilisé selon des règles de
sécurité, qu’il faut connaître et respecter.
Les risques d’explosion
Le méthane, le butane et le propane présentent un risque d’explosion.
Une explosion de gaz est une combustion quasi-instantanée, brutale, d’une grande
quantité de réactifs.
Les explosions de gaz sont le plus souvent causées par des fuites. Il faut vérifier que les
robinets de gaz sont bien refermés après usage, et que les tuyaux et canalisations sont en
bon état.
Les risques du tabac
Le tabac contient une substance, la nicotine, qui provoque une dépendance.
La combustion du tabac produit de très nombreuses substances toxiques, parmi
lesquelles les goudrons.
Résumé de cours de chimie 4/4
1
/
4
100%