Diapositive 1


La cellule
•Taille : de l’ordre du micromètre (10-6m)
•2 types de cellules
–Cellule procaryote (bactéries)
–Cellule eucaryote : animale, végétale
Cellule procaryote
•Vie unicellulaire
•Noyau non délimité par une membrane
•Présence possible de pili, flagelle, capsule
Cellule Eucaryote
•Végétale ou Animale
•Vrai noyau délimité par une membrane

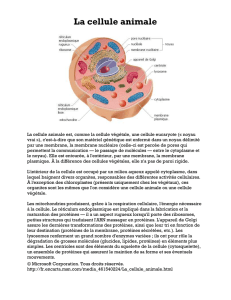
Composition
•Membrane plasmique
•Cytosol
•Noyau + enveloppe nucléaire
•Organites :
–Mitochondries
–Réticulum endoplasmique (lisse et rugueux)
–Appareil de Golgi
–Ribosomes
–Endosomes, lysosomes

Organites
Fonction principale
Mitochondrie
Apporte l’énergie à la cellule
Ribosomes
Permettent l’allongement des peptides
RE
Synthèse, translocation et adressage de protéines
Glycosylation (ajout de molécules de sucres sur les
protéines)
Synthèse des lipides
Stockage du calcium et autres substances
Appareil de Golgi
Transport des protéines
Glycosylation des protéines
Tri et adressage des protéines
Stockage du calcium
Endosome et lysosome
Dégradation de protéines, lipides, sucres, acides
nucléiques…
Noyau
Contient l’information génétique

 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
1
/
26
100%