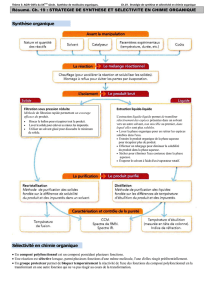
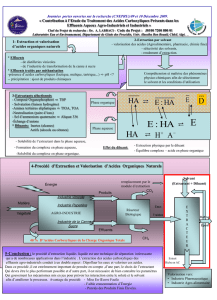
Extraction Liquide-Liquide : Principes et Applications
Telechargé par
sofiane Ben Hamouda

Extraction liquide-liquide
1
Introduction
Les méthodes d’extraction sont parmi les plus utilisées en analyses immédiate. Elles sont utilisées
depuis de nombreuse année à des fin de la récupération, séparation et purification des composés
en utilisant les différences de solubilités mutuelles de certains liquides au laboratoire et dans les
domaines de l’industrie chimique, pharmaceutique et nucléaire. Elle est d’une grande importance
aussi bien pour la valorisation des éléments extraits que pour la protection de l’environnement.
Le but :
La purification et séparations des mélanges liquides
Principe :
Le principe de l'extraction liquide-Liquide est basé sur la distribution d'une espèce métallique M
entre deux phases aqueuse et organique non miscibles. Au cours du transfert, le potentiel
chimique de l'espèce apparue en phase organique augmente, tandis que celui de la phase aqueuse
diminue. A l'équilibre, les potentiels chimiques du soluté M sont égaux dans les deux phases
Partie théorique
Extraction liquide-liquide
C’est une opération fondamentale de transfert de matière entre deux phases liquides non
miscibles, sans transfert de chaleur. Elle consiste à extraire un ou plusieurs constituants d’une
solution par dissolution au contact d’un solvant dans lesquels les corps sont solubles. Cette
opération est fréquemment utilisée pour séparer d’un mélange liquide des constituants dont les
volatilités sont faibles ou très voisines, ou qui donnent des azéotropes, ou encore qui sont thermo-
dégradables.

Extraction liquide-liquide
2
Pour que l’opération soit réalisable il est nécessaire :
- que les deux phases ne soient pas complètement miscibles.
- que leurs masses volumiques soient différentes.
- qu’il n’existe pas de réactions chimiques entre les divers constituants du mélange.
Terminologie :
Soluté : constituant à extraire
Diluant: liquide contenant les solutés
Solution: ensemble soluté + diluant
Solvant: liquide destiné à extraire les solutés
Extrait : phase issue de l’opération contenant les solutés extraits. Cette phase est riche en
solvant
Raffinat : phase résiduelle épuisée en soluté. Cette phase est riche en diluant.
Phase lourde : phase ayant la plus grande masse volumique.
Phase légère : phase ayant la plus faible masse volumique.
Phase aqueuse/Phase organique : ces termes sont liés à la nature du solvant et du diluant.

Extraction liquide-liquide
3
Phase continue/phase dispersée : le terme phase continue, utilisé lors de l’utilisation de colonnes
d’extraction caractérise la phase de «remplissage de la colonne » au sein de laquelle l’autre phase
dite dispersée se présente sous forme de gouttelettes.
Déséxtraction
Opération consistant à faire ressortir le ou les solutés de l’extrait. Le plus souvent, il s’agit d’un
transfert vers une 3ème phase de même nature que la phase d’alimentation, sans pour autant lui
être identique.
L’extractant
Composé possédant le pouvoir de former avec le soluté métallique de la phase aqueuse un
composé organométallique soluble dans la phase organique . Le choix de l’extractant pour un
procédé d’extraction liquide - liquide constitue une étape cruciale pour réaliser une extraction
efficace. Généralement il est déterminé suite à un compromis entre des considérations technico-
économiques et propriétés physico-chimiques, cependant il est impératif que l’extractant
présente un certain nombre de caractéristiques, parmi lesquels on peut citer :
Avoir un fort coefficient de distribution vis-à-vis du soluté à extraire.
Une faible solubilité ou pratiquement une insolubilité dans l’eau, ceci dans le but de
minimiser la perte en extractant dans la phase raffinat et éviter que l’opération se
transforme en un simple transfert de pollution.
Une différence de masses volumiques de l’ordre de 10% entre les phases en présence
(organique et aqueuse) est requise. Ceci dans le but d’assurer une décantation aisée.
Souvent, un deuxième élément est introduit dans la phase organique (diluant) afin d’en
modifier la masse volumique de l’extractant (en l’augmentant ou en l’abaissant suivant son
rapport à la masse volumique de l’eau).
Une viscosité faible moins que 3.10-3 Pascal. Seconde, la valeur de cette dernière
conditionne la quantité d’énergie qu’il faudra fournir au système (agitation, pompes…)
pour assurer une dispersion des phases favorable au transfert de matière.
La tension interfaciale joue un rôle important puisque elle détermine l’efficacité de la
dispersion, une tension interfaciale trop élevée est défavorable à la dispersion réciproque
des phases et par conséquent à un contact efficace. Par contre une valeur trop basse de la
tension interfaciale conduit à la formation d’émulsion stable : la décantation devient alors
quasiment impossible.
Une stabilité physico-chimique, l’extractant ne devra pas se dégrader sous l’effet d’une
oxydation, d’une augmentation de la température ou de pH, il ne devra pas non plus
participer à des réactions non réversibles avec les solutés.
Pour la mise en oeuvre du procédé, la toxicité, l’inflammabilité et la volatilité doivent être
pris en considération. L’extractant utilisé doit être non toxique et non corrosif et pour
éviter des pertes importantes, seules, les extractants peu volatil qui sont utilisés dans un
appareillage ouvert.
Le solvant
Un solvant est un liquide qui à la propriété de dissoudre, de diluer ou d’extraire d’autre substance
sans provoquer de modification chimique de ses substances et sans-lui même se modifier. Les
solvants permettent de mettre en ouvre, d’appliquer, de nettoyer ou de séparer des produits.

Extraction liquide-liquide
4
Les différentes familles de solvants
Les solvants organique sont des hydrocarbures c'est-à-dire des molécules formées d’atomes de
carbone et d’hydrogène. On distingue 8 principaux groupes aux quels s’ajoutent quelques solvants
particuliers :
Hydrocarbure aromatique (Benzène toluène xylène cumène…)
Solvant pétrolière (hors aromatiques : alcanes, alcènes…)
Alcools (méthanol, éthanol, glycols…)
Cétone (acétone, méthyéthylcétone…)
Esters (acétates, agrosolvants…)
Ether de glycol
Hydrocarbures halogénés (chlorés, bromés ou fluorés)
Solvant particuliers (amines, amides, terpénes…)
Propriété des solvants
En général, la phase d'alimentation initiale est imposée, et les possibilités se limitent au choix du
solvant possédant si possible les propriétés suivantes :
• une capacité d'extraction importante avec un rapport de distribution compris entre 5 et 50.
• une grande sélectivité vis-à-vis des solutés indésirables caractérisée par les facteurs de
séparation.
• une solubilité négligeable dans le raffinat.
• une bonne stabilité chimique lors des opérations requises.
• des caractéristiques physiques telles que les temps de séparation de phase et dispersion
soient acceptables : viscosité, tension superficielle, masse volumique.
• un impact minimal vis-à-vis de l'environnement, de la sécurité et de la tenue des Matériaux.
Choix du solvant
Etat physique du solvant
Miscibilité du solvant
Solubilité
Densité du solvant
Les types d’extraction liquide-liquide :
On distingue deux types d’extraction liquide-liquide :
L’extraction par échange d’ions : la phase d’alimentation s’enrichit d’une espèce contenue
dans le solvant pendant que le soluté passe dans le solvant. Elle repose sur une réaction
chimique et l’échange de cations et anions.
L’extraction non-compensée : simple transfert de molécules ou d’agrégats d’ions
globalement neutres. L’extraction peut être faite avec un réactif solvatant, permettant un
transfert résultant d’interactions chimique fortes, ou non solvatant.

Extraction liquide-liquide
5
Les étapes de l’extraction :
Deux opérations doive être effectué pour réaliser une extraction liquide-liquide.
-étape 1 : le mélange intime de deux phases par agitation.
-étape 2 : la séparation des deux phases par décantation.
AGITATION
F. ALIMENTATION E. EXTRAIT
solvant R. RAFFINAT
Les principales étapes sont :
Extraction du soluté : en hydrométallurgie, la phase d'alimentation est généralement aqueuse
et le solvant organique. En pétrochimie, les deux phases sont généralement organiques.
Lavage du solvant qui permet de retirer certaines impuretés extraites et ainsi améliorer
la sélectivité du procédé.
Récupération du soluté de l'extrait. Ceci peut être fait par distillation, évaporation ou nouvelle
extraction liquide-liquide suivie d'un précipitation selon la nature et les propriétés physico-
chimiques du soluté et du solvant.
FIG2. Les étapes de l'extraction du diiode d'une solution aqueuse par le cyclohexane
∞
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
1
/
13
100%