METABOLISME DES ACIDES
GRAS
1

Objectifs
1) Décrire le mécanisme de transfert de l’acylCoA dans
la mitochondrie
2) Décrire les étapes de l’oxydation des acides gras
3) Etablir le bilan en ATP de l’oxydation complète d’un
acide gras saturé
4) Citer les différentes destinées des produits de la β
oxydation
5) Décrire les étapes de la biosynthèse des acides gras
6) Expliquer le mécanisme de régulation du
métabolisme des acides gras
2

PLAN
I. GENERALITES
II. CATABOLISME DES ACIDES GRAS
A. Activation de l’AG
B. Transfert de l’acyl-CoA dans la mitochondrie
C. La βoxydation
1. Oxydation des AG à nombre pair de carbones
2. Oxydation des AG à nombre impair de carbones
3. Oxydation des AG mono-insaturés
4. Oxydation des AG polyinsaturés
D. Destinées de l’acétyl-CoA
3

PLAN
III. BIOSYNTHESE DES ACIDES GRAS
A. Transfert du radical acétyl de la mitochondrie vers le cytosol
B. Synthèse du malonyl-CoA
C. Biosynthèse de l’acide palmitique
1. Condensation de l’acétyl-ACP et du malonyl-ACP
2. Réduction de l’acétoacétyl-ACP
3. Déshydratation du β hydoxybutyryl-ACP
4. Réduction de la double liaison
5. Bilan énergétique et moléculaire de la biosynthèse
D. Biosynthèse des AG mono-insaturés
E. Biosynthèse des AG polyinsaturés
IV. REGULATION DU METABOLISME DES ACIDES GRAS
4

I. GENERALITES
METABOLISME = ANABOLISME +
CATABOLISME
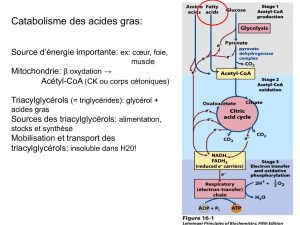
Catabolisme des AG = βoxydation
voie la plus énergétique de l’organisme, fournit 40%
de l’énergie.
processus mitochondrial +++
Produit final: Acétyl-CoA
Biosynthèse : n’est pas l’inverse de la β oxydation
processus extra-mitochondrial (cytosol +++)
Précurseur: Acétyl-CoA
5
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
 37
37
 38
38
 39
39
 40
40
 41
41
 42
42
1
/
42
100%