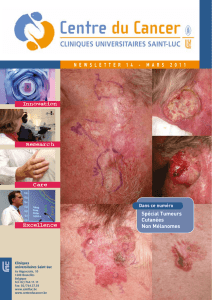
Lésions papulo-nodulaires chroniques et syndrome de Gorlin-Goltz
Telechargé par
Linda Manaa

February 23, 2011
Des lésions papulo-nodulaires chroniques
dermatologie-pratique.com/journal/article/des-lesions-papulo-nodulaires-chroniques
A. AOUSSAR*, M. AIT OURHROUIL*, N. ISMAILI*, F. BELGNAOUI*, Y. AFIFI*, F.
MANSOURI**, A. SEFIANI***, K. SENOUCI*, B. HASSAM* *Service de Dermatologie,
**Service d’anatomie pathologique, CHU Ibn Sina, Rabat, ***Service de Génétique,
Institut national d’hyg
Une patiente de 45 ans, sans antécédents pathologiques particuliers, observait depuis
12 ans l’apparition progressive de multiples lésions papulo-nodulaires intéressant
essentiellement le visage, le décolleté, les aisselles et le dos.
Observation
Une patiente de 45 ans, sans antécédents pathologiques particuliers, observait depuis
12 ans l’apparition progressive de multiples lésions papulo-nodulaires intéressant
essentiellement le visage, le décolleté, les aisselles et le dos.
Figures 1 a et b. Multiples lésions pigmentées, lisses et fermes de tailles diverses sur le
visage.
L’examen clinique, à l’admission, révélait de multiples lésions papulo-nodulaires,
pigmentées, lisses et fermes de quelques millimètres à 3 cm de diamètre localisées sur
1/6

le visage (figures 1 a et b), le décolleté, les aisselles et sur les épaules, ainsi que des
lésions érythémateuses à bordure perlée et de diamètre variant de quelques millimètres
à plusieurs centimètres dans le dos, sur le visage et dans le décolleté (figures 2 et 3).
Figure 2. Carcinomes basocellulaires multiples du visage et du décolleté.
Figure 3. Carcinome basocellulaire nodulaire du dos après intervention
chirurgicale.
Ces lésions étaient fortement évocatrices de carcinomes basocellulaires. On notait
également de multiples molluscums pendulums sur les épaules et les creux axillaires. Il
n’y avait pas de porokératose palmo-plantaire. Par ailleurs, il existait une malformation
du pied gauche (figure 4) avec boiterie et une cataracte corticale de l’œil gauche.
2/6

Figure 4. Malformation du pied gauche due au raccourcissement du 4e
métatarsien.
Quel est votre diagnostic ?
Malgré l’absence de cas similaire dans la famille, un syndrome de Gorlin-Goltz
sporadique a été évoqué.
L’étude anatomopathologique des lésions cutanées a montré des carcinomes
basocellulaires multiples. Le bilan radiologique comportant des radiographies du
squelette osseux, une radiographie du poumon, une échographie abdomino-pelvienne,
ainsi qu’un scanner cérébral, a révélé un raccourcissement du 4e métatarsien gauche et
des calcifications intracrâniennes au niveau de la faux du cerveau et de la tente du
cervelet.
L’étude du matériel génétique a montré un caryotype normal. L’examen des membres de
la famille ne révélait pas de cas similaire.
La patiente a été traitée par électrocoagulation avec curetage pour certaines lésions et
par exérèse chirurgicale pour d’autres.
Une photoprotection externe a été également recommandée.
Discussion
Le diagnostic de syndrome de Gorlin-Goltz doit être évoqué chez tout patient
développant un ou plusieurs carcinomes basocellulaires à un âge jeune.
Aspects génétiques
Le syndrome de Gorlin-Goltz, appelé également syndrome des hamartomes
basocellulaires, est une dysembryoplasie rare se transmettant sur un mode
autosomique dominant avec habituellement une forte pénétrance (97 %) et une
expression variable (1,2). Il a été diagnostiqué pour la première fois par Gorlin-Goltz en
1960 (3). Sa prévalence est estimée entre 1/57 000 et 1/164 000 (4). Grâce à des
études récentes, des progrès importants ont été réalisés dans la compréhension de
l’étiopathogénie du syndrome de Gorlin-Goltz. Il a été démontré que cette maladie
résulte d’une mutation ponctuelle d’un gène tumoro-suppresseur appelé « Patched »
(PTCH). Il s’agit d’un gène de développement présent dans la région 9q22.3-31 (5,6,7).
L’importance de PTCH dans la carcinogenèse basocellulaire a pu être établie grâce aux
techniques de la biologie de développement (5).
Des altérations du gène Patched sont détectées dans les familles atteintes du syndrome
de Gorlin-Goltz, ainsi que dans 50 % des carcinomes basocellulaires sporadiques.
3/6

Aspects cliniques
Cette pathologie s’exprime essentiellement par des manifestations cutanées, osseuses
et neurologiques.
Manifestations cutanées :
– hamartomes basocellulaires précoces à localisation centrofaciale surtout ou
thoracique (1) ;
– carcinomes basocellulaires multiples survenant à l’adolescence ou chez l’adulte jeune
(8), et intéressant surtout la face (3) ;
– puits épidermiques palmo-plantaires, sous forme de petites dépressions minuscules
(8).
Manifestations osseuses : kystes osseux des maxillaires, anomalies costales (côtes
bifides…) (3,8) ; déformations vertébrales (cyphoscoliose, spina bifida…).
Manifestations neurologiques : calcifications intracrâniennes, surtout au niveau de la
faux du cerveau ; débilité mentale (1).
D’autres manifestations ont été décrites telles que les molluscums pendulums (2), les
médulloblastomes (rares), l’hydrocéphalie, l’agénésie du corps calleux, cataracte et
glaucome (1).
Le diagnostic positif repose sur la présence de deux critères majeurs ou l’association
d’un critère majeur et deux critères mineurs (tableau)(4).
Le diagnostic différentiel se pose essentiellement avec le syndrome de Basex qui
associe carcinomes basocellulaires, hypotrichose, hypohidrose et une atrophodermie
folliculaire.
Critères diagnostiques du syndrome de Gorlin-Goltz.
4/6

Le diagnostic se fait en présence de deux critères majeurs ou d’un critère majeur et deux critères
mineurs.
Critères majeurs :
• Plus de deux carcinomes basocellulaires ou un seul apparu avant l’âge de 20 ans.
• Kératokystes odontogéniques des maxillaires prouvés histologiquement.
• Trois ou plus de puits (« pits ») épidermiques palmaires et/ou plantaires.
• Calcifications bilamellaires de la faux du cerveau.
• Anomalies costales : bifurcation, fusion ou déformation.
• Parent du premier degré ayant un syndrome de Gorlin-Goltz.
Critères mineurs :
• Macrocéphalie.
• Malformations congénitales du visage : fente palatine, bosse frontale ou hypertélorisme modéré
ou sévère.
• Autres anomalies squelettiques : déformation de Sprengel, déformation thoracique, syndactylie.
• Anomalies radiologiques : soudure de la selle turcique, anomalies vertébrales telles que des
hémivertèbres, la fusion ou l’élongation des corps vertébraux, anomalies des mains et des pieds.
• Fibromes ovariens.
• Médulloblastomes.
Conclusion
Le diagnostic a été retenu chez notre patiente sur deux critères majeurs que sont les
carcinomes basocellulaires multiples et les calcifications intracrâniennes de la faux du
cerveau, avec en plus d’autres signes en faveur, à savoir : le raccourcissement du 4e
métatarsien gauche, une cataracte de l’œil gauche et des molluscums pendulums. Notre
observation semble être un cas sporadique, vu l’absence de cas similaires dans la
famille.
C’est le deuxième cas colligé dans notre service avec un intervalle de 6 ans. Concernant
l’atteinte acrale de cette maladie, le raccourcissement du 4e métacarpien est
habituellement rapporté dans la littérature, alors que notre malade présentait un
raccourcissement du 4e métatarsien gauche.
L’intérêt de cette observation est de rappeler la nécessité du dépistage précoce de cette
maladie.
Celui-ci repose sur le diagnostic prénatal en cas de forme familiale et sur la présence de
signes prédictifs tels que des hamartomes basocellulaires multiples, des molluscums
pendulums multiples (2) ou encore des malformations osseuses et neurologiques
diverses. Des mesures de photoprotection, ainsi que la surveillance régulière des
malades et de leur descendance est nécessaire pour contrôler les complications
carcinologiques, parfois graves, de cette affection sans oublier l’intérêt du conseil
génétique.
5/6
 6
6
1
/
6
100%