PCSI%Brizeux%TP%N°2%Altmayer-Henzien%2016-2017%
!
TP#N°2#:#RÉACTION#DE#CANNIZZARO#-#PARTIE#1#:#TECHNIQUES#DE#SÉPARATION#
!
Objectif# :%Le% but% de% ce% TP% est% de% mettre% en% œuvre% des% techniques% de% séparation% (de% deux% liquides% non%
miscibles%ou%d'un%mélange%liquide/solide)%à%la%suite%d'une%synthèse.%
!
I. Introduction#:#La#réaction#de#Cannizzaro#
Le%benzaldéhyde%est%utilisé%dans%l'industrie%agro-alimentaire%comme%arôme%(odeur%d'amande%amère).%
En%présence%d'une%solution%aqueuse%d'hydroxyde%de%sodium%(Na+%+%HO−),%le%benzaldéhyde%est%susceptible%
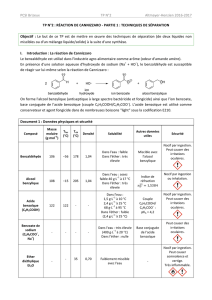
de%réagir%sur%lui-même%selon%la%réaction%de%Cannizzaro%:%
%
On%forme%l'alcool%benzylique%(antiseptique%à%large%spectre%bactéricide%et%fongicide)%ainsi%que%l'ion%benzoate,%
base% conjuguée% de% l'acide% benzoïque% (couple% C6H5COOH/C6H5COO−).% L'acide% benzoïque% est%utilisé% comme%
conservateur%et%agent%fongicide%dans%de%nombreuses%boissons%"light"%sous%la%codification%E210.%
#
Document#1#:#Données#physiques#et#sécurité#
Composé#
Masse#
molaire#
(g·mol−1)#
Tfus#
(°C)#
Teb#
(°C)#
Densité#
Solubilité#
Autres#données#
utiles#
Sécurité#
Benzaldéhyde#
106%
−56%
178%
1,04%
Dans%l'eau%:%faible%
Dans%l'éther%:%très%
élevée%
Miscible%avec%
l'alcool%
benzylique%
Nocif%par%ingestion.%
Peut%causer%des%
irritations%
oculaires.%
%
Alcool#
benzylique#
108%
−15%
205%
1,04%
Dans%l'eau%:%assez%
faible%40%g·L−1%à%17%°C%
Dans%l'éther%:%très%
élevée%
Indice%de%
réfraction%
𝑛!
!" =1,5384%
Nocif%par%ingestion%
ou%inhalation.%
%
Acide#
benzoïque#
(C6H5COOH)#
122%
122%
-%
-%
Dans%l'eau%:%
1,5%g·L−1%à%10%°C%
2,4%g·L−1%à%25%°C%
68%g·L−1%à%95%°C%
Dans%l'éther%:%faible%
(2,4%g·L−1%à%25%°C)%
Couple%
C6H5COOH/%
C6H5COO−%:%
pKA%=%4,2%
Nocif%par%ingestion.%
Peut%causer%des%
irritations%
oculaires.%
%
Benzoate#de#
sodium#
(C6H5COO−,#
Na+)#
-%
-%
-%
-%
Dans%l'eau%:%très%élevée%
(400%g·L−1%à%20%°C)%
Dans%l'éther%:%nulle%
Base%conjuguée%
de%l'acide%
benzoïque%
Peut%causer%des%
irritations%
oculaires.%
%
Ether#
diéthylique#
Et2O#
-%
-%
%
35%
%
0,70%
%
Faiblement%miscible%
avec%l'eau%
-%
Nocif%par%ingestion.%
Peut%causer%
somnolence%et%
vertige.%
Très%inflammable.%
%
H
O
2+HO−O
O
+OH
benzaldéhyde
ion
hydroxyde ion benzoate alcool benzylique

PCSI%Brizeux%TP%N°2%Altmayer-Henzien%2016-2017%
!
II. Travail#préparatoire#
1.#Dans%quel%état%physique%est%l'acide%benzoïque%à%la%température%du%laboratoire%?%C'est%sous%cette%forme%
qu'il%faudra%le%récupérer%en%fin%de%TP.%
%
2.%Calculer% les% quantités% de% matière% des% réactifs% engagés% dans% la% réaction% de% Cannizzaro.% (Donnée&
supplémentaire&:&MNaOH&=&40&g·mol−1)&
&
3.%Déterminer%le%volume%de%benzaldéhyde%qu'il%a%fallu%prélever%ainsi%que%la%quantité%de%matière%maximale%
d'acide%benzoïque%qu'il%est%possible%de%former%si%la%réaction%est%quantitative%(=quasi-totale).%
%
4.%Ecrire% l'équation% de% la% réaction% acido-basique% pouvant% avoir% lieu% entre% l'ion% benzoate% C6H5COO−%et% de%
l'acide%chlorhydrique.%(Donnée&supplémentaire&:&On&précise&que&l'acide&chlorhydrique&est&un&acide&fort&:&dans&
l'eau,& il& forme& H3O+(aq)& et& Cl−(aq).)&Cette% réaction% est% dite% "exothermique% ":% la% température% du% milieu%
réactionnel%augmente.%
#
5.%Tracer%le%diagramme%de%prédominance%de%l'acide%benzoïque.%
Document#2#:#Diagramme#de#prédominance#d'un#couple#acide/base#
Soit%AH/A−%un%couple%acide/base%dont%le%pKA%est%donné.%Le%diagramme%de%prédominance%est%représenté%ci-
dessous%:%
%
%
%
%
III. Séparation#des#produits#formés#lors#de#la#réaction#de#Cannizzaro#
Consignes#:%%
» L’organisation%lors%d’un%TP%est%primordiale.%Avant%de%commencer%la%manipulation,%il#est#obligatoire#de#
lire# intégralement# l’énoncé.# Les% temps% d’attente% devront% être% exploités% au% mieux% (anticipation% des%
prochaines% étapes% du% protocole,% rédaction% du% compte-rendu,% préparation% des% calculs% pour% le%
rendement…).%%
» Il% vous% est% demandé% d’être% particulièrement% vigilants% en% ce% qui% concerne% la% sécurité.% Les% produits%
doivent%être%manipulés%avec%le%matériel#de#protection%adapté.%Vous%veillerez%à%ce%que%votre%paillasse%
soit%en%permanence%propre#et#bien#rangée.%
Sur% votre% paillasse,% se% trouve% un% erlenmeyer% de% 100% mL% contenant% le% milieu% réactionnel% à% l'issue% d'une%
réaction%de%Cannizzaro.%Pour%cela,%2,0%g%d'hydroxyde%de%sodium%ont%été%dissous%dans%4,0%mL%d'eau%puis%5,0%g%
de%benzaldéhyde%ont%été%ajoutés%à%cette%solution%basique.%Un%barreau%aimanté%a%été%introduit%et%le%mélange%
réactionnel%a%été%agité%à%température%ambiante%pendant%48%h%(erlenmeyer%bouché).%
%
On%obtient%ainsi%un%mélange%constitué%principalement%d'alcool#benzylique%et%de%benzoate#de#sodium%dans%
l'eau.%Le%milieu%est%très%basique%(car%HO−%est%en%excès).%Il%peut%éventuellement%rester%du%benzaldéhyde%si%la%
réaction%n'a%pas%été%quantitative%(=%quasi-totale).%
%
Le%but%est%d'effectuer%la%séparation%des%produits%de%la%réaction,%de%manière%à%récupérer#uniquement#l'acide#
benzoïque.#
Utiliser%l'ensemble%des%documents%ainsi%que%les%fiches%TP%distribuées%pour%:%
» Proposer%un%protocole%pour%séparer%les%constituants%du%mélange%;%
» Récupérer%et%isoler%l'acide%benzoïque.%

PCSI%Brizeux%TP%N°2%Altmayer-Henzien%2016-2017%
!
Document#3#:#Matériel#à#disposition#
• Erlenmeyer%contenant%le%mélange%à%séparer%
• Ether%diéthylique%
• Solution% d'acide% chlorhydrique% à% 6% mol·L−1%
(Attention,%solution%très%concentrée)%
• Glace%pilée%
• Erlenmeyers%de%100%mL%
• Eprouvette%graduée%
• Agitateur%magnétique%+%barreau%aimanté%
• Ampoule%à%décanter%+%bouchon%+%support%
• 1%entonnoir%en%verre%
• Cristallisoir%
• Ampoule%de%coulée%+%support%
• Papier%pH%+%baguette%en%verre%+%coupelle%
• 1%entonnoir%Büchner%+%fiole%à%vide%
• Filtres%ronds%
#
IV. Consignes#et#questions#supplémentaires#pour#le#compte-rendu#
%
Document#4#:#Critères#généraux#de#rédaction#d'un#compte-rendu#complet#dans#le#cahier#de#TP#
» Travail%soigné%(lisible,%aéré,%résultats%encadrés).%
» L'objectif%des%manipulations%est%rappelé.%
» S'il% n'est% pas% fourni% dans% l'énoncé% du% TP,% le% protocole%des% manipulations% doit% être% détaillé%:% un%
expérimentateur% avisé% doit% pouvoir% refaire% les% manipulations% à% l'aide% de% votre% compte-rendu.% Un%
schéma#légendé%est%souhaitable.%
» Les%résultats%expérimentaux%et%observations%figurent%clairement.%
» L'exploitation%des% résultats% est% détaillée% avec% rigueur% (les% formules%utilisées% sont% rappelées% ;% les%
courbes%éventuelles% sont% jointes% au% compte-rendu,% munies% de% leur% titre,# légende,% ...% ;% les% calculs#
détaillés%;%les%résultats%sont%présentés%si%possible%avec%leur#incertitude).%
» Les%résultats%sont%validés%par%une%conclusion%objective,%et%éventuellement%comparés%à%des%grandeurs#
tabulées.%
%
Q1.# %Combien% de% phases% y% a-t-il% dans% le% milieu% réactionnel% au% début% du% TP% ?% Donner% la% composition% de%
chacune%des%phases.%
%
Q2.#Réaliser%un%organigramme%bilan%permettant%de% récupérer%et%isoler%l'acide%benzoïque%d'une%part%ainsi%
que%l'alcool%benzylique%d'autre%part.%
%
Q3.%Détailler%le%protocole%mené%pour%séparer%la%phase%contenant%l'ion%benzoate%de%celle%contenant%l'alcool%
benzylique.%Faire%un%schéma%légendé%de%la%verrerie%utilisée%avec%son%contenu.%
%
Q4.%Détailler%le%protocole%mené%pour%isoler%l'acide%benzoïque.%Indiquer%l'aspect%du%produit%obtenu.%
%
Q5.%Indiquer%le%rendement%brut%de%la%synthèse,%calculé%à%partir%de%la%quantité%d'acide%benzoïque%obtenue.%
%
%
Conclusion# :# Un% des% produits% de% la% réaction% de% Cannizzaro,% l'acide% benzoïque,% a% vraisemblablement% été%
isolé,% mais....% comment% en% être% sûrs% ??% Est-ce% bien% le%produit%attendu%?%Est-il% pur%?% On% mettra%en% œuvre%
différentes%techniques%de%purification%et%d'analyse%dans%le%prochain%TP%afin%de%répondre%à%ces%questions.%
%#

PCSI%Brizeux%TP%N°2%Altmayer-Henzien%2016-2017%
!
V. Evaluation#
%
%
Compétences#
Evaluation#
S’approprier#
• Lire% et% comprendre% l’énoncé,% se%
mobiliser% en% cohérence% avec% les%
consignes.%
%
%
%
%
Analyser#
• Proposer% ou% justifier% les% étapes% de%
traitement%d’une%synthèse%organique.%
%
%
%
%
%
Réaliser#
• Respecter%les%consignes%de%sécurité.%
• Organiser%son%poste%de%travail.%
• Mettre% en% œuvre% une% extraction%
liquide-liquide%
• Séparer%un%liquide%et%un%solide%et%laver%
un%solide.%
• Mettre%en%œuvre%une%pesée%«%à%masse%
constante%»%d’un%solide.%
%
Valider#
• Déterminer% le% rendement% d’une%
synthèse.%
%
%
%
%
Communiquer#
• Utiliser%un%vocabulaire%précis.%
• Présenter,% formuler% une% proposition,%
une% argumentation% ou% une% conclusion%
de% manière% cohérente,% complète% et%
compréhensible.%
• Rédiger% un% compte-rendu% soigné% et%
organisé.%
%
Etre#autonome,#faire#
preuve#d’initiatives#
• Travailler%seul,%prendre%des%initiatives.%
• Analyser% ses% difficultés% et% demander%
une%aide%pertinente.%
• Travailler%rapidement.%
%
%
1
/
4
100%