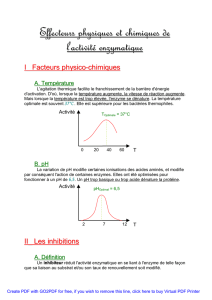
TGF
Faculté de science
Département de biologie
Thème: Les inhibiteurs
enzymatique
R É A L I S É E P A R :
A B D I R A Z A K I B R A H I M A D A N
I D H O U S S E I N A H M E D
S O U M E Y A M A H A M O U D I S M A E L
Z A M Z A M H A S S A N A H M E D

SOMMAIRE
I. Inhibition compétitive (fixation exclusive)
1. Définition
2. Représentation graphique
II. Inhibition non compétitive (fixation non exclusive)
1. Définition
2. Représentation graphique
III. Inhibition incompétitive (fixation non exclusive)
1. Définition
2. Représentation graphique
IV. Inhibition par excès de substrat
1. Définition
2. Représentation graphique

INTRODUCTION
Un inhibiteur enzymatique est une substance se liant à une enzyme et qui
en diminue l’activité.
Un inhibiteur peut empêcher la fixation du substrat sur le site actif en se
fixant à sa place, ou provoquer une déformation de l’enzyme qui rend
celle-ci inactive.
L'étude de l'effet d'inhibiteurs permet :
•d'affiner le mécanisme catalytique d'une réaction enzymatique
•de mieux connaître la spécificité d'une enzyme
•d'obtenir des données physiques et chimiques concernant le site actif
En effet, certains inhibiteurs s'associent de manière réversible à l'enzyme en
interagissant de manière non covalente.
D'autres se fixent de manière Irréversible et sont souvent utilisés
pour déterminer les groupes actifs du site catalytique.

I) INHIBITEUR COMPÉTITIVE
C'est un mécanisme où la fixation de l'inhibiteur empêche celle du
substrat (et réciproquement) : la fixation du substrat et celle de
l'inhibiteur sont donc mutuellement exclusives.
Le mécanisme réactionnel :

LES DIFFÉRENTS MODÈLES :
MODÈLE 1:
Il n'existe qu'un site de fixation pour les deux molécules : la
fixation mutuellement exclusive résulte d'une analogie de
structure entre le substrat et l'inhibiteur.
MODÈLES 2 À 4:
Le substrat et l'inhibiteur se fixent sur des sites distincts.
L'inhibition est malgré tout de type compétitif pour diverses
raisons structurales.
MODÈLE 5:
C'est le changement conformationnel de l'enzyme induit par la
fixation de l'inhibiteur qui empêche celle du substrat (et
réciproquement). Les enzymes sujettes à ce mode de régulation
sont souvent des enzymes multimériques à régulation
allostérique: par exemple, l'aspartate transcarbamylase,
la glutamine synthétase
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
1
/
23
100%