Physiologie cardiaque de grenouille : TP pharmacodynamique

1
Physiologie animale : les grandes fonctions
Compte rendu de TP
Etude de substances pharmacodynamiques
sur le cœur isolé de grenouille
Notre but sera d’étudier les caractéristiques contractiles du cœur isolé de grenouille perfusé par du
liquide de Ringer ainsi que l’action de certaines substance pharmacologique sur la contraction
cardiaque.
I. Généralités
A. Le cœur de grenouille, anatomie macroscopique
La grenouille est un amphibien de l’ordre des anoures. Le cœur isolé de grenouille présente de
faibles exigences quant aux conditions de température, d'oxygénation et de perfusion (méthode par
imbibition). Il est facile d'obtenir sa survie pendant de nombreuses heures par perfusion à l'aide du
liquide de Ringer.
L’activité autonome du cœur est induite par des tissus autonomes disposés au niveau du cœur. Le
cœur de grenouille est assez différent du cœur de mammifère. Il possède 2 oreillettes et un seul
ventricule, ce qui induit un mélange des sangs (oxygéné et non oxygéné) dans l’organisme qui est
expulsé par l’aorte, qui se sépare en 2 branches par la suite.
1 : Nœud de Remak : foyer d’automatisme primaire chez la grenouille.
2 : nœud de Ludwig, 3 : nœud de Bidder : foyers d’automatisme secondaire.
Sinus veineux situé en arrière de
l’oreillette droite : zone de collecte du
sang qui va arriver par les veines caves
Oreillette gauche
Oreillette droite
Ventricule unique
3
2
1
Schéma simplifié du cœur de grenouille
Aorte
Veines caves

2
Le cœur est enveloppé dans le péricarde, qui est constitué de deux couches, le péricarde fibreux et le
péricarde séreux. Le péricarde fibreux est composé de tissu conjonctif dense et résistant et il permet
notamment l’attachement du cœur dans la cavité générale et constitue une protection. Le péricarde
séreux est formé de deux lames, la lame pariétale, qui tapisse la face interne du péricarde fibreux, et
la lame viscérale, qui tapisse le myocarde. Elles sont reliées au niveau des vaisseaux émergeant du
cœur. Les deux lames sont séparées par la cavité du péricarde renfermant un film de sérosité, jouant
un rôle de lubrifiant évitant les frictions entre les deux lames lors des battements cardiaques.
La paroi du cœur est composée de 3 couches : la lame viscérale du péricarde séreux, le myocarde
(muscle cardiaque) et l’endocarde. Le myocarde se compose des cardiomyocytes associés à du tissu
conjonctif qui permet le maintient d’une structure en faisceaux spiralés ou circulaires. Le tissu
conjonctif se compose de fibres de collagène et d’élastine qui tissent un réseau dense, le squelette
fibreux du cœur (renforce le myocarde), qui, au niveau des vaisseaux et des valves cardiaques,
s’épaissit et forme des anneaux fibreux (soutient du point d’émergence du vaisseau dans le cœur). Ce
squelette fibreux permet un parcours bien défini de la contraction cardiaque. L’endocarde est
composé d’un épithélium simple squameux qui tapisse l’intérieur de la cavité cardiaque.
B. Anatomie microscopique du muscle cardiaque.
Les cellules cardiaques ont de nombreuses similitudes avec les fibres musculaires striées
squelettiques. Cependant la cellule musculaire cardiaque détient des caractéristiques propres à son
fonctionnement.
Les cellules musculaires sont appelées cardiomyocytes (littéralement cellule musculaire cardiaque).
Ce sont des cellules courtes, épaisses ramifiées et anastomosées. L’espace intercellulaire est comblé
par un tissu conjonctif, comportant de nombreux capillaires sanguins ( l’endomysium).
Les cellules cardiaques sont étroitement liées. En
effet une contraction coordonnée des cellules est
nécessaire pour un bon fonctionnement du cœur.
La jonction entre 2 cellules est appelée disque
intercalaire. Cette structure est caractérisée par
une ondulation de la membrane plasmique des
deux cellules adjacentes, ce qui permet une bonne
liaison entre les cellules. De plus, on y trouve de
nombreux desmosomes qui permettent le
maintient de la structure lors de la contraction. On
y trouve des jonctions GAP (connexon : assemblage
de molécules de connexine au niveau des
membranes plasmiques de 2 cellules voisines, ce
qui créé une lacune (pore dans la membrane) qui
peut laisser passer des molécules), qui vont
permettent des transferts ioniques, et alors
transmettre le courant dépolarisant dans le tissu
cardiaque. La présence de ce type de jonction
permet à l’ensemble des cellules cardiaques de se comporter comme un syncitium fonctionnel.
Figure 1 : Schéma d'une jonction GAP

3
Le cardiomyocyte comporte 1 ou 2 noyaux en son centre et un grand nombre de mitochondries qui
occupent environ 25 % du volume de la cellule. Les sarcomères présentes des stries A et I, formées
de myosine et d’actine. On trouve également des lignes Z. On note que les myofilaments cardiaques
ont un diamètre variable et sont moins organisés que dans les muscles squelettiques. Ils se ramifient
pour contourner les nombreuses mitochondries présentes dans le sarcoplasme. Les stries sont donc
moins bien définies.
L’organisation des tubules transverses est différente que dans les cellules musculaires. On n’en
trouve qu’un par cellule, plus large, qui pénètre au niveau des lignes Z. Le réticulum sarcoplasmique
est moins développé et on ne trouve pas de citernes terminales, donc il n’y a pas de triades au niveau
des cardiomyocytes, mais ce que l’on appelle diade, une intéraction entre un tubule transverse et un
saccule du réticulum sarcoplasmique.
Sur ce schéma de cardiomyocyte, on
distingue la proximité entre les
saccules du réticulum sarcoplasmique
(2) et le tubule transverse ou
invagination du sarcolemme (T) au
niveau de la ligne Z. L’interaction est
noté (3) sur le Schéma.
La lame basale est représentée
(endomysium) (1) avec ses filament
d’élastine (6).
On retrouve les faisceaux de
myofilaments (4).
On distingue par ailleurs le disque
intercalaire (5), liaison entre 2 cellules
musculaires.
Figure 2 : Schéma général de l'organisation des fibres cardiaques

4
A. Contraction cardiaque
1. Rappel : Contraction musculaire
C’est un muscle strié : le processus de contraction est similaire à celui de la contraction des muscles
striés squelettiques. La libération de calcium dans le cytosol va provoquer la contraction. Le calcium
se fixe sur la troponine C. La troponine C fait partie d’un complexe comprenant également la
troponine I et la troponine T. On trouve ce complexe entre les filaments d’actine et les têtes de
myosines. Fixée à ce complexe on trouve la tropomyosine, qui empêche l’interaction entre myosine
et actine. En faible concentration en Ca2+, il n’y a pas d’interaction entre actine et myosine. En forte
concentration en Ca2+, il y a changement de conformation de la troponine C. Ceci entraine une
modification du complexe des troponines, ce qui déplace la tropomyosine et favorise l’interaction
actine-myosine, et donc à l’activation de l’activité ATPasique des têtes de myosines. On a alors
hydrolyse de L’ATP et ainsi libération d’énergie qui va permettre le glissement des fibres de la
myosine le long des fibres d’actine, entrainant le raccourcissement des fibres musculaires ce qui
correspond au phénomène de contraction.
La reprise du calcium par le RS, grâce à la pompe SERCA (ATP dépendante), provoque une transition
conformationelles du complexe des troponines induisant le masquage du site de liaison des têtes de
myosine. L’actine et la myosine ne peuvent plus se lier. On a donc une relaxation.
2. Automatisme cardiaque
Le cœur possède une activé automatique de contraction, appelé automatisme cardiaque. L’influx
initiateur des contractions part de zones précises et se propage d’une façon bien définie. Ceci
permet au sang d’être expulsé de la cavité cardiaque. Comme il est signalé sur le schéma général du
cœur de grenouille, c’est le nœud de Remak, situé au niveau du sinus veineux, qui va initier la
contraction cardiaque. Si on ligature juste en aval de cette structure, la contraction est inhibée. C’est
une structure qui va envoyer des potentiels d’actions à intervalles réguliers (subit une régulation) qui
vont se propager dans le cœur, selon un parcours bien défini. Le nœud de Bidder, situé à l’apex du
cœur, qui initie les contractions ventriculaires : coupé de l’action des autres nœuds, il génère une
contraction ventriculaire de forte amplitude, à une fréquence relativement lente. Le Nœud de
Ludwig, situé à la liaison entre l’oreillette et le ventricule semble lui coordonner l’action des deux
nœuds. En effet, si on isole le cœur de cette structure (avec une ligature de chaque coté), on observe
une allorythmie (désynchronisation entre la contraction de l’oreillette et du ventricule). On peut
supposer que ce nœud transmet le potentiel d’action émit par le nœud de Remak au nœud de Bidder
pour synchroniser la contraction : on a alors (1) émission du potentiel d’action qui engendre (2) la
contraction de l’oreillette. (3) l’influx passe par le nœud de Ludwig, et est dirigé vers le nœud de
Bidder où il va (4) permettre l’initiation de la contraction du ventricule à partir de ce nœud. On a
ensuite (5) contraction du ventricule, de l’apex vers l’aorte.
Formation de l’impulsion cardiaque : Cet automatisme est possible grâce à des cellules pacemaker
ou cardionectrices. Elles se dépolarisent en permanence du fait d’une baisse de la conductance
potassique, d’une part, et par l’activation d’un courant IH, d’autre part. Le courant IH, correspond à
une augmentation de la conductance de certains cations. Ceux-ci vont diffuser de l’extérieur vers
l’intérieur de la cellule, ce qui va dépolariser lentement la cellule. Le potassium est, lui, séquestré à
l’intérieur de la cellule, ce qui créer un déséquilibre de charges par rapport au flux entrant de cations
qui n’est pas annulé par le flux sortant de potassium.
5
Le potentiel de membrane devient de plus en plus positif. On appelle ce phénomène le prépotentiel.
Le seuil d’excitabilité est alors atteint, ce qui provoque une entrée massive de calcium, par ouverture
des canaux voltage dépendant. L’inversion de polarité engendre la fermeture des canaux calciques,
et l’ouverture des canaux potassiques. Le courant potassique provoque alors une repolarisation de la
membrane de la cellule pacemaker.
Contraction cardiaque : Contrairement aux cellules musculaires squelettiques où seulement le
sodium joue un rôle, le calcium qui joue un rôle également dans les cellules contractiles cardiaques.
Un potentiel d’action particulier est alors initié. Celui-ci comporte une pointe et un plateau et dure
environ 200 ms.
Les canaux sodiques voltage dépendant sont activés par le PA provenant des cellules cardionectrices
(grâce aux jonctions GAP). On a une ouverture de ces canaux qui provoque une entrée brève mais
brutale de sodium. La cellule est dépolarisée, c’est la pointe du PA.
L’inversion de polarité entraine l’ouverture des canaux calciques voltage dépendants, appelés
canaux lent. Ils restent ouverts durant quelques centièmes de secondes et stimulent l’ouverture des
canaux calciques des saccules du réticulum sarcoplasmique. L’augmentation de la concentration de
calcium, nécessaire pour la contraction musculaire, prolonge le potentiel de dépolarisation, formant
le plateau. Ce phénomène est notamment important par rapport à la période réfractaire des fibres.
Lors de la stimulation des dernières fibres au cours du cycle de contraction, les premières sont
encore en période réfractaire, ce qui leur évite d’être à nouveau stimulés (reentry).
Les canaux potassium activés par le changement de polarité, s’ouvrent en même temps que les
canaux calciques pour faire revenir le potentiel de membrane vers le potentiel de repos.
Le calcium est repris dans le RS, par des pompes SERCA (CA++ ATPase) ainsi que dans le milieu
extracellulaire par une CA++ ATPase ou une pompe 3Na/Ca.
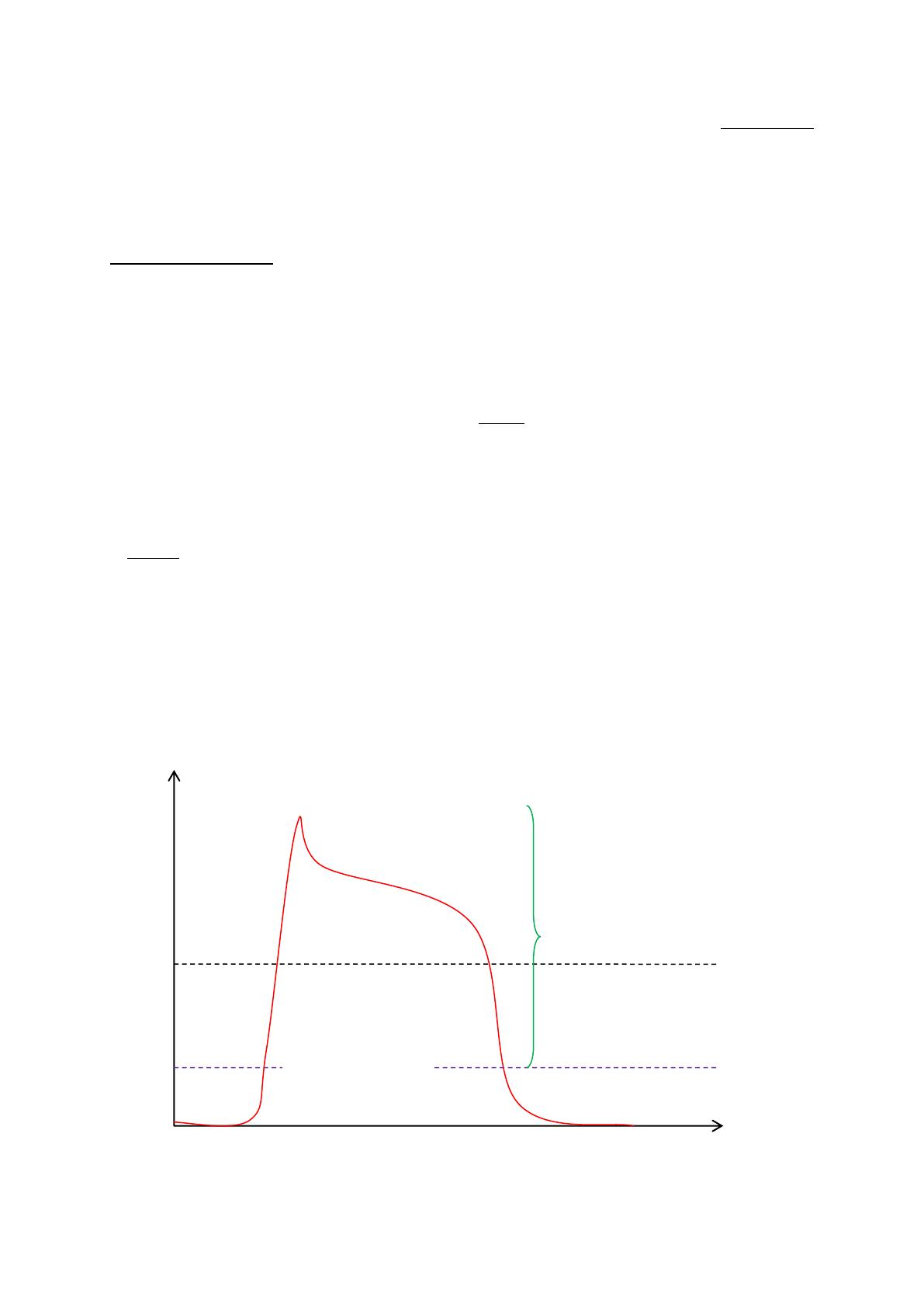
Potentiel de membrane
0 mV
Seuil d’excitabilité
Pointe
Plateau
Potentiel d’action
Temps
200 ms
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
1
/
18
100%