Lire l`article complet

CAS CLINIQUE
La Lettre du Cardiologue • n° 435 - mai 2010 | 29
Mots-clés
Anémie – Hémoglobinopathie – Hypertension pulmonaire – Insuffisance cardiaque
Keywords
Anaemia – Hemoglobinopathy – Pulmonary hypertension – Heart failure
HTAP chez une Antillaise :
penser à la drépanocytose !
PAHT in a caribbean woman: consider sickle-cell anemia
P.H. Gacon*
* Service de cardiologie clinique et interventionnelle, CHU de Dijon.
N
ous rapportons l’observation d’une patiente de 49 ans,
d’origine antillaise, hospitalisée pour une scène d’in-
suffisance cardiaque droite révélatrice d’une hémoglo-
binopathie SS, précédée d’une dyspnée d’effort du stade II de
la classification NYHA liée à une anémie chronique. Madame P.
est hospitalisée pour une insuffisance cardiaque droite récente
avec une prise de poids de 5 kilos, des œdèmes des membres
inférieurs, une hépatalgie douloureuse pulsatile avec une
turgescence jugulaire spontanée. Le seul antécédent est une
anémie d’étiologie inexpliquée à l’origine d’une tachycardie
sinusale et d’un souffle systolique éjectionnel mésocardiaque
découvert durant l’enfance.
Observation
Sa tension artérielle est symétrique et normale aux deux bras
à 125/70 mmHg, la patiente est en tachycardie sinusale à
95 bpm et l’on constate une insuffisance ventriculaire droite
associant des œdèmes des membres inférieurs, une hépatalgie
pulsatile et une turgescence jugulaire avec un souffle xyphoï-
dien d’insuffisance tricuspidienne 2/6. Il existe un éclat de B2P
au foyer pulmonaire. L’auscultation pulmonaire est libre et
la palpation thoracique montre un hydrothorax droit dont la
ponction est de culture négative, sans cellules néoplasiques,
avec protéinémie inférieure à 30 g/l.
L’électrocardiogramme en tachycardie sinusale montre une
hypertrophie ventriculaire droite, un axe de QRS dévié à droite,
un espace PR normal et une onde T négative en V1, V2, V3.
La radiographie du thorax montre une cardiomégalie modérée,
une dilatation bilatérale des artères pulmonaires et un hydro-
thorax droit minime.
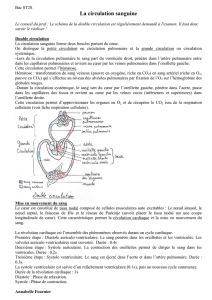
L’échocardiographie confirme une dilatation ventriculaire
droite avec une surface télédiastolique du ventricule droit à
40 cm2, une cinétique septale paradoxale évoquant une surcharge
en pression/volume du ventricule droit et un indice de Tei VD à 0,62.
L’on constate une insuffisance tricuspide de grade 3 de vélocité maxi-
male à 3,33 m/s attestant d’une HTAP avec PAP systolique entre
50 et 55 mmHg et une PAP diastolique entre 17 et 22 mmHg. Le
rapport VD/VG est à 1,2 (figure 1). Le VG est normal, sans fibrose
sous-endocardique ni aspect de cardiomyopathie restrictive, et le
doppler pulsé transmitral est lui aussi normal. Le doppler veineux
des 4 membres élimine une thrombose veineuse profonde. Le dosage
des D-dimères est normal ainsi que la scintigraphie pulmonaire de
ventilation-perfusion.
Le cathétérisme cardiaque droit confirme l’HTAP précapillaire, la
pression artérielle pulmonaire étant à 55/22 mmHg (moyenne de
26 mmHg), pour une PAP à 3 mmHg, sans modification pendant le
test du NO inhalé (50 ppm). Le débit cardiaque est de 5,9 l/mn et
les résistances pulmonaires à 310 dynes/s/cm-5.
Les gaz du sang artériel sont normaux, ainsi que les résultats des
explorations fonctionnelles pulmonaires.
Le bilan biologique révèle une anémie microcytaire hypochrome
(Hb à 9 g/dl) régénérative. Il n’y a pas de syndrome inflammatoire
ni d’insuffisance rénale. Les sérologies des hépatites B, C et VIH sont
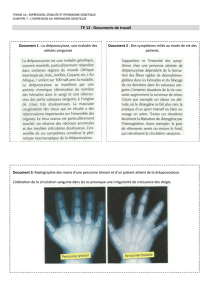
négatives et le bilan thyroïdien est normal. L’électrophorèse de l’hémo-
globine témoigne de l’existence d’une hémoglobine moins mobile
que l’hémoglobine fœtale à pH 8,6 ou que l’hémoglobine A, dite
“hémoglobine S”, mesurée à 40 % (figure 2). Le test de falciformation
(test d’EMMEL) révèle sur la lame l’existence d’hématies falciformes
minces et déformées en faucille rapportée à la polymérisation de
l’hémoglobine et à l’elliptocytose (figure 3).
Discussion
La drépanocytose est une maladie héréditaire initialement décrite
dans la race noire, mais aussi chez les védiques en Inde, les éti-turcs,
les Grecs, les Israéliens et les habitants d’Arabie du Sud, ce qui fait
douter du caractère absolu de la “discrimination raciale” du trait
drépanocytaire. Dès 1904, Herrich rapporta le cas d’un Antillais
atteint d’ictère, de dyspnée, de douleurs rhumatismales et d’ul-

CAS CLINIQUE
▼ Figure 3. Hématies falciformes avec elliptocytose.
▲ Figure 1. A. Dilatation de l’anneau tricuspidien. B. Insuffisance tricuspide de grade 3, Vmax à 3,23 m/s. C. Dilatation avec surcharge en pression du volume
du ventricule droit. D. Dilatation majeure de l’oreillette droite.
▼ Figure 2. Électrophorèse de l’hémoglobine avec Hb S.
C 1 2 3 4 5 6 7
Origine
Anhydrase carbonique
HbC, A2
HbS
HbF
HbA
A
C
B
D
30 | La Lettre du Cardiologue • n° 435 - mai 2010
cères de jambe. Beet en 1949 montre qu’à l’état homozygote
(hémoglobine SS) il s’agit d’une anémie sévère dite “sickle cell
anemia” et qu’à l’état hétérozygote AS (hémoglobine S < à 50 %) la
maladie est asymptomatique. Les hémoglobines S et C, et le gène
thalassémique (hémoglobine F) se transmettent, selon les lois de
Mendel, sur le mode autosomique récessif, aux hétérozygotes AS,
aux homozygotes SS, aux doubles hétérozygotes ou aux hétéro-
zygotes composites SC, AS et bêta-thalassémie. En Afrique, selon
l’haplotype, l’incidence du trait varie de 12 à 39 %, et la mortalité
est importante chez les enfants, ce qui contraste avec le fait que la
maladie n’est en règle générale découverte que chez les adultes en
Europe. Dès 1975, E. Bertrand et al. publient les résultats d’une série

CAS CLINIQUE
La Lettre du Cardiologue • n° 435 - mai 2010 | 31
de 476 adultes dont 0,9 % d’hétérozygotes sans myocardiopathie
et 2 % d’homozygotes avec atteinte myocardique (1). Des études
ont ensuite démontré que 83 % des sujets homozygotes ont des
anomalies cardiaques alors que 1 % des hétérozygotes présentent
des anomalies telles qu’un souffle cardiaque, une cardiomégalie
et des troubles peu spécifiques de la repolarisation. L’insuffisance
cardiaque létale fréquente chez l’enfant est associée à l’incidence
multipliée par 10 d’endocardite infectieuse à pneumocoque et
à Haemophilus influenza. Par ailleurs, l’altération de la plasti-
cité globulaire avec hyperviscosité inhabituelle lors d’anémie,
les vaso-occlusions artériolaires coronaires et la désaturation
artérielle modifient la fonction cardio-pulmonaire. On distingue
classiquement les cœurs anémiques, les myocardiopathies et les
cœurs pulmonaires.
Le cœur anémique associe une élévation du débit cardiaque de
repos et une augmentation des volumes ventriculaires et des
indices de contractibilité.
Les myocardiopathies s’expriment par un tableau de dysfonc-
tion systolique ventriculaire gauche chez les homozygotes. Les
infarctus du myocarde transmuraux sont rarement décrits dans
les séries coronarographiques ainsi que l’hypertension artérielle
systémique, qui doit faire redouter l’existence d’une complication
rénale associée (1-3). Cliniquement, il est difficile de distinguer
les signes congestifs de stase veineuse par augmentation de la
précharge d’un ventricule normal résultant d’une anémie des
signes de dysfonction ventriculaire liés à une atteinte drépano-
cytaire. Les études hémodynamiques cons tatent la normalité du
réseau coronaire et l’augmentation du débit cardiaque (4, 5). Une
myocardiopathie peut éventuellement compliquer l’évolution de
la drépanocytose par des crises de vaso-occlusions avec des foyers
d’infarcissement évoluant vers la fibrose cardio-pulmonaire,
qui limite l’adaptation de la fonction contractible ventriculaire
gauche classiquement conservée dans l’anémie falciforme.
Les cœurs pulmonaires
Les explorations hémodynamiques chez les drépanocytaires
révèlent des pressions pulmonaires normales et une diminu-
tion des résistances vasculaires pulmonaires moindre que dans
les anémies classiques. L’épreuve d’effort peut les démasquer.
La répétition d’accidents vaso-occlusifs artériolaires pulmo-
naires responsables d’infarctus pulmonaires et l’obstruction
extensive des vaisseaux pulmonaires entraînent un tableau de
cœur pulmonaire chronique et conduisent à une diminution
progressive de la capacité efficace du lit pulmonaire et à une
augmentation des résistances pulmonaires. L’élévation variable
des pressions pulmonaires dépend de l’étendue de l’obstruction
pulmonaire et de l’adaptation de son débit, qui est augmenté chez
le drépanocytaire au repos, les pressions pulmonaires augmen-
tant plus que chez le sujet normal pour une même amputation
du lit vasculaire pulmonaire. De plus, les phénomènes de shunt
gauche droit intrapulmonaire et de désaturation artérielle en
oxygène accentue l’élévation du débit cardiaque, favorisant ainsi
l’élévation des pressions pulmonaires. Il faut que plus des deux
tiers du lit vasculaire pulmonaire soient obstrués pour que des
troubles hémodynamiques sévères apparaissent ; il n’est donc
pas surprenant que le cœur pulmonaire chronique soit rare chez
l’enfant drépanocytaire et fréquent chez l’adulte.
La classification révisée de l’HTAP lors du Word Symposium de
Venise en 2003 (6) inclut l’HTAP associée aux hémoglobinopathies
dans le groupe des HTAP associées aux dysthyroïdies, à la maladie
de Gaucher, aux syndromes myéloprolifératifs, à la splénectomie
et aux télangiectasies.
L’étape diagnostique élimine les HTAP dites “secondaires”. Les
explorations fonctionnelles respiratoires, les gaz du sang artériels
et la tomodensitométrie sont des examens essentiels afin d’éli-
miner une pathologie respiratoire chronique sous-jacente et/ ou
un syndrome d’apnée du sommeil couplés à une scintigraphie
pulmonaire de ventilation-perfusion à la recherche d’une maladie
veineuse thrombo-embolique chronique (7).
Conclusion
Le diagnostic de l’HTAP chez le patient drépanocytaire adulte doit
être fait systématiquement devant toute scène d’insuffisance
cardiaque droite. Son traitement repose sur des mesures préven-
tives telles que le repos, l’hydratation (en pays chaud, notamment),
la prescription d’antalgiques et d’acide folique, l’utilisation ration-
nelle de la transfusion sanguine avec dépistage systématique de
l’infection à VIH et des hépatites B et C, la prophylaxie stricte de
l’endocardite infectieuse et la vaccination antipneumococcique. Les
cytostatiques comme l’Hydrea® ainsi que l’exsanguino-transfusion
se justifient en cas de crises vaso-occlusives fréquentes. ■
1. Bertrand E, Chauvet J, Lebras M et al. Les signes cardiaques dans la drépano-
cytose de l’adulte. À propos de 111 cas homozygotes ou hétérozygotes. Cardio-
logie tropicale 1975;1:63-1.
2. Botreau-Roussel P, Dobrinski G, Levy R et al. Infarctus du myocarde et dré-
panocytose hétérozygote. À propos de 2 cas. Arch Mal Cœur 1977;70:141-7.
3. Bertrand E. Signes hémodynamiques et écho-cardiographiques de la drépa-
nocytose. Arch Mal Cœur 1989;82;1881-4.
4. Louis-Gustave A, Louis-Gustave R. Signes cardiovasculaires de la drépano-
cytose. À propos de 62 cas. Arch Mal Cœur 1977;70:135-40.
5. Gacon PH, Donatien Y. Les manifestations cardiaques de la drépanocytose.
Presse Med 2001;30:841-5.
6. Simonneau G, Galie N, Rubin LJ et al. Clinical classification of pulmonary
hypertension. J Am Coll Cardiol 2004;43:55-125.
7. Galie N, Hoeper MM, Humbert M et al. Guidelines for the diagnosis and treat-
ment ot pulmonary hypertension: the task force for the diagnosis and treate-
ment of pulmonary hypertension of the European Society of cardiologie (ESC)
and European Respiratory Society (ERS). Eur Heart J 2009;30(20):2493-537.
Références bibliographiques
1
/
3
100%